3,024g kim loại M+hno3 loãng--> 940,8(ml) NxOy
d NxOy/H2= 22 tìm cthh NxOy
help me, please
Cho 3,024 g một kim loại M tan hết trong dd HNO3 loãng, thu được 940,8 ml khí NxOy(đktc) có tỉ khối đối với H2 bằng 22. Khí NxOy và kim loại M là
Cho 3,024 gam một kim loại M tan hết trong dung dịch HNO3 loãng, thu được 940,8 ml khí NxOy (sản phẩm khử duy nhất ở đktc) có tỉ khối đối với H2 bằng 22. Khí NxOy và kim loại M là:
A. NO và Mg
B. N2O và Al
C. N2O và Fe
D. NO2 và Al
Đáp án B:
![]()
có 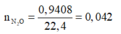
Gọi n là hóa trị của kim loại M. Các quá trình nhuờng và nhận electron:
Quá trình nhường electron: ![]()
Quá trình nhận electron: ![]()
Áp dụng định luật bảo toàn mol electron, ta có: ![]()
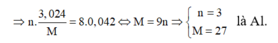
Cho 3,024 gam một kim loại M tan hết trong dung dịch HNO3 loãng, thu được 940,8 ml khí NxOy (sản phẩm khử duy nhất, ở đktc) có tỉ khối đối với H2 bằng 22. Khí NxOy và kim loại M là
A. NO và Mg.
B. N2O và Al
C. N2O và Fe.
D. NO2 và Al.
Đáp án B
MKhí = 22 chứng tỏ NxOy là N2O duy nhất
nN2O = 0,042 mol
2N+5+ 8e → N2O M→Mn++ne
0,336 0,042
BT e ⇒ne = 0,036 mol⇒nM = 0,036 /n
Khi đó M=3,024/ (0,336:n)
M=9n ⇒ n=3, M=27⇒ Chọn Al
\(\dfrac{d_k}{d_{H2}}=22\) => dk = 44 => NxOy là N2O
Ta có: nN2O = 0,03 mol
Gọi n là hóa trị của kim loại M
Bảo toàn e: \(\dfrac{2,16}{M}.n\) = nN2O . 8 = 0,24
Vì M là kim loại nên n ∈ \(\left\{1;2;3\right\}\)
Thay các giá trị của n thì được n = 3 cho M = 27 là thỏa mãn
=> M là Al
Cho 7,8 gam hỗn hợp X gồm kim loại M và Al (có tỉ lệ mol tương ứng 1 : 2) tan hết trong dung dịch HNO3 loãng dư, thu được 2,24 lít khí NxOy (sản phẩm khử duy nhất, ở đktc) có tỉ khối đối với H2 bằng 22. Tìm công thức khí NxOy và kim loại M.
MNxOy = 22.2 = 44(g/mol)
=> N2O
\(n_{N_2O}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Gọi số mol của M và Al là a, 2a
=> a.M + 54a = 7,8 (1)
M0 - ne --> M+n
a--->an
Al0 -3e --> Al+3
2a->6a
2N+5 +8e --> N2+1
_____0,8<--0,1
Bảo toàn e: an + 6a = 0,8
=> \(a=\dfrac{0,8}{n+6}\) (2)
Thay (2) vào (1), ta có:
\(\dfrac{0,8.M}{n+6}+54.\dfrac{0,8}{n+6}=7,8\)
=> 0,8.M + 43,2 = 7,8(n+6)
=> M = \(\dfrac{39}{4}n+\dfrac{9}{2}\)
Xét n = 1 => L
Xét n = 2 => M = 24(Mg)
Cho sơ đồ phản ứng của kim loại M với HNO 3 như sau : M + HNO 3 → M NO 3 n + N x O y + H 2 O
Sau khi cân bằng PTHH, hệ số tối giản của HNO 3 là
A. (3x - 2y)n
B. (3x - y)n
C. (2x - 5y)n
D. (6x - 2y)n
mn ơi giúp mình bài này với:
hợp chất NxOy,có d NxOy/O2 là 3,375
a.lập CTHH của hợp chất biết N chiếm 25,93% về khối lượng
b.1 lít khí NxOy ở ĐKTC nặng bao nhiêu gam và chứa bao nhiêu Phân tử
a) M(NxOy)=3,375.32=108(g/mol)
Vì NxOy có 25,93% khối lượng N, nên ta có:
14x= 108.25,93%=28 =>x=2
16y=108-28=80 => y=5
Với x=2; y=5 => CTHH là N2O5.
b) Khối lượng của 1 lít khí NxOy ở đktc:
1/22,4 x 108\(\approx\) 4,821(g)
1 lít khí NxOy ở đktc chứa số phân tử:
1/22,4 x 6 x 1023= 2,679.1022 (phân tử)
(Lên lớp cao em sẽ học số chính xác là x 6,023.1023 chứ không phải x 6.1023 nữa nè)
Chúc em học tốt!
FexOy + HNO3 → Fe(NO3)3 + NxOy + H2O
Fe3O4 + HNO3 → Fe(NO3)3 + NxOy + H2O
Cân bằng 2 pt trên
cho 3,024g một kim loại M tan hết trong dd HNO3 loãng, thu đc 940,8 ml khí N2O( sản phẩm khử duy nhất,ở đktc). Xác định kim loại M