khi phân tích một mẫu quặng người ta thấy có 2,8g Fe. Tính xem trong mẫu quặng đó có bao nhiêu gam Fe2O3 ứng với lượng sắt trên

Những câu hỏi liên quan
Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một lạo quặng sắt (thành phần chính là
F
e
2
O
3
). Khi phân tích mẫu quặng này, người ta nhận thấy có 2,8g sắt. Trong mẫu quặng trên, khối lượng sắt (III) oxit
F
e
2
O
3
ứng với hàm lượng sắt nói trên là: A. 6g. B. 8(g). C.4g. D.3g. Hãy chọn đáp số đúng...
Đọc tiếp
Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một lạo quặng sắt (thành phần chính là F e 2 O 3 ). Khi phân tích mẫu quặng này, người ta nhận thấy có 2,8g sắt. Trong mẫu quặng trên, khối lượng sắt (III) oxit F e 2 O 3 ứng với hàm lượng sắt nói trên là:
A. 6g. B. 8(g). C.4g. D.3g.
Hãy chọn đáp số đúng.
Phương trình hóa học:
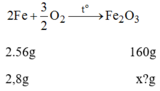
Khối lượng F e 2 O 3 ứng với lượng sắt trên là:
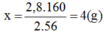
→ Chọn C.
Đúng 0
Bình luận (0)
Khi phân tích một mẫu quặng sắt,người ta thấy có 2,8g sắt .Tính xem trong mẫu quặng đó có bao nhiêu gam sắt(III) oxit Fe2O3 ứng với lượng sắt trên
Xem chi tiết
1 mol sắt 3 oxit năng 160g chứa 112g Fe
=>với 2,8g fe thì khối lượng oxit là 2,8*160/112
Đúng 0
Bình luận (0)
nFe=\(\frac{2,8}{56}=0,05\left(mol\right)\)
nF2O3=1/2.nFe=1/2.0,05=0,025mol
mFe2O3=0,025.160=4g
Đúng 0
Bình luận (0)
Bài 3: Khi phân tích một mẫu quặng bôxit (chứa Al,O,), người ta thấy có 5,4 g nhôm. Tính xem trong mẫu quặng đó có bao nhiêu gam nhôm oxit Al,O, ứng với lượng nhôm trên
\(Al_2O_3\\ n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ \Rightarrow n_O=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ m_{Al_2O_3}=0,2.27+0,3.16=10,2\left(g\right)\)
Đúng 0
Bình luận (1)
1) Đốt cháy sắt thu được 0,3 mol Fe3O4.Tính thể tích khí oxi (ở đktc) đã dùng2) Đốt cháy sắt thu được 0,2 mol Fe3O4. Thể tích khí oxi (ở đktc ) đã dùng là bao nhiêu ?3) Trong x gam quặng sắt hematit có chứa 5,6g Fe. Khối lượng Fe2O3 có trong quặng đó là:4) Muốn điều chế được 3,36 lít oxi (đktc) thì khối lượngKMnO4 cần nhiệt phân là bao nhiêu, viết phương trình điều chế.5) Trong oxit, kim loại có hóa trị III và chiếm 70 phần trăm về khối lượng là:6) Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa...
Đọc tiếp
1) Đốt cháy sắt thu được 0,3 mol Fe3O4.Tính thể tích khí oxi (ở đktc) đã dùng
2) Đốt cháy sắt thu được 0,2 mol Fe3O4. Thể tích khí oxi (ở đktc ) đã dùng là bao nhiêu ?
3) Trong x gam quặng sắt hematit có chứa 5,6g Fe. Khối lượng Fe2O3 có trong quặng đó là:
4) Muốn điều chế được 3,36 lít oxi (đktc) thì khối lượngKMnO4 cần nhiệt phân là bao nhiêu, viết phương trình điều chế.
5) Trong oxit, kim loại có hóa trị III và chiếm 70 phần trăm về khối lượng là:
6) Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa 90g nước để tạo thành axit photphoric. Tính khới lượng axit H3PO4 được tạo thành ?
3Fe+2O2-to>Fe3O4
0,9-----0,6--------------0,3
=>VO2=0,6.22,4=13,44l
2
3Fe+2O2-to>Fe3O4
0,4--------0,2
=>VO2=0,4.22,4=8,96l
Đúng 3
Bình luận (0)
Muối ăn gồm 2 nguyên tố hoá học là Na và Cl Trong đó Na chiếm39,3% theo khối lượng .Hãy tìm công thức hoá học của muối ăn ,biết phân tử khối của nó gấp 29,25 lần PT Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một loại quặng sắt. Khi phân tích mẫu quặng này người ta nhận thấy có 2,8 gam sắt. Trong mẫu quặng trên, khối lượng Fe2O3 ứng với hàm lượng sắt nói trên là: A. 6 gam B. 8 gam C. 4 gam D. 3 gam
Đọc tiếp
Muối ăn gồm 2 nguyên tố hoá học là Na và Cl Trong đó Na chiếm39,3% theo khối lượng .Hãy tìm công thức hoá học của muối ăn ,biết phân tử khối của nó gấp 29,25 lần PT Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một loại quặng sắt. Khi phân tích mẫu quặng này người ta nhận thấy có 2,8 gam sắt. Trong mẫu quặng trên, khối lượng Fe2O3 ứng với hàm lượng sắt nói trên là: A. 6 gam B. 8 gam C. 4 gam D. 3 gam
Muối ăn gồm 2 nguyên tố hoá học là Na và Cl Trong đó Na chiếm39,3% theo khối lượng .Hãy tìm công thức hoá học của muối ăn ,biết phân tử khối của nó gấp 29,25 lần PT Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một loại quặng sắt. Khi phân tích mẫu quặng này người ta nhận thấy có 2,8 gam sắt. Trong mẫu quặng trên, khối lượng Fe2O3 ứng với hàm lượng sắt nói trên là: A. 6 gam B. 8 gam C. 4 gam D. 3 gam
Đọc tiếp
Muối ăn gồm 2 nguyên tố hoá học là Na và Cl Trong đó Na chiếm39,3% theo khối lượng .Hãy tìm công thức hoá học của muối ăn ,biết phân tử khối của nó gấp 29,25 lần PT Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một loại quặng sắt. Khi phân tích mẫu quặng này người ta nhận thấy có 2,8 gam sắt. Trong mẫu quặng trên, khối lượng Fe2O3 ứng với hàm lượng sắt nói trên là: A. 6 gam B. 8 gam C. 4 gam D. 3 gam
=>%mCl =100-39,3=60,7%
Đặt CTHH cần tìm là : NaxCly
=> x:y=\(\dfrac{39,3}{23}:\dfrac{60,7}{35,5}\) =1,7:1,7=1:1
=>CTHH cần tìm là : NaCl
CTHH của quặng sắt là FeS2
PTHH:
\(4FeS_2+11O_2-->2Fe_2O_3+8SO_2\)
0,05___________________0,025
\(Fe_2O_3+3H_2-->2Fe+3H_2O\)
0,025______0,075_____0,05
=>\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
=>\(m_{Fe_2O_3}=0,025.160=4\left(g\right)\)
=> C
(Bạn gì đó ơi lần sau vt đề rõ hơn một chút nhé D:)
Đúng 0
Bình luận (0)
A là một loại quặng sắt chứa 60% Fe2O3; B là loại quặng sắt khác chứa 69,6% Fe3O4. Hỏi trong một tấn quặng A hoặc B có chứa bao nhiêu kg sắt? 2. Trộn quặng A với quặng B theo tỉ lệ khối lượng mA:mB = 2:5 ta được quặng C có bao nhiêu kg sắt
Câu 72) khi phân tích một mẫu quặng apatit Ca3(PO4)2 có chứa 6,1 g P. Hỏi mẫy quặng trên có chứa bao nhiêu gam Ca3(PO4)2 A . 32g B. 31g C.30,5g D. 41g
$n_P = \dfrac{6,1}{31} = 0,2(mol)$
Bảo toàn nguyên tố với P :
$n_{Ca_3(PO_4)_2} = \dfrac{1}{2}n_P = 0,1(mol)$
$m_{Ca_3(PO_4)_2} = 0,1.310 = 31(gam)$
Đáp án B
Đúng 4
Bình luận (0)
đốt 20g một mẫu quặng lưu huỳnh cần hết 16g khí oxi. Sau khi phản ứng xảy ra hoàn toàn thấy có 32g khí lưu huỳnh dioxit sinh ra.
a.viết PTHH
b.tính thành phần % khối lượng lưu huỳnh có trong mẫu quặng đó
(em cần gấp ạ)
PTHH : S + O2 ------> SO2
Áp dụng định luật bảo toàn khối lượng ta có :
mS + mO2 = mSO2
=> mS= mSO2- mO2
=32-16 = 16 (g)
Thành phần % khối lượng lưu huỳnh có trong mẫu quặng đó là
%mS = 16:32.100%=50%
Đúng 0
Bình luận (1)
a. PTHH: 4FeS2 + 11O2 ---to---> 2Fe2O3 + 8SO2
b. Ta có: \(n_{SO_2}=\dfrac{32}{64}=0,5\left(mol\right)\)
=> \(m_{S_{\left(FeS_2\right)}}=m_{S_{\left(SO_2\right)}}=0,5.32=16\left(g\right)\)
=> \(\%_{m_{S_{\left(FeS_2\right)}}}=\dfrac{16}{20}.100\%=80\%\)
Đúng 0
Bình luận (0)






















