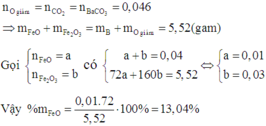Cho CO + 0,04 mol hỗn hợp FeO and Fe2O3 thu được chất rắn gồm 4 chất nặng 4,784 gam và khí X. X+Ba(OH)2 thu được 9,062 gam kết tủa. Tính % mFe2O3 trong hỗn hợp ban đầu ?

Những câu hỏi liên quan
Cho một luồng CO qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 đốt nóng. Sau khi kết thúc thí nghiệm thu được chất rắn B gồm 4 chất, nặng 4,784 gam. Khí đi ra khỏi ống sứ cho hấp thụ vào dung dịch Ba(OH)2 dư thu được 9,062 gam kết tủa. Khối lượng của FeO, Fe2O3 trong 0,04 mol hỗn hợp A lần lượt là A. 0,72g và 4,6g B. 0,84g và 4,8g C. 0,84g và 4,8g D. 0,72g và 4,8g
Đọc tiếp
Cho một luồng CO qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 đốt nóng. Sau khi kết thúc thí nghiệm thu được chất rắn B gồm 4 chất, nặng 4,784 gam. Khí đi ra khỏi ống sứ cho hấp thụ vào dung dịch Ba(OH)2 dư thu được 9,062 gam kết tủa. Khối lượng của FeO, Fe2O3 trong 0,04 mol hỗn hợp A lần lượt là
A. 0,72g và 4,6g
B. 0,84g và 4,8g
C. 0,84g và 4,8g
D. 0,72g và 4,8g
n B a C O 3 = 0,046 mol
Các phản ứng có thể xảy ra khi cho CO đi qua hỗn hợp A:
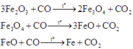
Do đó 4 chất trong hỗn hợp B gồm Fe, FeO, Fe3O4 và Fe2O3 và khí thoát ra là CO2. Khi hấp thụ CO2 vào dung dịch Ba(OH) dư:
![]()
Do đó ![]()
Từ đây, ta có một số cách để tính khối lượng của hỗn hợp ban đầu như sau:
Cách 1: Áp dụng định luật bảo toàn khối lượng
Quan sát các phương trình phản ứng, ta có
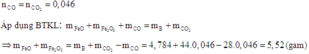
Cách 2: Tăng giảm khối lượng
Nhận thấy: Cứ mỗi phân tử CO lấy một nguyên tử O từ oxit tạo thành 1 phân tử CO2 thì khối lượng chất rắn giảm 16 gam.
Do đó để tạo thành 0,046 mol CO2 thì khối lượng chất rắn đã giảm: 16.0,046 = 0,736 (gam)
Nên m c h ấ t r ắ n b a n đ ầ u = m B + m g i ả m = 4,784 + 0,736 = 5,52 (gam)
Cách 3: Sử dụng hệ quả của định luật bảo toàn khối lượng trong phản ứng nhiệt luyện
Quan sát đặc điểm của các phương trình phản ứng cũng như kiến thức - phương pháp đã nêu ở phần trên ta có:
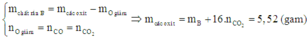
Khi đã biết tổng khối lượng hỗn hợp ban đầu và tổng số mol các chất trong hỗn hợp ban đầu, để tính được số mol cụ thể của từng chất ta tiến hành lập hệ:
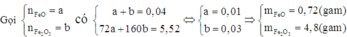
Đáp án D.
Đúng 0
Bình luận (0)
Cho luồng khí CO đi qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 đốt nóng. Sau khi kết thúc thí nghiệm thu được B gồm 4 chất nặng 4,784 gam. Khí đi ra khỏi ống sứ cho hấp thụ vào dung dịch Ba(OH)2 dư thì thu được 9,062 gam kết tủa. Phần trăm khối lượng Fe2O3 trong hỗn hợp A bằng: A. 86,96% B. 76,01% C. 73,04% D. 66,01%
Đọc tiếp
Cho luồng khí CO đi qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 đốt nóng. Sau khi kết thúc thí nghiệm thu được B gồm 4 chất nặng 4,784 gam. Khí đi ra khỏi ống sứ cho hấp thụ vào dung dịch Ba(OH)2 dư thì thu được 9,062 gam kết tủa. Phần trăm khối lượng Fe2O3 trong hỗn hợp A bằng:
A. 86,96%
B. 76,01%
C. 73,04%
D. 66,01%
Đáp án A
Đặt số mol FeO là x mol; Số mol Fe2O3 là y mol
→ x+ y = 0,04 mol (1)
Bản chất phản ứng: CO + Ooxit → CO2
CO2+ Ba(OH)2 → BaCO3 ↓ + H2O
Theo PT: nO (oxit) = n C O 2 = n B a C O 3 = 9,062/197 = 0,046 mol
Khi cho CO qua hỗn hợp A thì khối lượng chất rắn giảm. Lượng giảm chính là lượng O trong oxit tách ra
→mhỗn hợp A = mB+ mO (oxit tách ra) = 4,784+ 0,046.16 = 5,52 gam
→72x+ 160y = 5,52 gam (2)
Giải hệ gồm (1), (2) ta có x = 0,01; y = 0,03
→ % m F e 2 O 3 = 0 , 03 . 160 5 , 52 . 100 % = 86 , 96 %
Đúng 0
Bình luận (0)
Cho một luồng khí CO đi qua 0,04 mol hỗn hợp A gồm FeO và Fe2O3 ở nhiệt độ cao. Sau thí nghiệm, được hỗn hợp B gồm 4 chất rắn, cân nặng 4,784 gam và chất khí C. Dẫn C vào dung dịch Ba(OH)2 dư được 9,062 gam kết tủa.Tính khối lượng các oxit trong A. A.
m
FeO
2
,
16
g
;...
Đọc tiếp
Cho một luồng khí CO đi qua 0,04 mol hỗn hợp A gồm FeO và Fe2O3 ở nhiệt độ cao. Sau thí nghiệm, được hỗn hợp B gồm 4 chất rắn, cân nặng 4,784 gam và chất khí C. Dẫn C vào dung dịch Ba(OH)2 dư được 9,062 gam kết tủa.Tính khối lượng các oxit trong A.
A. m FeO = 2 , 16 g ; m Fe 2 O 3 = 1 , 6 g
B. m FeO = 1 , 6 g ; m Fe 2 O 3 = 2 , 16 g
C. m FeO = 4 , 78 g ; m Fe 2 O 3 = 0 , 72 g
D. m FeO = 0 , 72 g ; m Fe 2 O 3 = 4 , 8 g
Cho khí CO đi qua ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, ta nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi ra khỏi ống dẫn qua dung dịch Ba(OH)2 dư thì thu được 9,062g kết tủa. Phần trăm khối lượng FeO trong hỗn hợp X là: A. 13,04% B. 25,15% C. 24,42% D. 32,55%
Đọc tiếp
Cho khí CO đi qua ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, ta nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi ra khỏi ống dẫn qua dung dịch Ba(OH)2 dư thì thu được 9,062g kết tủa. Phần trăm khối lượng FeO trong hỗn hợp X là:
A. 13,04%
B. 25,15%
C. 24,42%
D. 32,55%
Giải thích: Đáp án A
n BaCO3 = n CO2 = 9,062 : 197 = 0,046 mol
=> n O đã pư = 0,046 mol => m O = 0,736 g
Bảo toàn khối lượng m hhđầu = m O pư + m hh sau = 0,736 + 4,784 = 5,52 g
Ta có hệ 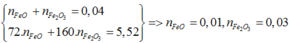
=> m FeO = 0,72 g
=> % m FeO = 13,04%
Chú ý : Bản chất của phản ứng dùng CO hay H2 khử oxit kim loại là việc CO hay H2 lấy O trong oxit ra tạo thành CO2 và H2O , số mol CO , H2 sẽ bằng số mol O ( nằm trong oxit ) đã bị lấy ra
Đúng 0
Bình luận (0)
Cho khí CO đi quA ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi rA khỏi ống dẫn quA dung dịch BA(OH)2 dư thì thu được 9,062g kết tủa. Phần trăm khối lượng FeO trong hỗn hợp X là A. 24,42%. B. 25,15%. C. 32,55%. D. 13,04%.
Đọc tiếp
Cho khí CO đi quA ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi rA khỏi ống dẫn quA dung dịch BA(OH)2 dư thì thu được 9,062g kết tủa. Phần trăm khối lượng FeO trong hỗn hợp X là
A. 24,42%.
B. 25,15%.
C. 32,55%.
D. 13,04%.
Đáp án D
nCO2 = nBACO3 = 9,062/197 = 0,046
BTKL => mX = mY + mCO2 – mCO = 4,784 + 0,046(44 – 28) = 5,52
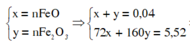
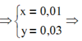
%mFeO = 0,01.72.100%/5,52 = 13,04%
Đúng 0
Bình luận (0)
Cho khí CO đi qua ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi ra khỏi ống dẫn qua dung dịch BA(OH)2 dư thì thu được 9,062g kết tủa. Phần trăm khối lượng FeO trong hỗn hợp X là A. 24,42%. B. 25,15%. C. 32,55%. D. 13,04%.
Đọc tiếp
Cho khí CO đi qua ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi ra khỏi ống dẫn qua dung dịch BA(OH)2 dư thì thu được 9,062g kết tủa. Phần trăm khối lượng FeO trong hỗn hợp X là
A. 24,42%.
B. 25,15%.
C. 32,55%.
D. 13,04%.
Đáp án D
nCO2 = nBACO3 = 9,062/197 = 0,046
BTKL => mX = mY + mCO2 – mCO = 4,784 + 0,046(44 – 28) = 5,52
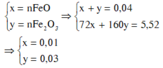
=> %mFeO = 0,01.72.100%/5,52 = 13,04%
Đúng 0
Bình luận (0)
Cho khí CO đi qua ống chứa 0,04 mol X gồm FeO và Fe2O3 đốt nóng, ta nhận được 4,784g chất rắn Y (gồm 4 chất), khí đi ra khỏi ống dẫn qua dung dịch Ba(OH)2 dư thì nhận được 9,062g kết tủa. Tính số mol FeO,Fe2O3 trong hỗn hợp X.(có ghi PTHH và 4 chất trong Y rõ ràng)
GIÚP VỚI Ạ<3
Cho mọt luồng khí CO đi qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 nung nóng. Sau một thời gian thu được chất rắn B gồm 4 chất nặng 4,784g. Khí thoát ra khỏi ống cho hấp thụ vào dung dịch Ba(OH)2 dư thu dược 9,062g kết tủa. Phần trăm khối lượng của FeO trong A là A. 31,03%. B. 13,04%. C. 86,96%. D. 68,97%.
Đọc tiếp
Cho mọt luồng khí CO đi qua ống sứ đựng 0,04 mol hỗn hợp A gồm FeO và Fe2O3 nung nóng. Sau một thời gian thu được chất rắn B gồm 4 chất nặng 4,784g. Khí thoát ra khỏi ống cho hấp thụ vào dung dịch Ba(OH)2 dư thu dược 9,062g kết tủa. Phần trăm khối lượng của FeO trong A là
A. 31,03%.
B. 13,04%.
C. 86,96%.
D. 68,97%.
Khử 4,64 gam hỗn hợp X gồm các oxit MgO, FeO, Fe3O4, và Fe2O3 bằng khí CO ở nhiệt độ cao, người ta thu được m gam hỗn hợp chất rắn Y và khí Z. Khí Z dẫn qua dung dịch Ba(OH)2 dư thu được 1,97 gam kết tủa. Giá trị của m là
A. 4,84
B. 4,40
C. 4,48
D. 4,68
Đáp án C
Bản chất phản ứng:
CO + Ooxit → CO2
CO2+ Ba(OH)2 → BaCO3↓ + H2O
Theo PTHH: nO (oxit)= nCO2= nBaCO3= 1,97/197 = 0,01 mol
→m= mchất rắn X - mO (oxit tách)= 4,64 -0,01.16= 4,48 gam
Đúng 0
Bình luận (0)