Nguyên tố X có tổng số electro trong phân lớp p là 9.Nguyên tố Y có tổng số hạt cơ bản là 82,số hạt mang điện nhiều hơn số hạt ko mang điện là 22.X và Yclaf các nguyên tố:
A.F và Fe
B.N và CO
C.P và Fe
D.P và Ni
nguyên tử của một nguyên tố X có tổng cơ bản (proton,notron,electron)là 82 biết số hạt mang điện nhiều hơn số hạt không mang điện là 22. Tổng số proton và số notrong của nguyên tố X là
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Số hiệu nguyên tử, số khối, tên nguyên tố X và kí hiệu hóa học tương ứng là:
A. 27, 60 và tên gọi là coban, kí hiệu hóa học Co.
B. 26, 56 và tên gọi là sắt, kí hiệu hóa học Fe.
C. 28, 59 và tên gọi là niken, kí hiệu hóa học Ni.
D. 29, 63 và tên gọi là đồng, kí hiệu hóa học Cu.
Đáp án B
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82 → 2p + n = 82
Số hạt mang điện nhiều hơn số hạt không mang điện là 22 → 2p - n =22
→ p= 26 và n = 30
→ Số hiệu nguyên tử của X là 26, số khối là 56. Tên nguyên tố sắt( Fe)
Câu 2: Nguyên tử của một nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Xác định số p,e,n, số khối và kí hiệu nguyên tố.
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82 → 2p + n = 82
Số hạt mang điện nhiều hơn số hạt không mang điện là 22 → 2p - n =22
→ p= 26 và n = 30
→ Số hiệu nguyên tử của X là 26, số khối là 56. Tên nguyên tố sắt( Fe)
Câu 2: Nguyên tử nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Xác định số hiệu nguyên tử, số khối và kí hiệu nguyên tử X.
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 82:
p + e + n = 82 hay 2p + n = 82 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 22 hạt
(p+e) – n = 22 hay 2p – n = 22 (2)
Giải (1), (2) ta có p = e = 26; n =30
Số khối của X = Z + N = p + n =56
Nguyên tử của 1 nguyên tố X có tổng số hạt cơ bản (proton, nơtron, electron) là 82 hạt. Trong đó hạt mang điện nhiều hơn hạt không mang điện là 22 hạt. Nguyên tố X là:
A. Fe
B. Cr
C. Al
D. Cu
Với dạng bài toán này thì ta có thể giải theo 2 cách:
Cách 1:
Áp dụng công thức:
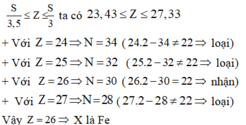
Cách 2: Gọi số p, n, e trong nguyên tử lần lượt là Z, N, E (nguyên dương)
+ Nguyên tử của nguyên tố X có tổng số hạt cơ bản (proton, nơtron, electron) là 82 hạt: 2Z + N = 82
+ Hạt mang điện nhiều hơn hạt không mang điện là 22 hạt: 2Z - N = 22
Từ đó ta có:
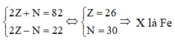
Đáp án A.
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8. X và Y là các nguyên tố:
A. Al và Br
B. Al và Cl
C. Mg và Cl
D. Si và Br.
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8. X và Y là các nguyên tố
A. Al và Cl
B. Mg và Cl
C. Si và Br
D. Al và Br
Đáp án A
Tổng số e trong phân lớp p là 7 => Al
=> tổng số hạt mang điện = 13 + 13 = 26
Trong Y:
Tổng số hạt mang điện = 26 + 8 = 34
=> Z =p = e = 17 => Y là Cl
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8. X và Y là các nguyên tố:
A. Al và Br
B. Al và Cl
C. Mg và Cl
D. Si và Br
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8. X và Y là các nguyên tố:
A. Al và Sc
B. Al và Cl
C. Mg và Cl
D. Si và Br
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. X có cấu hình 1s22s22p63s23p1 → X là Al (Z= 13)
Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8
→ nguyên tử của nguyên tố Y có số proton hơn số proton trong X là 4
pY=13+4=17 là Cl
Đáp án B.