Cho 19.1g hỗn hợp kim loại Al và Ba vào dung dịch H2SO4 dư. Sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp muối và 8.96l khí H2 thu được ở đktc
a. Tính % KL mỗi kim loại có trong hỗn hợp
b. Tính KL H2SO4 cần dùng
Cho m gam bột Fe vào 800ml dung dịch hỗn hơp gồm Cu(NO3)2 0,2M và H2SO4 0,25M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,6m gam hỗn hợp bột kim loại và V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của m và V lần lượt là:
A. 17,8 và 4,48
B. 17,8 và 2,24
C. 10,8 và 4,48
D. 10,8 và 2,24
Đáp án B
Ta có:
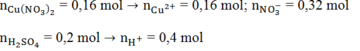
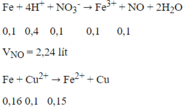
Do Fe nên tiếp tục xảy ra phản ứng:

nFe phản ứng = 0,1 + 0,05 + 0,16 = 0,31 mol
0,6m (g) hỗn hợp bột kim loại sau phản ứng gồm Fe dư và Cu sinh ra:
m - mFe pư + mCu = 0,6m → m - 0,31.56+ 64.0,16 = 0,6m
m = 17,8 (g)
hoà tan hoàn toàn 3,28g hỗn hợp kim loại trong hỗn hợp kim loại gồm cu, fe vào dung dịch h2so4 đặc nóng dư thu được 1,568l khí so2 và hai muối sunfat tính khối lượng dung dịch của h2so4 98% đã dùng
n SO2 = 1,568/22,4 = 0,07(mol)
Trong bài toán kim loại tác dụng với H2SO4, ta luôn có :
n H2SO4 pư = 2n SO2 = 0,07.2 = 0,14(mol)
=> m dd H2SO4 = 0,14.98/98% = 14(gam)
cho a gam Fe vào 500 ml dung dịch hỗn hợp gồm Hcl 1,8M và Cu(NO3)2 0,2M . Sau khi các phản ứng xảy ra hoàn toàn thu được 0,5 gam hỗn hợp kim loại và khí NO( sản phẩm khử duy nhất ). Giá trị của a là?
\(n_{Cu\left(NO_3\right)_2}=0,5.0,2=0,1\left(mol\right)\)
\(n_{NO_3^-}=0,1.2=0,2\left(mol\right)\)
\(n_{Cu^{2+}}=0,1\left(mol\right)\)
\(n_{HCl}=n_{H^+}=0,5.1,8=0,9\left(mol\right)\)
\(n_{NO}=\dfrac{n_{H^+}}{4}=\dfrac{0,9}{4}=0,225\left(mol\right)\)
Sau phản ứng thu được hỗn hợp kim loại \(\Rightarrow\) Cu và Fe \(\Rightarrow\) \(Fe^{2+}\)
Bảo toàn e:
\(2n_{Fe.pứ}=3n_{NO}+2n_{Cu^{2+}}\)
\(\Rightarrow n_{Fe.pứ}=0,4375\left(mol\right)\)
Có: \(a-m_{Fe.pứ}+m_{Cu}=m_{hh.kl}=0,5\)
\(\Leftrightarrow a-0,4375.56+64.0,1=0,5\\ \Rightarrow a=18,6\)
Cho 6,4g hỗn hợp A gồm Fe và Mg phản ứng với 100g dung dịch H2SO4 loãng vừa đủ được 3,584 lít (đkc) và dung dịch B a, tính % theo khối lượng mỗi chất có trong A b, tính C% của từng muối trong dung dịch B c, đốt cháy 6,4g hỗn hợp A ở trên với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không có khí dư). Hòa tan Y bằng 1 lượng vừa đủ 120ml dung dịch HCl 2M thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z thu được 56,69g kết tủa. Tính % theo thể tính của Cl2 trong hỗn hợp X
Hòa tan 16,6 gam hỗn hợp kim lọai Fe và Al cần dùng 300g dung dịch HCl, sau phản ứng thu được 11,2 lít khí H2 ở đktc
a. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
b. Tính nồng độ phần tram của dung dịch HCl đã dùng
a, Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
a--->2a------------------>a
2Al + 6HCl ---> 2AlCl3 + 3H2
b---->3b-------------------->1,5b
=> \(\left\{{}\begin{matrix}56a+27b=16,6\\a+1,5b=0,5\end{matrix}\right.\Leftrightarrow a=b=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
b) \(C\%_{HCl}=\dfrac{\left(0,2.2+0,2.3\right).36,5}{300}.100\%=12,167\%\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
gọi nFe : a , nAl: b (a,b>0) => 56a + 27b = 16,6 (g)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a a
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b \(\dfrac{3b}{2}\)
=> \(a+\dfrac{3b}{2}=0,5\)
ta có hệ pt
\(\left\{{}\begin{matrix}56a+27b=16,6\\a+\dfrac{3b}{2}=0,5\end{matrix}\right.\)
=> a= 0,2 , b = 0,2
\(\left\{{}\begin{matrix}m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=16,6-11,2=5,4\left(g\right)\end{matrix}\right.\)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2 0,4
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6
=> \(m_{HCl}=\left(0,4+0,6\right).36,5=36,5\left(g\right)\)
=> \(C\%=\dfrac{36,5}{200}.100\%=18,25\%\)
Hòa tan hoàn toàn 5,95g hỗn hợp muối cacbonat của kim loại hóa trị I và kim loại hóa trị II trong dd HCl thì sinh ra 1,12l khí (đktc). Đem cô cạn dung dịch sau phản ứng thì thu được bao nhiêu (g) muối khan.
Ta có:
\(n_{CO_2}=\frac{1.12}{22.4}=0.05\left(mol\right)\) \(\Rightarrow m_{CO_2}=0.05\times44=2.2\left(g\right)\)
\(X_2CO_3+2HCl\rightarrow2XCl+H_2O+CO_2\)
\(YCO_3+2HCl\rightarrow YCl_2+H_2O+CO_2\)
Ta thấy
\(n_{HCl}=2n_{CO_2}=2\times0.05=0.1\left(mol\right)\)
\(\Rightarrow\) \(m_{HCl}=0.1\times36.5=3.65\left(g\right)\)
\(n_{H_2O}=n_{CO_2}=0.05\left(mol\right)\)
\(\Rightarrow\) \(m_{H_2O}=0.05\times18=0.9\left(g\right)\)
Áp dụng định luật bảo toàn khối lượng ta được:
\(m_{XCl+YCl_2}=\left(5.95+3.65\right)-\left(2.2+0.9\right)=9.6-3.1=6.5\left(g\right)\)
Hỗn hợp gồm ba kim loại Al Fe Cu . Cho m g hỗn hợp X vào dung dịch CuSO4 dư sau khi phản ứng xảy ra hoàn toàn thu được 35.2g kim loại. Nếu cũng hòa tan m g hỗn hợp X vào 500ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8.96l khí H2(đktc) dung dịch Y và a gam rắn.Cho từ từ dung dịch NaOH 2M vào dung dịch Y khuấy đều đến khi thấy bắt đầu có kết tủa thì dùng hết V1 l dung dịch NaOH 2M, tiếp tục cho tiếp dung dịch NaOH vào đến khi lượng kết tủa không có sự thay đổi nữa thì lượng dung dịch NaOH đã dùng hết 600nl.
Tính các giá trị m và V1
Cho 18,5 gam hỗn hợp X gồm Fe và Fe3O4 tác dụng với 200ml dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí NO duy nhất (đktc), dung dịch Y và 1,46 gam kim loại. Nồng độ mol của dung dịch HNO3 là:
A. 2M
B. 2,4M
C. 2,5M
D. 3,2M
Cho hỗn hợp gồm 6,72 gam Mg và 0,8 gam MgO tác dụng hết với lượng dư dung dịch HNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,896 lít một khí X (đktc) và dung dịch Y. Làm bay hơi dung dịch Y thu được 46 gam muối khan. Khí X là
A. NO2
B. N2O
C. N2
D. NO.