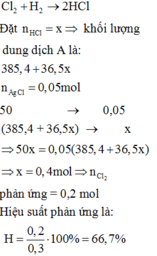cho 1l H2 tác dụng vs 0,672 l Cl2. Rồi hòa tan sp vafp 19,27g nước đk dd A . Lấy 5g dd A cho tác dụng AgNO3 dư thu đk 0,7175g kết tủa . Tính hiệu suất H2 và Cl2(CÁC KHÍ Ở ĐKTC)

Những câu hỏi liên quan
. cho 1 lít khí H2 và 0,672 lít khí Cl2(dktc) tác dụng với nhau rồi hòa tan sản phẩm vào 38,54g nước ta thu được dung dịch A. Lấy dung dịch A trên cho tác dụng với dung dịch AgNO3 (lấy dư) thu được 7,175g kết tủa. Tính hiệu suất của phản ứng giữa H2 và Cl2
\(n_{H_2}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: H2 + Cl2 --as--> 2HCl
Xét tỉ lệ: \(\dfrac{\dfrac{5}{112}}{1}>\dfrac{0,03}{1}\) => Hiệu suất tính theo Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
Bảo toàn Cl: \(n_{Cl_2\left(pư\right)}=0,025\left(mol\right)\)
\(H\%=\dfrac{0,025}{0,03}.100\%=83,33\%\)
Đúng 3
Bình luận (0)
Cho 2 lít (đktc) H2 tác dụng với 1,344 lít Cl2 (đktc) rồi hòa tan sản phẩm vào nước để được 40 gam dụng dịch A. Lấy 10 gam A tác dụng với dung dịch AgNO3 dư thu được 3,444 gam kết tủa. Tính hiệu suất phản ứng giữa H2 và Cl2 (giả sử Cl2 và H2 không tan trong nước)? A. 20% B. 80% C. 40% D. 50%
Đọc tiếp
Cho 2 lít (đktc) H2 tác dụng với 1,344 lít Cl2 (đktc) rồi hòa tan sản phẩm vào nước để được 40 gam dụng dịch A. Lấy 10 gam A tác dụng với dung dịch AgNO3 dư thu được 3,444 gam kết tủa. Tính hiệu suất phản ứng giữa H2 và Cl2 (giả sử Cl2 và H2 không tan trong nước)?
A. 20%
B. 80%
C. 40%
D. 50%
Cho 2 lít (đktc) H2 tác dụng với 1,344 lít Cl2 (đktc) rồi hòa tan sản phẩm vào nước để được 40 gam dụng dịch A. Lấy 10 gam A tác dụng với dung dịch AgNO3 dư thu được 3,444 gam kết tủa. Tính hiệu suất phản ứng giữa H2 và Cl2 (giả sử Cl2 và H2 không tan trong nước)?A. 20%. B. 80%. C. 40%. D. 50%.giải chi tiết hộ mk nhé
Đọc tiếp
Cho 2 lít (đktc) H2 tác dụng với 1,344 lít Cl2 (đktc) rồi hòa tan sản phẩm vào nước để được 40 gam dụng dịch A. Lấy 10 gam A tác dụng với dung dịch AgNO3 dư thu được 3,444 gam kết tủa. Tính hiệu suất phản ứng giữa H2 và Cl2 (giả sử Cl2 và H2 không tan trong nước)?
A. 20%. B. 80%. C. 40%. D. 50%.
giải chi tiết hộ mk nhé
Cho 10,00 lít H2 và 6,72 lít khí Clo (đktc) tác dụng với nhau rồi hòa tan sản phẩm vào 385,40 gam nước thu được dung dịch A. Lấy 50 gam dung dịch A cho tác dụng với AgNO3 dư thu được 7,175 gam kết tủa. Tính hiệu suất phản ứng giữa H2 và Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
PTHH: HCl + AgNO3 ---> AgCl↓ + HNO3
0,05<---------------0,05
\(\rightarrow m_{HCl}=0,05.36,5=1,825\left(g\right)\\
\rightarrow C\%_{ddA}=\dfrac{1,825}{50}.100\%=3,65\%\)
\(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Đặt H = x%
PTHH: Cl2 + H2 --as--> 2HCl
LTL: 6,72 < 10 => H2 dư
=> nHCl = 0,3x (mol)
\(\rightarrow C\%_{HCl}=\dfrac{0,3x.36,5}{0,3x.36,5+385,4}.100\%=3,65\%\\ \Leftrightarrow20,23\%\)
Đúng 2
Bình luận (0)
Cho 1 lít H2 (đktc) tác dụng với 0,672 lít Cl2 (đktc) rồi hòa tan sản phẩm vào 19,27g nước được dung dịch A . Lấy 5 gam A tác dụng với dung dịch AgNO3 dư thu được 0,7175 g kết tủa. Tính hiệu suất giữa H2 và Cl2 . Biết các thể tích khí đều đo ở đktc
PTHH :
\(H_2+Cl_2\rightarrow2HCl\left(1\right)\)
\(HCl+AgNO_3\rightarrow AgCl+HNO_3\) \(\left(2\right)\)
Ta có : \(n_{H_2}=\frac{V}{22,4}=\frac{1}{22,4}=0,446\left(mol\right)\)
\(n_{Cl_2}=\frac{V}{22,4}=\frac{0,672}{22,4}=0,3\left(mol\right)\)
Vì \(n_{H_2}>n_{Cl_2}\Leftrightarrow n_{H_2}\) dư, \(n_{Cl_2}\) hết
Theo pt (2) : \(n_{HCl}=n_{AgCl}=0,01\left(mol\right)\) (trong 5g)
\(\Leftrightarrow n_{HCl}=0,01.4=0,04\left(mol\right)\) (trong 20g)
Theo pt (1) : \(n_{Cl_2pư}=\frac{1}{2}n_{HCl}=0,02\left(mol\right)\)
\(H=\frac{0,02}{0,03}.100\%=66,67\%\)
Vậy....
nH2=\(\frac{12}{2,4}\)=0,0446mol
nCl2=0,03mol
H2 + Cl2 → 2HCl (1)
Vì nH2>nCl2nH2>nCl2\(\rightarrow\) Hiệu suất phản ứng tính theo Cl2
AgNO3 + HCl → AgCl + HNO3
\(\rightarrow\) nHCl (trong 5g A) = nAgCl = 0,01 mol
\(\rightarrow\) nHCl (trong 20g A) = 0,01.4 = 0,04 mol
(1) => nCl2 phản ứng = 0,5.nHCl = 0,5.0,04 = 0,02 mol
=> H% = \(\frac{0,02}{0,03}.100\%\)= 66,67%
cho 16,8l khí h2 tác dụng với 14,56l khí cl2 ở điều kiện thích hợp. sản phẩm sinh ra hòa tan trong nước được dd D. lấy 1/10 dd D cho tác dụng với agno3 dư thì thu được 17,22g kết tủa trắng. tiinhs hiệu xuất phản ứng tổng hợp ban đầu, biết các chất khí đó ở đktc
H2 + Cl2 ---> 2HCl (khí) (1)
nH2 = \(\frac{16,8}{22,4}\) = 0,75 (mol)
nCl2 = \(\frac{14,56}{22,4}\) = 0,65 (mol)
So sánh: \(\frac{nH2}{1}\) > \(\frac{nCL2}{1}\)
=> H2 dư sau phản ứng, chọn nCl2 để tính
Theo PTHH: nHCl = 2.nCl2 = 2. 0,65 = 1,3 (mol)
Khi hòa tan hỗn hợp khí gồm khí HCl và H2 dư vào H2O, thu được dd D là dd HCl
Khi cho dd HCl vào AgNO3 dư thì:
HCl + AgNO3 ----> AgCl + HNO3 (2)
Vì HNO3 dư nên tính theo nHCl
nHCl = \(\frac{1}{10}\).1,3 = 0,13 (mol)
Theo PTHH (2) nAgCl (lí thuyết) = nHCl = 0,13 (mol)
=> mAgCl (lí thuyết) = 0,13 . 143,5 = 18,655 (g)
Hiệu suất phản ứng:
H = \(\frac{17,22.100}{18,655}\) = 92,31 %
Đúng 1
Bình luận (0)
Cho 10,0 lít H2 và 6,72 lít Cl2 (đktc) tác dụng với nhau rồi hòa tan sản phẩm vào 358,4 gam nước ta thu được dung dịch A. Lấy 50,0 gam dung dịch A tác dụng với dung dịch AgNO3 dư thu được 7,175 gam kết tủa. Hiệu suất của phản ứng giữa H2 và Cl2 là: A. 32,4% B. 20,0% C. 44,8% D. 66,7%
Đọc tiếp
Cho 10,0 lít H2 và 6,72 lít Cl2 (đktc) tác dụng với nhau rồi hòa tan sản phẩm vào 358,4 gam nước ta thu được dung dịch A. Lấy 50,0 gam dung dịch A tác dụng với dung dịch AgNO3 dư thu được 7,175 gam kết tủa. Hiệu suất của phản ứng giữa H2 và Cl2 là:
A. 32,4%
B. 20,0%
C. 44,8%
D. 66,7%
cho 1 l khí h2 tác dugj với khí cl2 0,672l rồi hoà tan sản phẩm vào 19,27g nước được dd A . lấy 5 g ddA cho tác dụng với AgNO3 dư được 0,7175g kết tủa . tính hiệu xuất của cl2 và h2. bt các thể tichs khí đều đo ở điều kiện tiêu chuẩn
Cho 0,672 lít khí H2 tác dụng với 0.56 lít khí Cl2 (đktc) rồi hòa tan sản phẩm vào nước để được 10gam dung dịch A. Lấy 5g dung dịch A tác dụng với AgNO3 dư thu được 1,435 gam kết tủa. Tính hiệu suất phản ứng giữa Cl2 và H2, giả sử Cl2 và H2 không tan trong nước.
\(H_2+Cl_2\rightarrow2HCl\)
\(AgNO_3+HCl\rightarrow AgCl+HNO_3\)
\(n_{H2}=\frac{0,672}{22,4}=0,03\left(mol\right)\)
\(n_{CL2}=\frac{0,56}{22,4}=0,025\left(mol\right)\)
\(\rightarrow\) Tính theo Cl2
\(n_{AgCl}=\frac{1,435}{143,5}=0,01\left(mol\right)\)
\(\rightarrow n_{HCl_{bđ}}=0,02\left(mol\right)\)
\(\rightarrow n_{HCl_{lt}}=0,025.2=0,05\left(mol\right)\)
\(\rightarrow H=\frac{0,02}{0,05}.100=40\%\)