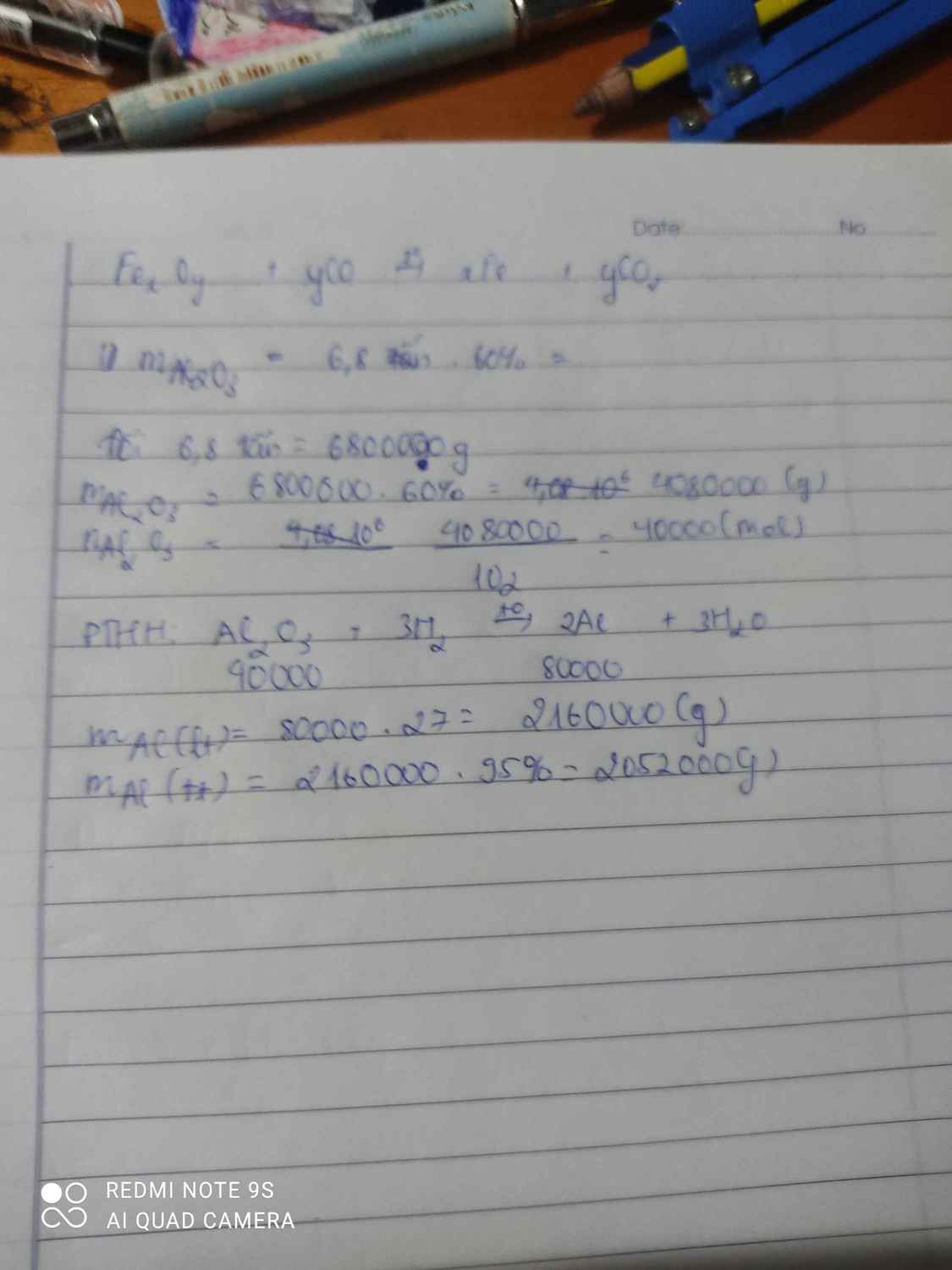Biết rằng quặng boxit có chứa 60% nhôm oxit. Điên phân nóng chảy hoàn toàn thu được m tấn quặng thu được 54 tấn kim loại. m = ?

Những câu hỏi liên quan
Biết rằng quặng boxit có chứa 60% nhôm oxit. Điên phân nóng chảy hoàn toàn thu được m tấn quặng thu được 54 tấn kim loại. m = ?
2Al2O3 \(\rightarrow\)4Al+3O2
2 mol.........4mol
x tấn............54 tấn
=> x=27 tấn
m=\(27\dfrac{100}{60}=45\left(tấn\right)\)
Mình cx ko chắc lắm để cô coi đúng ko rồi hãy chọn nha
Đúng 0
Bình luận (1)
Trong một loại quặng boxit có 50% nhôm oxit. Nhôm luyện từ oxit đó còn chứa 1,5% tạp chất. Tính lượng nhôm thu được khi luyện 0,5 tấn quặng boxit trên. Hiệu suất phản ứng 100%.
Lượng nhôm oxit có trong 0,5 tấn quặng là : 0,5x50/100 = 0,25 tấn = 250kg
Phương trình hoá học điều chế Al :
2 Al 2 O 3 → 4Al + 3 O 2
Khối lượng Al nguyên chất thu được từ 250 kg quặng :
x = 250x4x27/(2x102) = 132,4(kg)
Khối lượng Al lẫn tạp chất: 132,4 x 101,5% = 134,386 (kg).
Đúng 0
Bình luận (0)
1 loại quặng boxit có chứa 60% tạp chất AL2O3. AL luyện từ oxit đó có chứa % tạp chất. tính khối lượng AL thu được khi luyện 6,8 tấn quặng trên. Biết hiệu suất =95%
Giải hộ mình vớiiiiiii
chứa % tạp chất vậy đó là bao nhiêu phần trăm em ơi?
Đúng 1
Bình luận (0)
Bài 2. Nhôm oxit (Al2O3) là thành phần chính của quặng boxit, còn lại là tạp chất . điện phân nóng chảy 127,5 gam quặng boxit theo phản ứng :Al2O3 Al + O2.Thu được 54 gam Al (nhôm) và 48 gam O2 (khí oxi) a.Tính khối lượng Al2O3 (Nhôm oxit) đã phản ứng? b.Tính tỉ lệ phần trăm về khối lượng của Nhôm oxit có trong quặng boxit?
Đọc tiếp
Bài 2. Nhôm oxit (Al2O3) là thành phần chính của quặng boxit, còn lại là tạp chất . điện phân nóng chảy 127,5 gam quặng boxit theo phản ứng :
Al2O3 Al + O2.
Thu được 54 gam Al (nhôm) và 48 gam O2 (khí oxi)
a.Tính khối lượng Al2O3 (Nhôm oxit) đã phản ứng?
b.Tính tỉ lệ phần trăm về khối lượng của Nhôm oxit có trong quặng boxit?
a/ nAl= 54/27= 2(mol)
nO2=48/32=1,5(mol)
PTHH: 2 Al2O3 -to-> 4 Al +3 O2
Ta có: 2/4 = 1,5/3
=> P.ứ hết
=> nAl2O3= 1/2. nAl=1/2. 2=1(mol)
=> mAl2O3=1.102=102(g)
b) %mAl2O3= (102/127,5).100= 80%
Đúng 2
Bình luận (0)
Trong quặng boxit có chứa AI2O3.Khi phân hủy quặng boxit thì AI2O3 đã tham gia phản phân hủy thu được 1,35 tấn nhôm (AI) và 1,2 tấn khí O2. Tính khối lượng AI2O3 phản ứng
Bảo toàn khối lượng: \(m_{Al_2O_3}=m_{Al}+m_{O_2}=2,55\left(tấn\right)\)
Đúng 3
Bình luận (0)
1 một kim loại X chứa 64% Fe2O3, quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z có thể điều chế được 481,25 kg gang chứa 4% cacbon.( Gang là hợp chất của sắt và cacbon).2 Phân hủy hoàn toàn một hợp chất A ở nhiệt độ cao theo phương trình sau: 4A nhiệt phân------ 4B+ C + 2DCác sản phẩm tạo thành đều ở thể khí. Tính tỉ khối của hỗn hợp khí sau phản ứng so với khí hidro là 18. Xác định khối lượng mol của chất A C...
Đọc tiếp
1> một kim loại X chứa 64% Fe2O3, quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z có thể điều chế được 481,25 kg gang chứa 4% cacbon.( Gang là hợp chất của sắt và cacbon).
2> Phân hủy hoàn toàn một hợp chất A ở nhiệt độ cao theo phương trình sau:
4A nhiệt phân------> 4B+ C + 2D
Các sản phẩm tạo thành đều ở thể khí. Tính tỉ khối của hỗn hợp khí sau phản ứng so với khí hidro là 18. Xác định khối lượng mol của chất A
Các bạn giúp tui nha cám ơn mn nhiều:))
2)
Giả sử có 1 mol A
PTHH: 4A --to--> 4B + C + 2D
1------->1-->0,25->0,5
=> nkhí sau pư = 1 + 0,25 + 0,5 = 1,75 (mol)
BTKL: mA = mB + mC + mD
Có \(\overline{M}=\dfrac{m_B+m_C+m_D}{1,75}=18.2=36\)
=> mA = 63 (g)
=> \(M_A=\dfrac{63}{1}=63\left(g/mol\right)\)
Đúng 3
Bình luận (0)
câu 1) đề có nói rõ điều chế 481,25kg gang từ bao nhiêu Z không vậy bn :) ?
Đúng 1
Bình luận (3)
1)
Giả sử a + b = 1 (tấn)
Do cacbon chiếm 4%
=> Fe chiếm 96% khối lượng gang
\(m_{Fe}=\dfrac{481,25.10^3.96}{100}=462.10^3\left(g\right)\)
=> \(n_{Fe}=\dfrac{462.10^3}{56}=8,25.10^3\left(mol\right)\)
\(m_{Fe_2O_3\left(X\right)}=\dfrac{a.10^6.64}{100}=640.10^3.a\left(g\right)\)
=> \(n_{Fe_2O_3}=\dfrac{640.10^3.a}{160}=4.10^3.a\left(mol\right)\)
\(m_{Fe_3O_4\left(Y\right)}=\dfrac{b.10^6.69,6}{100}=696.10^3.b\left(g\right)\)
=> \(n_{Fe_3O_4}=\dfrac{696.10^3.b}{232}=3.10^3.b\left(mol\right)\)
Bảo toàn Fe:
2.4.103.a + 3.3.103.b = 8,25.103
=> 8a + 9b = 8,25
Mà a + b = 1
=> a = 0,75; b = 0,25
=> \(\dfrac{a}{b}=\dfrac{0,75}{0,25}=\dfrac{3}{1}\)
Đúng 1
Bình luận (0)
Trong 1 loại quặng boxit có 50 % nhôm oxit . Nhôm luyện từ oxit đó còn chứa 1,5 % tạp chất . Tính lượng nhôm thu được khi luyện 0,5 tấn quặng boxit . Hiệu suất phản ứng là 90%.
PTHH
2Al2O3 \(\rightarrow\) 4Al + 3O2
mAl2O3(ĐB) = 50% x 0,5 = 0,25(tấn)
H = mAl2O3(PƯ) : mAl2O3(ĐB) x 100% = 90%
=> mAl2O3(PƯ) : 0,25 =0,9
=> mAl2O3(PƯ) = 0,9 x 0,25 =0,225(tấn)
Theo PT : 204g Al2O3 : 108g Al
Theo ĐB : 0,225 tấn Al2O3 : x tấn Al
=> x = 0,225 x 108 : 204 = 81/680 (tấn)
mà nhôm luyện từ oxit đó có chứa 1,5% tạp chất
=> %mAl(tinh khiết) = 100% - 1,5% =98.5%
=> mAl(tinh khiết) = 98,5% x 81/680 =0,1173(tấn)
Đúng 0
Bình luận (3)
0,5 tấn=500000g
\(m_{Al_2O_3\left(khôngtinhkhiet\right)}=\frac{500000.50}{100}=250000\left(g\right)\)
\(m_{Al_2O_2\left(tinhkhiet\right)}=250000-\left(\frac{250000.1,5}{100}\right)=246250\left(g\right)\)
\(2Al_2O_3\underrightarrow{t^o}4Al+3O_2\)
\(n_{Al_2O_3}=\frac{246250}{102}=\frac{123125}{51}\left(mol\right)\)
\(n_{Al}=2.n_{Al_2O_3}=2.\left(\frac{123125}{51}\right)=\frac{246250}{51}\left(mol\right)\)
\(m_{Al\left(lt\right)}=\frac{246250}{51}.27=130367,6471\left(g\right)\)
\(m_{Al\left(thucte\right)}=\frac{130367,5471.90}{100}=117330,8824\left(g\right)=0,11733\left(tấn\right)\)
Đúng 0
Bình luận (1)
Điện phân nóng cháy m (kg) quặng boxit ( chứa 60% Al2O3) thu được 5,4 kg nhôm và 4,8 kg oxi. Tính a (biết phản ứng Al2O3 ->Al+O2)
Bảo toàn khối lượng :
$m_{Al_2O_3} = m_{Al} + m_{O_2} = 5,4 + 4,8 = 10,2(kg)$
$m_{quặng\ boxit} = \dfrac{m_{Al_2O_3}}{60\%} = \dfrac{10,2}{60\%} = 17(kg)$
Đúng 2
Bình luận (0)
Tính lượng nhôm nguyên chất điều chế dc từ 1 tấn quặng boxit . Biết rằng trong quặng boxit chứa 50% là nhôm oxit và kim loại luyện từ oxit đó còn chứa 2,5% tạp chất.
m Al2O3 = 0.5 tấn
2Al2O3 -to-> 4Al + 3O2
204_________108
0.5_________x
x =0.265
mAl thực = 0.265*(100-2.5)/100= 0.258375 tấn
Đúng 0
Bình luận (0)