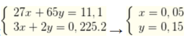1.Cho m g hỗn hợp fe và zn tác dụng vừa hết vs dung dịch hcl 2,5 M ( D=1,19g/ml ) thấy thoát ra 1 chất khí và thu đc 1200g đungịch xác định m
2. cho 2 mẩu fe có khối lượng bằng nhau . cho 1 mẩu hào tan hòa toàn trong dung dịch hcl tạo 19.05g muối . cho mẩu còn lại tan hòa toàn trong dung dịch h2so4 loãng thì khối lượng muối sắt tạo thành là bao nhiêu