Anh chị ơi! Chỉ hộ em cách làm bài toán này với ạ, em cảm ơn rất nhiều ạ: Chuẩn độ 10ml dung dịch CH3COOH Co= 0,1M (pKa= 4,75) bằng dung dịch NaOH 0,1M. Tính VNaOH tại thời điểm tương đương và tính pH tại điểm tương đương?
Giúp em với!!!
Giúp em với em xin cảm ơn ạ
Cho 500ml dung dịch CH3COOH 0,1M. Người ta thêm thêm từ từ dung dịch NaOH 0,1N vào 500ml dung dịch trên. Tính pH ở các thời điểm sau:
a. Thêm 100ml NaOH 0,1N c. Thêm 500ml NaOH 0,1N
b. Thêm 300ml NaOH 0,1N d. Thêm 600ml NaOH 0,1N
tính ph tại điểm tương đương khi chuẩn độ dung dịch ch3cooh. a. 1M và b. 0,1 M bằng dung dịch chuẩn naoh cùng nồng độ
dạ đây là toán 9 ạ mong anh chị thầy cô giúp đỡ em ạ .
BT1: Cho 3,2g Đồng oxit ta1xc dụng vừa đủ với dung dịch H2SO4 , 4,9% .Tính nồng độ phần trăm của dung dịch CuSO4
BT2 : Biết rằng 1,12l khí cacbon đioxit (điều kiện tiêu chuẩn) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hòa
a) Viết chương trình hóa học
b) Tính nồng độ mol của dung dịch NaOH đã dùng
dạ 2 bài tập quá nhiều nhưng em cần rất gấp mong anh chị thầy cô giúp đỡ em ạ . Em xin chân thành cảm ơn.
Bài 1 chị giải ở trên rồi nhé em
Bài 2
nCO2=1,12/22,4=0,05 mol
CO2 +2 NaOH => Na2CO3 + H2O
0,05 mol=>0,1 mol
CM dd NaOH=0,1/0,1=1M
thầy cô giúp em với ạ, đề cương của em còn 2 bài này mắc
HOÁ PHÂN TÍCH
1, Cho biết dung dịch H2A có Ka2= 10-4, Ka2= 10-8. tính pH và nồng độ của các dạng H2A, HA- và A2- trong dung dịch
a, NaHA
b, Na2A
( ??? dung dịch NaHA liệu có thể tạo được H2A không)
2,chuẩn độ 100ml một đa axit yếu H2A 0,1M ( pKa1=4, pKa2=8) bằng bazo NaOH, tính pH tại các thời điểm thể tích V(HCl) =0; 1; 5; 9; 9.9; 10; 10,1; 11; 15; 19,2 ; 22 ml
a.Tính pH của 100 ml dung dịch Xchứa HCl 0,1M và HNO30,1M.
b.Tính pH của 200 ml dung dịchY chứa NaOH 0,1M và KOH 0,2M .
c.Trộn 100 ml dung dịch X với 200 ml dung dịch Y(ở câu a và b)thu được dung dịch Z . Tính giá trị pH của dung dịch Z
GIúp em với ạ em xin chân thành cảm ơn
dung dịch Z có pH=13-> dung dịch Z chứa OH có nồng độ là 0,1M
ta có nH+=0,5anH+=0,5a mol ,nOHnOH = 0,5b mol
H++OH→H2OH++OH→H2O
dung dịch Z chứa OH →nOHdư=0,5b−0,5a→nOHdư=0,5b−0,5a mol
→[OH−]=0,5b−0,5aa+b=0,1M→0,4b−0,6a=0(1)→[OH−]=0,5b−0,5aa+b=0,1M→0,4b−0,6a=0(1)
theo đề bài -> a + b = 1 (2)
giải hệ chứa (1) và (2) -> a = 0,4 và b = 0,6
0,4 và 0,6 nha bnaj
Dung dịch A chứa HF 0,1M và NaF 0,1M. Tính pH của dung dịch biết pKa = 3,17
Chuẩn độ CH 3 COOH bằng dung dịch NaOH 0,1M. Kết quả thu được bảng sau đây:
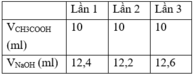
Vậy khối lượng CH 3 COOH có trong 1 lít dung dịch là:
A.7,44
B. 6,6
C. 5,4
D. 6,0
1) để trung hòa 10mL dung dịch HCL nồng độ x M cần 50mL dung dịch NaOH 0,5M. Xác định giá trị của x 2) để chuẩn độ 10mL dung dịch HCL cần 20mL dung dịch NaOH 0,1M. Xác định nồng độ của dung dịch HCL trên
1) Để trung hòa HCl, số mol HCl phải bằng số mol NaOH. Vì vậy, ta có:
n(HCl) = n(NaOH)
x * 10 = 0,5 * 50
x = (0,5 * 50) / 10
x = 2,5 triệu
Vậy, nồng độ của dung dịch HCl là 2.5 M.
2) Ta có:
n(HCl) = n(NaOH)
n(HCl) = 0,1 * 20/10
Vậy, nồng độ của dung dịch HCl là 0.2 M.
\(1)n_{NaOH}=0,05.0,5=0,025mol\\ NaOH+HCl\rightarrow NaCl+H_2O\\ \Rightarrow n_{NaOH}=n_{HCl}=0,025mol\)
\(C_M\) \(_{HCl}=\dfrac{0,025}{0,01}=2,5M\)
\(2)n_{NaOH}=0,1.0,02=0,002mol\\ HCl+NaOH\rightarrow NaCl+H_2O\\ n_{NaOH}=n_{HCl}=0,002mol\)
\(C_M\) \(_{HCl}=\dfrac{0,002}{0,01}=0,2M\)
Dung dịch có chứa CH3COOH 0,1M và CH3COONa 0,1M. Tính độ pH của dung dịch. Biết rằng hằng số axit của CH3COOH là Ka = 10-4,76.
Sửa đề bài Vì CH3COONa là chất điện li mạnh nên được viết trước để tạo môi trường cho cân bằng của chất điện li yếu phân li và cân bằng:
CH³COOH ⇔ CH³COO -+H+
Ban đầu 0,1 0. 0
Phân li xM x. x
Cân bằng 0,1-x 0,1+x x
Suy ra K = \(\dfrac{x(x+0,1)}{0,1-x}\) = 1,8.10 mũ âm ⁵
⇒ x = 1,8 . 10 mũ âm ⁵
⇒pH = log x = 1745