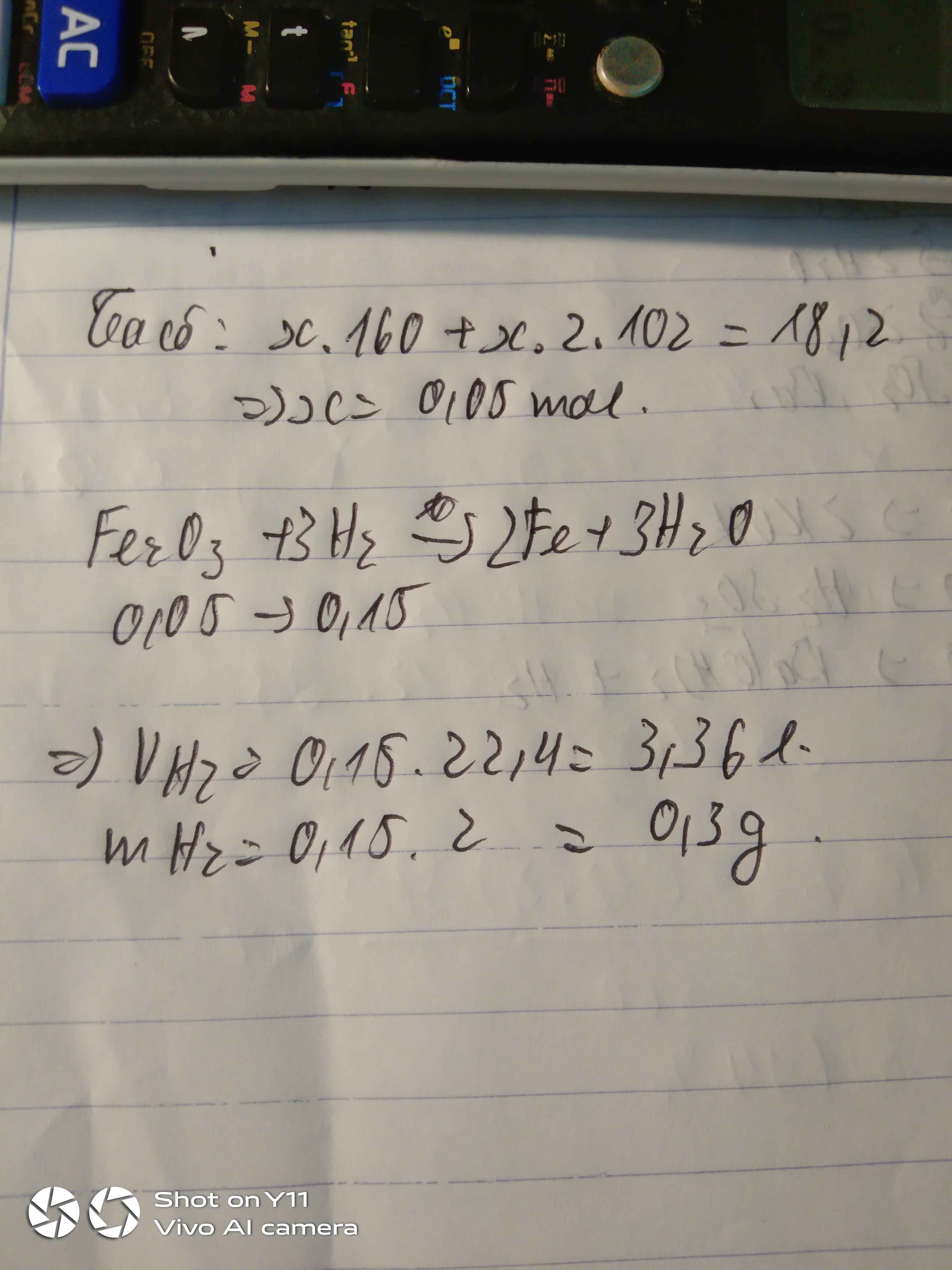Tính thể tích H2 tối thiểu cần dùng để phản ứng hết 30 , 3 g hỗn hợp M gồm al2o3 , zno , cuo ( tỉ lệ mol tương ứng là 2 : 2 : 3 )

Những câu hỏi liên quan
Một hỗn hợp A gồm fe2o3 và al2o3 có tỉ lệ mol tương ứng 1:2 tính thể tích h2 cần dùng để khử 18.2 g hỗn hợp A trên
Tính thể tích khí \(H_2\) (đktc) tốt thiểu cần dùng để phản ứng hết với 30,3 gam hỗn hợp M gồm \(Al_2O_3,Zno\) và \(CuO \) (tỉ lệ mol tương ứng là 2 : 2 : 3)
gọi x là số mol \(Al_2O_3\)=> \(n_{ZnO}\)=x và\(n_{CuO}=1,5x\) mol.
=> 102x + 81x + 80.1,5x = 30,3=> x=0,1 mol
\(Al_2O_3+H_2\underrightarrow{to}\) không sảy ra
\(ZnO+H_2\underrightarrow{to}Zn+H_2O\)
0,1->0,1
\(CuO+H_2\underrightarrow{to}Cu+H_2O\)
0,15->0,15
=>\(n_{H2}\) phản ứng =0,1+0,15=0,25 mol
=)\(V_{H2}=0,25.22,4=5,6\) (lít)
#hoctot
Đúng 0
Bình luận (0)
Gọi a là số mol của Al2O3
nAl2O3 = nZnO = 1,5a (mol)
=> 102a+81a+81.1,5a=30,3
giải phương trình trên a=0,1
PTHH: Al2O3 + H2 ---> ko xảy ra pứ
ZnO + H2 --> Zn + H2O
0,1......0,1.....0,1.....0,1
CuO + H2 --> Cu + H2O
0,15....0,15....0,15...0,15
nH2 pứ= 0,1+ 0,15 = 0,25 mol
=> VH2 = 0,25.22,4=5,6 lít
Đúng 0
Bình luận (0)
tính thể tích khí h2 tối thiểu cần dùng để phản ứng hết với 30,3 gam hỗn hợp M gồm oxit và kẽm oxit và đồng 2 oxit .tỉ lệ mol tương ứng là 2:@Nguyễn Thơ nn :3
Khử hoàn toàn m g hỗn hợp gồm CuO, Al2O3, Fe2O3 cần dùng 13,44l khí H2 ở đktc. Tính m biết tỷ lệ số mol của Fe2O3, Al2O3, CuO lần lượt là 1:2:3
Gọi \(\left\{{}\begin{matrix}n_{Fe_2O_3}=a\left(mol\right)\\n_{Al_2O_3}=2a\left(mol\right)\\n_{CuO}=3a\left(mol\right)\end{matrix}\right.\)
PTHH:
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
a ---------> 3a
CuO + H2 --to--> Cu + H2O
3a ------> 3a
\(\rightarrow3a+3a=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ \Leftrightarrow a=0,1\left(mol\right)\\ \rightarrow m=0,1.160+0,1.2.102+0,1.3.80=60,4\left(g\right)\)
Đúng 3
Bình luận (1)
Gọi \(n_{Fe_2O_3}=x\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al_2O_3}=2x\left(mol\right)\\n_{CuO}=3x\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
3x 3x
\(Al_2O_3+3H_2\rightarrow2Al+3H_2O\)
2x 6x
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
x 3x
\(\Rightarrow\Sigma n_{H_2}=3x+6x+3x=0,6\Rightarrow x=0,05mol\)
\(\Rightarrow m=m_{CuO}+m_{Al_2O_3}+m_{Fe_2O_3}\)
\(\Rightarrow m=3\cdot0,05\cdot80+2\cdot0,05\cdot102+0,05\cdot160=30,2g\)
Đúng 1
Bình luận (1)
Hỗn hợp A gồm CuO, Fe2O3 và Al2O3. Để khử hết 200g hỗn hợp A cần dùng hết V(l) khí H2 ở đktc, sau khi phản ứng xảy ra hoàn toàn thu được chất rắn B có khối lượng là 156g (biết tỷ lệ số mol giữa CuO và Fe2O3 trong hỗn hợp A là 1:15)a. Tính V(l) ở đktcb. Tính % khối lượng mỗi chất trong hỗn hợp Ac. Nếu 1/5 lượng khí H2 dùng ở trên phản ứng với 36g FeO thu được 29,6g chất rắn. Tính H phản ứng
Đọc tiếp
Hỗn hợp A gồm CuO, Fe2O3 và Al2O3. Để khử hết 200g hỗn hợp A cần dùng hết V(l) khí H2 ở đktc, sau khi phản ứng xảy ra hoàn toàn thu được chất rắn B có khối lượng là 156g (biết tỷ lệ số mol giữa CuO và Fe2O3 trong hỗn hợp A là 1:15)
a. Tính V(l) ở đktc
b. Tính % khối lượng mỗi chất trong hỗn hợp A
c. Nếu 1/5 lượng khí H2 dùng ở trên phản ứng với 36g FeO thu được 29,6g chất rắn. Tính H phản ứng
a) Gọi số mol H2 là x
=> nH2O=x(mol)
Theo ĐLBTKL: mA+mH2=mB+mH2O
=> 200 + 2x = 156 + 18x
=> x = 2,75 (mol)
=> VH2=2,75.22,4=61,6(l)
b) Gọi nCuO=a(mol)
nFe2O3=1,5a(mol)
=> 80a + 240a + 102b = 200
=> 320a + 102b = 200
PTHH: CuO + H2 --to--> Cu + H2O
a---------------->a
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
1,5a------------------>3a
=> 64a + 168a + 102b = 156
=> 232a + 102b = 156
=> a = 0,5; b = \(\dfrac{20}{15}\)
%mCuO=\(\dfrac{0,5.80}{200}\).100%=20%
%mFe2O3=\(\dfrac{0,75.160}{200}\).100%=60%
%mAl2O3=\(\dfrac{\dfrac{20}{15}102}{200}\).100%=20%
c) nH2=\(\dfrac{2,75}{5}\)=0,55(mol)
nFeO(tt)=\(\dfrac{36}{72}\)=0,5(mol)
Gọi số mol FeO phản ứng là t (mol)
PTHH: FeO + H2 --to--> Fe + H2O
t--------------->t
=> 56t + (0,5-t).72 = 29,6
=> t = 0,4 (mol)
=> H%=\(\dfrac{0,4}{0,5}\).100%=80%
Đúng 2
Bình luận (0)
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, th...
Đọc tiếp
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
Câu 4: Hỗn hợp A gồm bột CuO và Fe2O3 có tỉ lệ khối lượng tương ứng là 1: 2.
a. Tính khối lượng từng chất có trong 24 g hỗn hợp A.
b. Khử hoàn toàn hỗn hợp A bằng khí H2. Tính thể tích khí H2 cần dùng ở đktc.
c. Lấy toàn bộ chất rắn thu được cho tác dụng với dung dịch có chứa 7,3 g axit HCl. Tính khối lượng chất rắn còn
lại sau phản ứng.
\(\left\{{}\begin{matrix}CuO:a\\Fe2O3:2a\end{matrix}\right.\)
a.\(80a+320a=24\Leftrightarrow a=0.06\)
\(\Rightarrow\left\{{}\begin{matrix}CuO=0.06\\Fe2O3=0.12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}CuO=4.8g\\Fe2O3=19.2g\end{matrix}\right.\)
b.\(CuO+H2\rightarrow Cu+H2O\)
a a a
\(Fe2O3+3H2\rightarrow2Fe+3H2O\)
2a 6a 4a
\(\Rightarrow V_{H2}=\left(a+6a\right)\times22.4=9.408l\)
c.nHCl = 0.2 mol
\(Fe+2HCl\rightarrow FeCl2+H2\)
0.1 0.2
m chất rắn còn lại = mCu + m Fe ban đầu - m Fe bị hòa tan
= \(a\times64+4a\times56-0.1\times56=11.68g\)
Đúng 1
Bình luận (1)
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
Đọc tiếp
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
Đọc tiếp
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.