Hòa tan 3,38g oleum X vào nước người ta phải dùng 800ml dung dịch KOH 0,75M trung hòa dd X. Tìm công thức phân tử oleum X

Những câu hỏi liên quan
Hoà tan 3,38 gam oleum vào nước được dung dịch X. Để trung hoà dung dịch X cần 800ml dung dịch KOH 0,1 M. Công thức phân tử oleum đã dùng là A. H2SO4 .4SO3 B. H2SO4 .2SO3 C. H2SO4 .nSO3 D. H2SO4 .3SO3.
Đọc tiếp
Hoà tan 3,38 gam oleum vào nước được dung dịch X. Để trung hoà dung dịch X cần 800ml dung dịch KOH 0,1 M. Công thức phân tử oleum đã dùng là
A. H2SO4 .4SO3
B. H2SO4 .2SO3
C. H2SO4 .nSO3
D. H2SO4 .3SO3.
Đáp án D
Gọi công thức oleum là H2SO4.nSO3
=> Sau hòa tan vào H2O:
nH+ = 2nH2SO4 sau = 2(nH2SO4 + nSO3)
= 2(n+1)nOleum
=> nKOH = nH+ = 2(n+1) .3,38/(98+80n)
=0,08 mol
=> n = 3
Đúng 0
Bình luận (0)
hòa tan 3,38 gam oleum X vào nước người ta phải dùng 800ml dung dịch KOH 0,1 M để trung hòa dung dịch X . công thức phân tử oleum X là
Hòa tan 6,76 gam oleum vào nước dung dịch Y, để trung hòa dung dịch Y cần 160 ml dung dịch NaOH 1M. Công thức phân tử tử oleum là A.
H
2
SO
4
.
nSO
3
B.
H
2
SO
4
.
5
SO
3
C.
H
2
SO...
Đọc tiếp
Hòa tan 6,76 gam oleum vào nước dung dịch Y, để trung hòa dung dịch Y cần 160 ml dung dịch NaOH 1M. Công thức phân tử tử oleum là
A. H 2 SO 4 . nSO 3
B. H 2 SO 4 . 5 SO 3
C. H 2 SO 4 . 3 SO 3
D. H 2 SO 4 . 4 SO 3
Đáp án C
Số mol NaOH là: n NaOH = 0 , 16 . 1 = 0 , 16 mol
Đặt công thức của oleum là H 2 SO 4 . nSO 3
Oleum tác dụng với H 2 O :
H 2 SO 4 . nSO 3 + nH 2 O → ( n + 1 ) H 2 SO 4 ( 1 )
Dung dịch Y là dung dịch H 2 SO 4 . Trung hòa dung dịch Y bằng dung dịch NaOH:
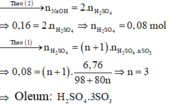
Đúng 0
Bình luận (0)
Hòa tan 3,38 gam oleum A vào lượng nước dư ta được dung dịch A. Để trung hòa 1/20 lượng dung dịch A cần dùng 40 ml dung dịch NaOH 0,1M. Tìm công thức của oleum
CTPT oleum: H2SO4.nSO3 có x (mol)
H2SO4.nSO3 + nH2O → (n + 1)H2SO4
x → x(n + 1)
H2SO4 + 2NaOH → Na2SO4 + 2H2O
x(n + 1)→ 2x(n + 1)
=> (98 + 80n)x = 3,38 và 2x (n + 1) = 0,08
=> x = 0,01 và nx = 0,03
=> n = 3
Suy ra CTPT oleum: H2SO4.3SO3
Đúng 0
Bình luận (0)
Hãy xác định công thức của oleum A, biết rằng khi hàm tan 3,38 gam A vào nước người ta phải dung 800 ml dung dịch KOH 0,1M để trung hòa dung dịch A. A. H2SO4.5SO3 B. H2SO4.6SO3 C. H2SO4.3SO3 D. H2SO4.4SO3
Đọc tiếp
Hãy xác định công thức của oleum A, biết rằng khi hàm tan 3,38 gam A vào nước người ta phải dung 800 ml dung dịch KOH 0,1M để trung hòa dung dịch A.
A. H2SO4.5SO3
B. H2SO4.6SO3
C. H2SO4.3SO3
D. H2SO4.4SO3
Đáp án C
Đặt công thức của oleum là H2SO4.nSO3
Khi hòa tan oleum vào nước:
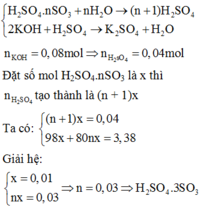
Đúng 0
Bình luận (0)
Hãy xác định công thức của oleum A, biết rằng khi hàm tan 3,38 gam A vào nước người ta phải dung 800 ml dung dịch KOH 0,1M để trung hòa dung dịch A A. H2SO4.5SO3 B. H2SO4.6SO3 C. H2SO4.3SO3 D. H2SO4.4SO3
Đọc tiếp
Hãy xác định công thức của oleum A, biết rằng khi hàm tan 3,38 gam A vào nước người ta phải dung 800 ml dung dịch KOH 0,1M để trung hòa dung dịch A
A. H2SO4.5SO3
B. H2SO4.6SO3
C. H2SO4.3SO3
D. H2SO4.4SO3
Đặt công thức của oleum là H2SO4.nSO3
Khi hòa tan oleum vào nước:

Đáp án C
Đúng 0
Bình luận (0)
hòa tan 8,6 gam oleum X vào nước được dung dịch Y . Để trung hòa dung dịch Y cần 200 ml dung dịch NaOH 1M . Công thức của oleum X là gì ?
Gọi CT oleum là H2SO4.nSO3 a mol
Hòa tan vào H2O tổng nH2SO4=a+an mol
nNaOH cần=0,2 mol
SO3 + H2O =>H2SO4
an mol =>an mol
H2SO4 +2 NaOH =>Na2SO4 + 2H2O
0,1 mol<=0,2 mol
=>a+an=0,1
Mà m oleum=8,6=a(98+80n)
Giải hpt có a=1/30 và an=1/15
=>n=2
CT oleum H2SO4.2SO3
Đúng 0
Bình luận (0)
Trung hoà dung dịch thu được sau khi hoà tan 3,38g oleum A vào nước phải dùng hết 800ml dd NaOH 0,1M.a)Xđ công thức của một mẫu oleum A. b)Tính khối lượng A cần hoà tan 200g nước để được dd H2SO4 15%
Gọi CT của oleum có dạng: H2SO4.nSO3
H2SO4.nSO3+H2O → (n+1)H2SO4
H2SO4+2NaOH → Na2SO4+2H2O
Ta có:
nNaOH = 0,08mol
=> nH2SO4 = 0,04mol
=> nH2SO4.nSO3 = 1/n+1nH2SO4 = 0,04/n+1mol
=> MH2SO4.nSO3 = 84,5(n+1) = 98+80n
=> n = 3
=> H2SO4.3SO3
Gọi a là số mol của H2SO4.3SO3
H2SO4.3SO3+H2O → 4H2SO4
mdd = mH2SO4.3SO3 + mH2O
C%H2SO4 = 4a.98/338a+200.100 = 15
=> a = 0,088mol
=> mH2SO4.3SO3 = 29,744g
Đúng 0
Bình luận (0)
Hòa tan hết 1,69 gam oleum có công thức H 2 S O 4 . 3 S O 3 vào nước dư. Trung hòa dung dịch thu được cần V ml dung dịch KOH 1M. Giá trị của V là
A. 20
B. 40
C. 30
D. 10











