Cho 2,4 gam kim loại X hóa trị II vào 200 ml dung dịch HCl 0,75M thấy sau phản ứng vẫn còn một phần kim loại chưa tan hết. Cũng 2,4 gam X tác dụng với 250ml dung dịch HCl 1M thấy sau phản ứng vẫn còn axit dư. Kim loại X là?

Những câu hỏi liên quan
Cho 11,7 gam một kim loại X hóa trị II vào 350 ml dung dịch HCl 1M, khi phản ứng kết thúc ta thấy kim loại vẫn còn dư. Mặt khác để hòa tan hoàn toàn lượng kim loại trên phải cần chưa đến 200 ml dung dịch HCl 2M. Tìm X.
nHCl = 0,35 . 1 = 0,35 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,175 0,35 0,175 0,175 (mol)
nHCl (pứ 2 ) = 0,2 . 2 = 0,4 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,2 0,4
\(nX=0,175+0,2=0,375\left(mol\right)\)
=> \(MX=\dfrac{11,7}{0,375}=\) 31,2 .-. k ra là s
Đúng 3
Bình luận (0)
Hoà tan hoàn toàn 2,4g kim loại A hóa trị II vào trong 100ml dung dịch HCl 1,5M. Sau phản ứng vẫn thấy còn một phần A chưa tan hết. Cũng 2,4g A trên nếu tác dụng với 125ml dung dịch HCl 2M thì thấy còn dư axit sau phản ứng. Xác đinh kim loại R.
Số mol HCl trong 100ml dd HCl1.5M= 0.15mol
Hòa tan 3.4g R trong 100ml dd HCl
PTHH: R+2HCl=RCl2+H2
3.4/R(mol) ----0.15 mol
Do R tan không tan hết nên 3.4/R> 0.075 suy ra R<45
Số mol HCl trong 125ml dd HCl 2M =0.25mol
PTHH:R+2HCl=RCl2+H2
3.4/R mol----0.25mol
Do R tan hết nên 3.4/R<0.125 nên R>27.2
Vì 27.2<R<45 nên R là Ca.
Đúng 0
Bình luận (1)
A là 1 kim loại hóa trị 2. Nếu cho 2,4 gam kim loại A tác dụng với 100ml dd HCl 1,5M. Thấy sau PƯ vẫn còn 1 phần kim loại A chưa tan hết. Cũng 2,4 kim loại A nếu tác dụng với 125 ml dd HCl, thấy sau PƯ vẫn còn dư axit. Xác định kim loại A(Mg)
Đề cho thiếu chỗ nồng độ HCl (125ml)
A+2HCl==>ACl2+H2(1)
\(n_{HCl}=\frac{100}{1000}.1,5=0,15mol\)
\(n_A=\frac{2,4}{A}\)
Vì kim loại không tan hết nên: \(\frac{\frac{2,4}{A}}{1}>\frac{0,15}{2}\)
\(\frac{2,4}{A}>0,075\Rightarrow A< 32\)
A+2HCl==>ACl2+H2(2)
\(n_{HCl}=\frac{125}{1000}.2=0,25mol\)
\(n_A=\frac{2,4}{A}\)
Vì axit dư nên: \(\frac{2,4}{A}< \frac{0,25}{2}\)
=> \(\frac{2,4}{A}< 0,125\Rightarrow A>19,2\)
Vậy A là Mg ( II)
Đúng 0
Bình luận (1)
A là 1 kim loại hóa trị 2. Nếu cho 2,4 gam kim loại A tác dụng với 100ml dd HCl 1,5M. Thấy sau PƯ vẫn còn 1 phần kim loại A chưa tan hết. Cũng 2,4 kim loại A nếu tác dụng với 125 ml dd HCl, thấy sau PƯ vẫn còn dư axit. Xác định kim loại A(Mg)
Cách biện luậnA là 1 kim loại hóa trị 2. Nếu cho 2,4 gam kim loại A tác dụng với 100ml dd HCl 1,5M. Thấy sau PƯ vẫn còn 1 phần kim loại A chưa tan hết. Cũng 2,4 kim loại A nếu tác dụng với 125 ml dd HCl, thấy sau PƯ vẫn còn dư axit. Xác định kim loại A(Mg)
Cách biện luậnVẫn không cho nồng độ của HCl (125ml) à
Đúng 0
Bình luận (1)
Hòa tan hết 6,5475 gam kim loại T trong một lượng vừa đủ dung dịch NaOH 1M. Cho từ từ dung dịch HCl vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch HCl 1M. Xác định kim loại T. A.Al B.Cr C.Zn D.Be
Đọc tiếp
Hòa tan hết 6,5475 gam kim loại T trong một lượng vừa đủ dung dịch NaOH 1M. Cho từ từ dung dịch HCl vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch HCl 1M. Xác định kim loại T.
A.Al
B.Cr
C.Zn
D.Be
Có thứ tự các phản ứng xảy ra như sau:
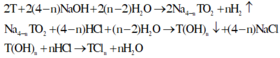
Do đó
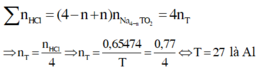
Đáp án A.
Đúng 0
Bình luận (0)
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau: Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím. Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím. Công thức oxit kim loại đã dùng là: A.Li2O. B. Na2O. C.K2O. D.Rb2O.
Đọc tiếp
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau:
Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím.
Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím.
Công thức oxit kim loại đã dùng là:
A.Li2O.
B. Na2O.
C.K2O.
D.Rb2O.
Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
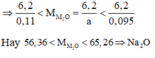
Đáp án B
Đúng 0
Bình luận (0)
Cho 2,4 gam kim loại hóa trị II tác dụng với dung dịch HCl lấy dư , sau khi phản ứng kết thúc thu được 2,24 lít H2 (đktc) . Xác định kim loại ?
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_R\)
\(\Rightarrow M_R=\dfrac{2,4}{0,1}=24\) (Magie)
Đúng 5
Bình luận (1)
Cho 16,25 gam Zn vào 200 ml dung dịch FeSO4 1M, sau phản ứng thu được m gam hỗn hợp kim loại X. Hòa tan m gam X bằng dung dịch HCl dư thấy thoát ra V lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn, giá trị của V là A. 4,48 B. 5,60 C. 10,08 D. 1,12
Đọc tiếp
Cho 16,25 gam Zn vào 200 ml dung dịch FeSO4 1M, sau phản ứng thu được m gam hỗn hợp kim loại X. Hòa tan m gam X bằng dung dịch HCl dư thấy thoát ra V lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn, giá trị của V là
A. 4,48
B. 5,60
C. 10,08
D. 1,12














