sau khi kết thúc thí nghiệm lấy 1ml dung dịch đem cô cạn trên mặt kính đồng hồ sẽ thấy chất rắn trắng tạo thành, đó là natri hidroxit(NaOH)
Dung dịch X chứa các ion: Ca2+, Na+, HCO3– và Cl–, trong đó số mol của ion Cl– là 0,1.
Thí nghiệm 1: cho 1/2 dung dịch X phản ứng với dung dịch NaOH dư, thu được 2 gam kết tủa.
Thí nghiệm 2: Cho 1/2 dung dịch X còn lại phản ứng với dung dịch Ca(OH)2 dư, thu được 5 gam kết tủa.
Mặt khác, nếu đem đun nóng để cô cạn dung dịch X thì thu được m1 gam chất rắn khan Y, lấy m1 gam chất rắn khan Y trên nung ở nhiệt độ cao đến khối lượng không đổi thu được m2 gam chất rắn khan Z. Giá trị của m1 và m2 lần lượt là:
A. 10,26 và 8,17
B. 14,01 và 9,15
C. 10,91 và 8,71
D. 10,91 và 9,15
BT2 : Để 1 mẩu Natri hidroxit trên tấm kính trong kk, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn trắng thấy có khí thoát ra, khí này làm đục nước vôi trong. Chất rắn màu trắng là sản phẩm phản ứng của Natri hidroxit với chất nào sau đây? Giải thích và viết phương trình hóa học minh họa.
a) Oxi trong kk
b) Hơi nước trong kk
c) Cacbon đioxit và oxi trong kk
d) Cacbon đioxit và hơi nước trong kk
e) Cacbon đioxit trong kk
mn giúp mình nha C:
Đáp án e
PTHH: \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
cho hai thí nghiệm như sau: TN1: cho a gam sắt vào V lít (đktc) dung dịch HCl, sau khi phản ứng kết thúc đem cô cạn dung dịch thu được 6,91gam chất rắn X.
TN2: Cho hỗn hợp a gam sắt và b gam Mg vào V lít ( đktc) dung dịch HCl, sau phản ứng thu được 1,12 lít khí H2( ddktc) và cô cạn dung dịch được 7,63 gam chất rắn Y.
a.Tính a,b
b.Tính khối lượng mỗi chất con trong X,Y
( Giả sử Mg không phản ứng với nước, và trong phản ứng với axit, Mg phản ứng trước, hết Mg mới đến Fe, các phản ứng xảy ra hoàn toàn)
Xét TN1:
PTHH: Fe + 2HCl FeCl2 + H2 (1)
Giả sử: Fe phản ứng hết Chất rắn là FeCl2
*Xét TN2:
PTHH: Mg + 2HCl MgCl2 + H2 (2)
Fe + 2HCl FeCl2 + H2 (3)
Ta thấy: Ngoài a gam Fe như thí nghiệm 1 cộng với b gam Mg mà chỉ giải phóng: < 0,024 (mol)
Chứng tỏ: Trong TN1: Fe dư, HCl hết
Ta có: nHCl (TN 1) = nHCl(TN 2) = 2nH = 2 . 0,02 = 0,04(mol)
TN1:
nFe(pư) = nFeCl= nHCl = . 0,04 = 0,02(mol)
=> mFe(dư) = 3,1 – 0,02.127 = 0,56 (gam)
mFe(pư) = 0,02 . 56 = 1,12(gam)
=> mFe = a = 0,56 + 1,12 = 1,68(gam)
*TN2:
Áp dụng ĐLBTKL:
a + b = 3,34 + 0,02.2 - 0,04.36,5 = 1,92 (g)
Mà a = 1,68g b = 1,92 - 1,68 = 0,24 (g)
cho hai thí nghiệm như sau: TN1: cho a gam sắt vào V lít (đktc) dung dịch HCl, sau khi phản ứng kết thúc đem cô cạn dung dịch thu được 6,91gam chất rắn X.
TN2: Cho hỗn hợp a gam sắt và b gam Mg vào V lít ( đktc) dung dịch HCl, sau phản ứng thu được 1,12 lít khí H2( ddktc) và cô cạn dung dịch được 7,63 gam chất rắn Y.
a.Tính a,b
b.Tính khối lượng mỗi chất con trong X,Y
( Giả sử Mg không phản ứng với nước, và trong phản ứng với axit, Mg phản ứng trước, hết Mg mới đến Fe, các phản ứng xảy ra hoàn toàn)
Gọi $n_{HCl} = x(mol) ; n_{Fe} = y(mol) ; n_{Mg} = z(mol)$
Thí nghiệm 1 : HCl hết, Fe dư
Fe + 2HCl → FeCl2 + H2
0,5x....x.............0,5x......................(mol)
Ta có :
127.0,5x + (y - 0,5x).56 = 6,91(1)
Thí nghiệm 2 : Mg,HCl hết, Fe dư
Mg + 2HCl → MgCl2 + H2
z.........2z.............z.........z..........(mol)
Fe + 2HCl → FeCl2 + H2
0,5(x - 2z).....(x-2z)...........0,5(x-2z)....0,5(x-2z)......(mol)
Ta có :
$n_{H_2} = z + 0,5(x -2z) = 0,05(2)$
95z + 0,5(x -2z).127 + [y-0,5(x - 2z)].56 = 7,63(3)$
Từ (1)(2)(3) suy ra x = 0,1 ; y = 0,06 ; z = 0,03
Vậy :
a = 0,06.56 = 3,36 gam
b = 0,03.65 = 1,95 gam
Ủa bài này hôm qua chị Phương Thảo làm giúp em rồi mà nhỉ ?
Đốt cháy hoàn toàn 3,4 gam hợp chất hữu cơ X (phân tử chỉ chứa một loại nhóm chức), cho toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thấy xuất hiện 16 gam kết tủa trắng đồng thời khối lượng dung dịch giảm 7,16 gam. Đun nóng 34 gam X trong 500 ml dung dịch NaOH 1M thấy tạo thành chất hữu cơ Y. Phần dung dịch còn lại đem cô cạn thu được 41,6gam chất rắn, trong đó có một muối natri của axit hữu cơ đơn chức. Chất Y phản ứng với Cu(OH)2 cho dung dịch xanh lam. Cho tỉ khối hơi của X so với khí H2 là 85 (ở cùng điều kiện). Các phản ứng hóa học đều xảy ra hoàn toàn. Khẳng định nào sau đây là đúng?
A. X có thể tham gia phản ứng tráng gương.
B. Trong Y, oxi chiếm 56,47% theo khối lượng.
C. Muối tạo thành có thể dùng để điều chế metan trong phòng thí nghiệm.
D. X cộng hợp brom theo tỉ lệ tối đa 1 : 2.
Tiến hành 2 thí nghiệm sau:
Thí nghiệm 1:
Cho a gam Fe hòa tan trong dung dịch HCI,kết thúc thí nghiệm,cô cạn sản phẩm thu được 3,1 gam chất rắn
Thí nghiệm 2:
Nếu cho a gam Fe và b gam Mg và dung dịch HCI (cùng với lượng như trên ) .Kết thúc thí nghiệm cô cạn sản phẩm thu được 3,34 gam chất rắn và thấy giải phóng 0,448 lít khí (đktc.)
Tính a và b?
Biết : \(\left(Mg=24,Fe=56,Na=23,Ca=40,Cu=64,Zn=65,Ba=137\right)\)
Xét thí nghiệm 1:
\(PTHH:Mg+2HC1->FeCI_2+H_2\) (1)
Giả sử Fe phản ứng hết -> Chất rắn là \(FeCI_2\)
\(\Rightarrow n_{Fc}=n_{FeCI_2}=n_{h_2}=\frac{3,1}{127}\approx0,024\left(mol\right)\)
Xét thí nghiệm 2:
\(PTHH:Mg+2HCI->MgCI_2+H_2\)(2)
\(Fe+2HCI->FeCI_2+H_2\) (3)
Ta thấy :Ngoài a gam Fe như thí nghiệm 1 cộng với b gam Mg mà chỉ giải phóng :
\(n_{H_2}=\frac{0,0448}{22,4}=0,024\left(mol\right)\)
-> Chứng tỏ TH1:Fe dư HCI hết :
Ta có \(n_{HCI}\left(TN1\right)=n_{HCI}\left(TN2\right)=2_{n_{H2}}=2.0,02=0,04\left(mol\right)\)
TH1:
\(n_{Fe\left(pư\right)}=n_{nFeCI_2}=\frac{1}{2}n_{HCI}=\frac{1}{2}.0,04=0,02\left(mol\right)\)
\(\Rightarrow m_{fe\left(dư\right)}=3,1-0,02.127=0,56\left(gam\right)\)
\(m_{Fe\left(dư\right)}=0,02.56=1,12\left(gam\right)\)
\(\Rightarrow m_{Fe}=a=0,56+1,12=1,68\left(gam\right)\)
TN2:
Áp dụng ĐLBTKL :
\(a+b=3,34+0,02.2-0,04.36,5=1,92\left(g\right)\)
Mà \(a=1,68gam->b=1,92-1,68=0,24\left(g\right)\)
P/s:Thằng lười :v
ủa sao thí nghiệm 1 lại có mg vậy, vô lý quá
Trên bàn thí nghiệm có những chất rắn màu trắng là :
Na 2 SO 3 , K 2 CO 3 , CaCO 3 , NaHCO 3 , Na 2 CO 3 , CaSO 4 .
Bạn em đã lấy một trong những chất trên bàn để làm thí nghiệm và có kết quả như sau :
Thí nghiệm 1
Cho tác dụng với dung dịch HCl, thấy giải phóng khí cacbon đioxit.
Thí nghiệm 2
Khi nung nóng cũng thấy giải phóng khí cacbon đioxit.
Thí nghiệm 3
Chất rắn còn lại sau khi nung ở thí nghiệm 2 tác dụng với dung dịch HCl cũng thấy giải phóng khí cacbon đioxit.
Em hãy cho biết bạn em đã lấy chất nào trên bàn để làm thí nghiệm. Viết các phương trình hoá học.
Hướng dẫn :
TN1 cho biết chất đem làm thí nghiệm là muối cacbonat hoặc hiđrocacbonat ( K 2 CO 3 , CaCO 3 , NaHCO 3 , Na 2 CO 3 ).
K 2 CO 3 + 2HCl → 2KCl + H 2 O + CO 2
CaCO 3 + 2HCl → CaCl 2 + H 2 O + CO 2
NaHCO 3 + HCl → NaCl + H 2 O + CO 2
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
TN2 cho biết muối đem làm thí nghiệm là CaCO 3 hoặc NaHCO 3 , là những muối bị phân huỷ ở nhiệt độ cao.
CaCO 3 → CaO + CO 2
2 NaHCO 3 → Na 2 CO 3 + CO 2 + H 2 O
TN3 cho biết sản phẩm thu được ở thí nghiêm 2 phải là muối cacbonat, không thể là canxi oxit CaO.
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
Kết luận : Bạn em đã lấy muối NaHCO 3 làm thí nghiệm.
Viết các phương trình hoá học của phản ứng xảy ra trong ba thí nghiệm trên.
| Hiện tượng | Giải thích. Viết PTHH |
|
Mẩu natri chuyển động như thế nào ? Mẩu natri có giữ mguyên hình dạng ban đầu không ? Khí thoát ra là khí gì ? Cách chứng minh khí đó. Sau khi kết thúc thí nghiệm, lấy 1 ml dung dịch đem cô cạn trên mặt kính đồng hồ sẽ thấy chất rắn trắng tạo thành, đó là natri hiđroxit (NaOH). Viết PTHH của phản ứng xảy ra. |
.................................... .................................... .................................... .................................... .................................... .................................... .................................... ................................... |
Mẩu natri chuyển động hình xoắn ốc từ ngoài chạy vào giữa.
Mẩu natri tan dần
Khí thoát ra là H2
Để biết khí này là khí gì thì ta đốt khí này trong kk nếu thấy khí này cháy với ngọn lửa màu xanh và tạo hơi nước.
2Na + 2H2O -> 2NaOH + H2
Hấp thụ hết a mol khí CO2 vào dung dịch chứa hỗn hợp KOH và Ba(OH)2. Kết quả thí nghiệm được biểu diễn theo sơ đồ sau:
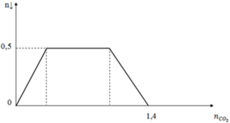
Khi a = 1, lọc bỏ kết tủa sau đó cô cạn dung dịch rồi nung chất tạo thành ở nhiệt độ cao đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là?
A. 47,3
B. 59,7
C. 42,9
D. 34,1