có 100ml dung dịch X H2SO4 80 phần trăm D=1,75g/ml.đem pha loãng dung dịch H2SO4 80 phần trăm bằng V (ml) nước cất ta thu được dd H2SO4 20 phần trăm. Cho biết khối lượng riêng của nc cất (D) bằng 1g/ml .Tính giá trị của V.
ai giúp với !!
Để thu được 500 ml dung dịch H2SO4 2M cần lấy m gam H2SO4 đặc 98% (D = 1,87 gam/ml) và V ml nước cất. Coi quá trình pha loãng không làm thay đổi thể tích chất lỏng. a. Tính giá trị của m, V và nồng độ phần trăm của dung dịch H2SO4 2M thu được ở trên. b. Trình bày cách pha loãng để thu được dung dịch H2SO4 2M ở trên.
Bạn em đã pha loãng axit bằng cách rót từ từ 20g dung dịch H2SO4 50% vào nước và sau đó thu được 50g dung dịch H2SO4.
a) Tính nồng độ phần trăm của dung dịch H2SO4 sau khi pha loãng.
b) Tính nồng độ mol của dung dịch H2SO4 sau khi pha loãng biết rằng dung dịch này có khối lượng riêng là 1,1g/cm3.
Có 100ml dung dịch H2SO4 98%, khối lượng riêng là 1,84 g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
Tính thể tích nước cần dung để pha loãng.
Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên: 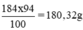
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất: 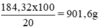
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.
người ta pha 150g dd H2SO4 30%vào 50ml dd h2so4 1M (có khối lượng riêng D=1,07g/ml).tính nồng độ phần trăm dd thu đc
Ta có: \(m_{H_2SO_4}=150\cdot30\%+0,05\cdot1\cdot98=49,9\left(g\right)\)
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{49,9}{150+50\cdot1,07}\cdot100\%\approx24,52\%\)
Hòa tan hoàn toàn 11,84g hỗn hợp X gồm Fe và Cu trong 90g dung dịch H2SO4(đặc, nóng). Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y và V lít SO2 (sản phẩm khử duy nhất, đktc). Đổ 124,8ml nước cất vào Y, thu được 200g dung dịch Z, trong đó nồng độ H2SO4 là 13,72%.
a/ Tính giá trị của V và phần trăm khối lượng của mỗi kim loại trong X.
b/ Tính nồng độ phần trăm của H2SO4 ban đầu.
(Khối lượng riêng của nước nguyên chất là 1g/ml)
Cho 9,75 gam kẽm tác dụng vừa đủ với 500ml dd H2SO4 (D= 1,2g/ml).
a. Viết PTHH.
b. Tính khối lượng H2SO4 tham gia phản ứng.
c. Tính nồng độ phần trăm của dung dịch H2SO4.
d. Tính nồng độ phần trăm của dung dịch muối sau phản ứng.
a)\(PTHH:Zn+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2\)
b)Số mol của kẽm là:
\(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\)
\(PTHH:Zn+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2\)
tỉ lệ : 1 1 1 1 (mol)
số mol : 0,15 0,15 0,15 0,15 (mol)
Khối lượng H2SO4 tham gia phản ứng là:
\(m_{H_2SO_4}=0,15.98=14,7\left(g\right)\)
c)Khối lượng của dung dịch H2SO4 là:
\(m_{ddH_2SO_4}=D.V_{dd}=500.1,2=600\left(g\right)\)
Nồng độ phần trăm của dung dịch H2SO4 là:
\(C_{\%H_2SO_4}=\dfrac{m_{H_2SO_4}}{m_{ddH_2SO_4}}.100\%=\dfrac{14,7}{600}.100\%=2,45\%\)
d) Khối lượng của khí H2 là:
\(m_{H_2}=0,15.2=0,3\left(g\right)\)
Khối lượng của ZnSO4 là:
\(m_{ZnSO_4}=0,15.161=24,15\left(g\right)\)
Khối lượng của dung dịch ZnSO4 là:
\(m_{ddZnSO_4}=9,75+600-0,3=609,45\left(g\right)\)
Nồng độ dung dịch của muối sau phản ứng là:
\(C_{\%ZnSO_4}=\dfrac{m_{ZnSO_{\text{4}}}}{m_{ddZnSO_4}}.100\%=\dfrac{24,15}{609,45}.100\%=3,9\%\)
1. Trộn 400ml dd KOH 1,5M với 600ml dd KOH 1,2M. Tính nồng độ mol và nồng động phần trăm của của dd sau khi trộn dung dịch sau trộn có khối lượng riêng bằng 1,12g/ml?
2.
a/ Trộn lẫn 100 gam dd H2SO4 10% với 200 gam dd H2SO4 C% thu được dd H2SO4 30%. Tính C%
b/ Trong Cho m gam NaCl vào nước được 200 gam dung dịch NaCl 15%. Tính nồng độ mol của dung dich NaCl. Biết dung dich NaCl có D= 1,1g/ml
2
b
mNaCl=\(\dfrac{200.15}{100}\)=30(g)
nNaCl=\(\dfrac{30}{58,5}\)=0.51(mol)
VddNaCl=\(\dfrac{200}{1,1}\)=181.8(ml)=0.1818(l)
CMNaCl=\(\dfrac{0,51}{0,1818}\)=2.8(M)
a,tính khối lượng NaOH có trong 200ml dung dịch NaOh 1M b,tính số mol H2SO4 có trong 100ml dung dịch H2SO4 2M c,hoà tan 6g NaCl vào nước thu được 200g dung dịch tính nồng độ phần trăm của dung dịch d,tính khối lượng NaCl có trong 200g dung dịch NaCl 8%
a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)
Cho 22,2 gam hỗn hợp A gồm Al, Fe vào cốc đựng 200 ml dung dịch H2SO4 4M, khuấy đều cho các phản ứng hoàn toàn, thu được 13,44 lít khí H2 (đktc). Pha loãng phần dung dịch sau phản ứng bằng nước, thu được 500 ml dung dịch B có khối lượng riêng d = 1,2 g/ml.
1) Hãy cho biết hỗn hợp A phản ứng hết hay không?
2) Tính % theo khối lượng của mỗi kim loại trong hỗn hợp A.
3) Tính nồng độ mol/lit và nồng độ % khối lượng của dung dịch B.
Giúp mình vs ạ mai mình phải nộp rùi. Thanks :3