tỉ khối của khí A đối với oxi là 0,9375 .lập luận để xác định công thức hóa học của A . biết rằng khi đốt cháy A chỉ thu được khí cacbonic và hơi nước .

Những câu hỏi liên quan
tỉ khối của khí A đối với oxi là 0,9375 .lập luận để xác định công thức hóa học của A . biết rằng khi đốt cháy A chỉ thu được khí cacbonic và hơi nước .
Để đốt cháy hết 16 g hợp chất X cần 44,8 lít khí oxi (điều kiện tiêu chuẩn) . Sau khi kết thúc phản ứng chỉ thu được CO2 và hơi nước theo tỉ lệ số mol là 1 : 2 . Xác định công thức hóa học của x biết công thức đơn giản chính là công thức hóa học
Gọi số mol CO2, H2O là a, b
=> 2a = b
\(n_{O_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
Theo ĐLBTKL: 44a + 18b = 16 + 2.32 = 80
=> a = 1; b = 2
Bảo toàn C: nC = 1(mol)
Bảo toàn H: nH = 4 (mol)
Xét mC + mH = 1.12 + 4.1 = 16(g)
=> X chỉ chứa C và H
nC : nH = 1 : 4
=> CTPT: CH4
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít oxi (đkt) và thu được thể tích CO2 bằng 2 phần 3 thể tích hơi nước. Xác định công thức hoá của A. Biết rằng tỉ khối hơi của A so với khí oxi là 1,4375.
Tham khảo:
Đốt cháy A chỉ tạo ra CO2 và H2O nên A chứa C;H;O
Vậy A có dạng CxHyOz
Phản ứng xảy ra:
CxHyOz+(x+y/4−z/2)O2to→xCO2+y2H2O
Ta có:
MA=1,4375MO2=1,4375.32=46
→12x+y+16z=46
Ta có:
nA=23/46=0,5 mol
nO2=33,6/22,4=1,5 mol
→x+y/4−z/2=nO2/nA=1,5/0,5=3
Ta có:
nCO2:nH2O=x:y2=2:3→x:y=2:6=1:3
Giải được: x=2;y=6;y=1
Vậy A là C2H6O
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 0,1 mol khí CxHy cần 6,72 lít khí oxi (ở đktc). Sau phản ứng thu được 8,8 gam khí cacbonic và 3,6 gam nước. Tính Khối lượng mol và xác định công thức hóa học của CxHy, biết tỉ lệ giữa x và y là 1:2.
$n_{CO_2} = \dfrac{8,8}{44} = 0,2(mol) ; n_{H_2O} = \dfrac{3,6}{18} = 0,2(mol)$
$C_xH_y + (x + \dfrac{y}{4})O_2 \xrightarrow{t^o} xCO_2 + \dfrac{y}{2}H_2O$
Theo PTHH :
$0,1.x = 0,2$ và $0,1.\dfrac{y}{2} = 0,2$
Suy ra : x = 2 ; y = 4
Vậy CTHH cần tìm là $C_2H_4$(M = 28)
Đúng 0
Bình luận (0)
Đốt cháy 4,5g chất hữu cơ A thu được 6,6g khí cacbonic và 2,7g nước. Xác định công thức phân tử hợp chất hữu cơ A. Viết tỉ khối hơi của chất hữu cơ với không khí là 2,069
Vì đốt cháy A thu CO2 và H2O nên A gồm C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\Rightarrow n_H=0,15.2=0,3\left(mol\right)\)
⇒ mC + mH = 0,15.12 + 0,3.1 = 2,1 (g) < mA
Vậy: A gồm C, H và O.
⇒ mO = 4,5 - 2,1 = 2,4 (g) \(\Rightarrow n_O=\dfrac{2,4}{16}=0,15\left(mol\right)\)
Giả sử: CTPT của A là CxHyOz
⇒ x : y : z = 0,15 : 0,3 ; 0,15 = 1:2:1
⇒ CTĐGN của A là (CH2O)n.
Có: \(M_A=29.2,069\approx60\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{60}{12+2.1+16}=2\)
Vậy: A là C2H4O2.
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
.Đốt cháy hoàn toàn 11,2 lít hợp chất A bởi Oxi thu được 11,2 lít khí cacbonic và 18 gam nước. Xác định công thức của A, biết rằng tỷ khối của khí A so với khí H2 bằng 8 (giả sử các khi đều đo ở đktc)help me
$n_{CO_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
$n_{H_2O} = \dfrac{18}{18} = 1(mol)$
Bảo toàn nguyên tố C,H :
$n_C = n_{CO_2} = 0,5(mol)$
$n_H = 2n_{H_2O} = 2(mol)$
$n_A = \dfrac{11,2}{22,4} = 0,5(mol)$
Số nguyên tử $C = \dfrac{0,5}{0,5} = 1$
Số nguyên tử $H = \dfrac{2}{0,5} = 4$
Mà : $M_A = 8.2 = 16$
$\Rightarrow A$ là $CH_4$
Đúng 1
Bình luận (0)
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít
O
2
. Sản phẩm thu được chỉ gồm có 1,80 g
H
2
O
và 2,24 lít
C
O
2
. Các thể tích khí đo ở đktc.1. Xác định công thức đơn giản nhất của A.2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.3. Xác định công thức cấu tạo có thể có của chất A, ghi...
Đọc tiếp
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít O 2 . Sản phẩm thu được chỉ gồm có 1,80 g H 2 O và 2,24 lít C O 2 . Các thể tích khí đo ở đktc.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.
3. Xác định công thức cấu tạo có thể có của chất A, ghi tên tương ứng, biết rằng A là hợp chất cacbonyl.
1. Theo định luật bảo toàn khối lượng:
m A = m C O 2 + m H 2 O − m O 2
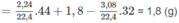
Khối lượng C trong 1,8 g A là: 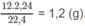
Khối lượng H trong 1,8 g A là: 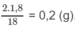
Khối lượng O trong 1,8 g A là : 1,8 - 1,2 - 0,2 = 0,4 (g).
Công thức chất A có dạng C x H y O z :
x : y : z = 0,1 : 0,2 : 0,025 = 4 : 8 : 1
CTĐGN là C 4 H 8 O
2. M A = 2,25.32 = 72 (g/mol)
⇒ CTPT trùng với CTĐGN: C 4 H 8 O .
3. Các hợp chất cacbonyl C 4 H 8 O :
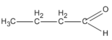 (butanal)
(butanal)
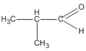 (2-metylpropanal)
(2-metylpropanal)
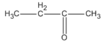 (butan-2-ol)
(butan-2-ol)
Đúng 0
Bình luận (0)
a/ Đốt cháy hoàn toàn 1 lít khí (Y) cần 6,5 lít khí oxi. Sau phản ứng thu được 4 lít khí cacbonic và 5 lít hơi nước. Xác định công thức phân tử của (Y) và viết công thức cấu tạo. b/ Đốt cháy 100ml hơi khí (Z) cần 300ml oxi. Sản phẩm thu được 200ml khí CO, và 200ml hơi nước. Tìm công thức phân tử của (Z). Phân tử khối của (Z) bằng bao nhiêu? Biết rằng các khí và hơi nước đo ở cùng điều kiện nhiệt độ và áp suất.
Đọc tiếp
a/ Đốt cháy hoàn toàn 1 lít khí (Y) cần 6,5 lít khí oxi. Sau phản ứng thu được 4 lít khí cacbonic và 5 lít hơi nước. Xác định công thức phân tử của (Y) và viết công thức cấu tạo. b/ Đốt cháy 100ml hơi khí (Z) cần 300ml oxi. Sản phẩm thu được 200ml khí CO, và 200ml hơi nước. Tìm công thức phân tử của (Z). Phân tử khối của (Z) bằng bao nhiêu? Biết rằng các khí và hơi nước đo ở cùng điều kiện nhiệt độ và áp suất.
Giải thích các bước giải:
⋅⋅ 2Cu+O2→to2CuO2
Do đun trong không khí 1 thời gian
⇒ A: CuO,Cudư
⋅⋅ Hòa tan A trong H2SO4 đặc nóng
CuO+H2SO4→CuSO4+H2O
Cu+2H2SO4→toCuSO4+SO2+2H2O
ddB:CuSO4
khíD:SO2
⋅⋅cho Na vào dd CuSO44 thì Na sẽ tác dụng với H2O2 ở trong muối trước sau đó sẽ tác dụng với CuSO4
2Na+2H2O→2NaOH+H22
2NaOH+CuSO4→Cu(OH)2⏐↓+Na2SO42
Khí G:H2
Kết tủa M:Cu(OH)2
⋅⋅Cho SO2 vào KOH
SO2+2KOH→K2SO3
K2SO3+SO2+H2O→2KHSO
K2SO3+BaCl2→BaSO3↓+2KCl
2KHSO3+2NaOH→K2SO3+Na2SO3+2H2O
Đúng 0
Bình luận (1)
Đốt cháy hoàn toàn 23g hợp chất A cần 33,6 lít oxi (đ.k.t.c) và thu được thể tích \(CO_2\) bằng 2/3 thể tích hơi nước. Xác định CTHH của A. Biết rằng tỉ khối hơi của A si với khí oxi là 1,4375
Vì đốt cháy A sinh ra \(CO_2\)và nước nên \(\Rightarrow\)hợp chất ban đầu chứa C,H,O
\(M_A=1,4375.32=46\left(đvC\right)\)
Vì tỉ lệ thể tích cũng là tỉ lệ mol nên: \(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\)vì \(n_{CO_2}< n_{H_2O}\)
\(\Rightarrow\)Hợp chất A no
Gọi A có CTC là \(C_nH_{2n+2}O\)và số mol A là 1 mol, ta có:
\(C_nH_{2n+2}O+\dfrac{3n}{2}O_2\rightarrow nCO_2+\left(n+1\right)H_2O\)
\(\dfrac{n}{n+1}\)\(=\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\)⇒ n=2
\(C_2H_6O\)(46 đvC)
Đúng 2
Bình luận (0)





















