Đốt cháy lưu huỳnh trong 1 bình kín chứa không khí .Sau khi đốt cháy xong đưa về nhiệt độ ban đầu .Hãy tính tỷ khối của hỗn hợp khí sau phản ứng so với H2 và O2

Những câu hỏi liên quan
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, thu được hỗn hợp ba khí (CO2, SO2, O2). Sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ thay đổi như thế nào? A. Tăng. B. Giảm. C. Có thể tăng hoặc giảm phụ thuộc vào lượng S và C. D. Không đổi.
Đọc tiếp
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, thu được hỗn hợp ba khí (CO2, SO2, O2). Sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ thay đổi như thế nào?
A. Tăng.
B. Giảm.
C. Có thể tăng hoặc giảm phụ thuộc vào lượng S và C.
D. Không đổi.
Đáp án D
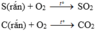
Từ 2 phương trình trên ta thấy số mol khí của chất tham gia phản ứng và sau phản ứng bằng nhau và không phụ thuộc vào lượng C, S => do vậy áp suất của bình sẽ không thay đổi khi ta đưa về nhiệt độ ban đầu
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng khí oxi dư, sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ: A. tăng, giảm hoặc không đổi phụ thuộc lượng C, S B. tăng C. giảm D. không đổi
Đọc tiếp
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng khí oxi dư, sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ:
A. tăng, giảm hoặc không đổi phụ thuộc lượng C, S
B. tăng
C. giảm
D. không đổi
đốt cháy lưu huỳnh trong bình đựng không khí thì lưu huỳnh và oxi phản ứng vừa hết .Tính khối lượng của 16,8 lít hỗn hợp khí sau khi đốt cháy lưu huỳnh nếu lưu huỳnh cháy hết oxi còn dư .Tính phần trăm các khí sau phản ứng biết 1 mol hỗn hợp khí sau phản ứng nặng 33,6 gam
\(n_{hhkhí}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
Gọi \(n_{SO_2}=a\left(mol\right)\left(0< a< 0,75\right)\)
\(\rightarrow n_{O_2\left(dư\right)}=0,75-b\left(mol\right)\)
Ta có: \(\dfrac{64a+32\left(0,75-a\right)}{0,75}=\dfrac{33,6}{1}=33,6\left(\dfrac{g}{mol}\right)\)
\(\rightarrow a=0,0375\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}\%V_{SO_2}=\dfrac{0,0375}{0,75}=5\%\\\%V_{O_2\left(dư\right)}=100\%-5\%=95\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
đốt cháy lưu huỳnh trong bình đựng không khí thì lưu huỳnh và oxi vừa hết .Tính khối lượng của 16,8 lít hỗn hợp khí sau khi đốt cháy lưu huỳnh nếu lưu huỳnh cháy hết oxi còn dư .Tính % các khí sau phản ứng biết 1 mol hỗn hợp khí sau phản ứng nặng 33,6 gam
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ A.Tăng, giảm hoặc không đổi phụ thuộc lượng C, S. B.Tăng C.Giảm D. Không đổi
Đọc tiếp
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ
A.Tăng, giảm hoặc không đổi phụ thuộc lượng C, S.
B.Tăng
C.Giảm
D. Không đổi
Chọn đáp án D
Nhận xét thấy ngay
C + O2 → CO2
và S + O2 → SO2 .
Do đó số mol khí không thay đổi trong quá trình phản ứng
Đúng 0
Bình luận (0)
Đốt cháy x(gam) cacbon trong bình kín chứa 32 gam O2.Khi phản ứng xong trong bình kín không còn chất rắn mà chỉ chứa hỗn hợp khí có tỉ khối hơi so với khí hidro là 19. [Các khí đo cùng điều kiện nhiệt độ và áp suất] a.Hỗn hợp khí trong bình là khí gì?Tính thành phần phần trăm về thể tích mỗi khí trong hỗn hợp; b.Tính khối lượng cacbon ban đầu(Tính x);
Đọc tiếp
Đốt cháy x(gam) cacbon trong bình kín chứa 32 gam O2.Khi phản ứng xong trong bình kín không còn chất rắn mà chỉ chứa hỗn hợp khí có tỉ khối hơi so với khí hidro là 19. [Các khí đo cùng điều kiện nhiệt độ và áp suất]
a.Hỗn hợp khí trong bình là khí gì?Tính thành phần phần trăm về thể tích mỗi khí trong hỗn hợp;
b.Tính khối lượng cacbon ban đầu(Tính x);
Hỗn hợp khí sau phản ứng gồm CO;CO2
2C+O2to→2CO
C+O2→toCO2
Mhh¯=19MH2=19.2=38
Áp dụng quy tắc đường chéo:
CO(28) 6
hh(38)
CO2(44) 10
→nCO\nCO2=6\10=3\5
→%nCO=3\3+5=37,5%→%nCO2=62,5%
Giả sử số mol CO là 3a suy ra số mol CO2 là 5a.
→nO2=1\2nCO+nCO2=3a\2+5a=6,5a=32\32=1
→a=2\13→nC=nCO2+nCO=2a=4\13→mC=4\13.12=3,692 gam = x
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn m1 gam muối KClO3 ở trên, thu toàn bộ khí oxi thoát ra cho vào bình kín chứa không khí sao cho tỉ lệ thể tích . Cho hỗn hợp Y chứa m2 gam cacbon và lưu huỳnh vào bình rồi đốt cháy, lượng oxi trong bình vừa đủ để cháy hết Y. Sau phản ứng thu được hỗn hợp khí Z gồm 3 khí, trong đó khí SO2 chiếm 20% về thể tích.a) Tìm tỉ khối của khí Z đối với H2.b) Đưa nhiệt độ trong bình về 0 độ C, áp suất 760mmHg thì khí Z có thể tích là 13,44 lít. Tính m1, m2. Cho rằng không khí chứa 80% n...
Đọc tiếp
Nhiệt phân hoàn toàn m1 gam muối KClO3 ở trên, thu toàn bộ khí oxi thoát ra cho vào bình kín chứa không khí sao cho tỉ lệ thể tích . Cho hỗn hợp Y chứa m2 gam cacbon và lưu huỳnh vào bình rồi đốt cháy, lượng oxi trong bình vừa đủ để cháy hết Y. Sau phản ứng thu được hỗn hợp khí Z gồm 3 khí, trong đó khí SO2 chiếm 20% về thể tích.
a) Tìm tỉ khối của khí Z đối với H2.
b) Đưa nhiệt độ trong bình về 0 độ C, áp suất 760mmHg thì khí Z có thể tích là 13,44 lít. Tính m1, m2. Cho rằng không khí chứa 80% nitơ và 20% oxi về thể tích.
6/ Một bình kín dung tích 8,96 lít (đktc) chứa đầy hỗn hợp X gồm N2, O2, SO2 (Tỉ lệ mol tương ứng là 2:1:1). Đốt cháy hết một lượng lưu huỳnh trong hỗn hợp X rồi đưa bình về nhiệt độ ban đầu thì thu được hỗn hợp khí Y. Biết dY/X 1,1684. a/ Áp suất trong bình có thay đổi hay không? Vì sao? b/ Xác định phần trăm thể tích của hỗn hợp khí Y c/ Chứng minh: Khi lượng lưu huỳnh biến đổi thì 1 dY/X 1,21 các Mod Hoidap247 vào giúp với ạ
Đọc tiếp
6/ Một bình kín dung tích 8,96 lít (đktc) chứa đầy hỗn hợp X gồm N2, O2, SO2 (Tỉ lệ mol tương ứng là 2:1:1). Đốt cháy hết một lượng lưu huỳnh trong hỗn hợp X rồi đưa bình về nhiệt độ ban đầu thì thu được hỗn hợp khí Y. Biết dY/X = 1,1684. a/ Áp suất trong bình có thay đổi hay không? Vì sao? b/ Xác định phần trăm thể tích của hỗn hợp khí Y c/ Chứng minh: Khi lượng lưu huỳnh biến đổi thì 1< dY/X 1,21 các Mod Hoidap247 vào giúp với ạ
a, Áp suất trong bình không thay đổi vì quá trình đốt cháy lưu huỳnh trong hỗn hợp X là quá trình xảy ra ở áp suất không đổi và sau khi đốt cháy, các sản phẩm khí sinh ra có cùng nhiệt độ và áp suất với hỗn hợp ban đầu.
b,Để tính phần trăm thể tích của hỗn hợp khí Y, ta cần biết tỉ lệ mol của các khí trong hỗn hợp Y. Theo phương trình phản ứng, khi đốt cháy lưu huỳnh trong hỗn hợp X, ta có:
S + O2 → SO2
Vì tỉ lệ mol giữa N2, O2 và SO2 trong hỗn hợp X là 2:1:1 nên khi đốt cháy hết lưu huỳnh, tỉ lệ mol giữa N2 và O2 trong hỗn hợp Y sẽ là 2:5. Do đó, ta có:
Tổng số mol khí trong hỗn hợp Y: 2 + 5 = 7 (vì tỉ lệ mol giữa N2 và O2 là 2:5)
Phần trăm thể tích của hỗn hợp Y: \(d\dfrac{Y}{X}\) = \(\dfrac{V_Y}{V_X}\) = \(\dfrac{n_Y.\dfrac{RT}{P}}{n_X.\dfrac{RT}{P}}=\dfrac{n_Y}{n_X}\) = 7/4 ≈ 175%
Vậy phần trăm thể tích của hỗn hợp khí Y là khoảng 175%.
c, Ta có:
\(d\dfrac{Y}{X}=\dfrac{V_Y}{V_X}=\dfrac{n_Y.\dfrac{RT}{P}}{n_X.\dfrac{RT}{P}}=\dfrac{n_Y}{n_X}\)
Với mỗi mol lưu huỳnh đốt cháy, số mol khí trong hỗn hợp Y tăng thêm 2, do đó nY = nX + 2 nhân số mol lưu huỳnh đốt cháy.
Từ đó suy ra: dY/X = (nX + 2 . số mol lưu huỳnh đốt cháy) / nX = 1 + 2 . số mol lưu huỳnh đốt cháy / nX
Do đó:
1 dY/X 1,21 tương đương với (dY/X) / 1,1684 = 1 + 2 . số mol lưu huỳnh đốt cháy / nX / 1,1684
=> 1,21 / 1,1684 - 1 = 2 . số mol lưu huỳnh đốt cháy / nX
=> số mol lưu huỳnh đốt cháy / nX = 0,0217
=> số mol lưu huỳnh đốt cháy = 0,0217 . nX
Vậy khi lượng lưu huỳnh biến đổi, 1 dY/X tăng thêm 2 . 0,0217 = 0,0434.
Đúng 1
Bình luận (0)
Đốt cháy lưu huỳnh trong bình đựng không khí, lưu huỳnh cháy hết. Tính tỉ khối đối với He của hỗn hợp khí thu được sau phản ứng, nếu oxi trong bình vừa đủ đốt cháy hết S.
Nitơ chiếm 80% thể tích không khí, điều đó có nghĩa là trong không khí mỗi khi có 1 mol oxi sẽ có 4 mol nitơ.
S + O 2 → S O 2
Khi tạo thành 1 mol S O 2 hì hỗn hợp thu được gồm 1 mol S O 2 và 4 mol N 2
![]()
Tỉ khối của hỗn hợp đối với He là : d = 35,2/4 = 8,8
Đúng 0
Bình luận (0)
















