Một hỗn hợp gồm CO2;SO2;C2H2 có tỉ khối so với CH4 là 3.55
Tính % về thể tích và % về khối lượng của mỗi chất có trong hỗn hợp ban đầu biết SO2 có thể tích gấp đôi O2 trong hỗn hợp
1. Một hỗn hợp khí (X) gồm CO, CO2 và đơn chất (A). Biết % vể thể tích từng khí trong hỗn hợp khí (X) gồm CO, CO2 và đơn chất (A) tương ứng là 40%, 30% và 30%. Trong hỗn hợp khí CO2 chiếm 52,8% về khối lượng hỗn hợp khí (X).
a. Tìm công thức hóa học của khí (A). Các khí đo trong cùng điều kiện nhiệt độ và áp suất.
b. Có thể thu khí (A) vào bình (từ những thí nghiệm trong phòng thí nghiệm) bằng cách đặt bình thế nào (đứng bình,…)? Vì sao?
Một hỗn hợp gồm CaO và BaO có khối lượng 20,9g tác dụng với CO2 tạo 29,7 g hỗn hợp 2 muối. Tính thể tích CO2 đã tham gia phản ứng và khối lượng mỗi oxit trong hỗn hợp ban đầu
Gọi \(x,y\) lần lượt là số mol của \(CaO,BaO\)
\(m_{CaO}+m_{BaO}=m_{hh}\\ \rightarrow56x+153y=20,9\left(1\right)\)
\(PTHH:CaO+CO_2\rightarrow CaCO_3\downarrow+H_2O\\ \left(mol\right)--x\rightarrow--x---x---x\\ PTHH:BaO+CO_2\rightarrow BaCO_3\downarrow+H_2O\\ \left(mol\right)--y\rightarrow--y---y---y\)
\(m_{CaCO_3}+m_{BaCO_3}=m_{muối}\\ \rightarrow100x+197y=29,7\left(2\right)\)
Từ (1) và (2) ta có hpt: \(\left\{{}\begin{matrix}56x+153y=20,9\\100x+197y=29,7\end{matrix}\right.\)
\(\leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{CaO}=\dfrac{56.0,1}{20,9}.100\%=26,8\%\\\%m_{BaO}=100\%-26,8\%=73,2\%\end{matrix}\right.\\ \rightarrow V_{CO_2}=\left(x+y\right).22,4=\left(0,1+0,1\right).22,4=4,48\left(l\right)\)
Hỗn hợp X gồm các hợp chất hữu cơ đều mạch hở gồm một axit cacboxylic, một ancol và một este (trong phân tử mỗi chất chỉ chứa một loại nhóm chức). Đốt cháy hoàn toàn 20,36 gam X, thu được 38,28 gam CO2 và 17,28 gam H2O. Mặt khác, cho 20,36 gam X tác dụng vừa đủ với dung dịch NaOH, thu được một ancol Y hai chức và hỗn hợp Z gồm các muối. Đốt cháy toàn bộ Z cần dùng 0,5 mol O2, thu được 6,89 gam Na2CO3 và 0,71 mol hỗn hợp gồm CO2 và H2O. Phần trăm khối lượng của axit trong hỗn hợp X là.
A. 36,45%.
B. 20,63%.
C. 25,44%.
D. 29,47%.
Chọn đáp án C
Ta có: X → c h á y C O 2 : 0 , 87 H 2 O : 0 , 96 → n O t r o n g X = 0 , 5
Khi muối cháy → n N a 2 C O 3 = 0 , 065 → C O 2 : 0 , 355 H 2 O : 0 , 355 → gốc muối là no, đơn chức.
![]()
Xếp hình cho C

Hỗn hợp X gồm các hợp chất hữu cơ đều mạch hở gồm một axit cacboxylic, một ancol và một este (trong phân tử mỗi chất chỉ chứa một loại nhóm chức). Đốt cháy hoàn toàn 20,36 gam X, thu được 38,28 gam CO2 và 17,28 gam H2O. Mặt khác, cho 20,36 gam X tác dụng vừa đủ với dung dịch NaOH, thu được một ancol Y hai chức và hỗn hợp Z gồm các muối. Đốt cháy toàn bộ Z cần dùng 0,5 mol O2, thu được 6,89 gam Na2CO3 và 0,71 mol hỗn hợp gồm CO2 và H2O. Phần trăm khối lượng của axit trong hỗn hợp X là.
A. 36,45%.
B. 20,63%.
C. 25,44%.
D. 29,47%.
Đáp án C
Ta có: 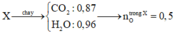
Khi muối cháy 
→ gốc muối là no, đơn chức.
![]()
![]()
Xếp hình cho C 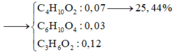
Có một hỗn hợp khí gồm: O2; CO2; CO. Làm thế nào để thu được CO2 tinh khiết?
Đốt hỗn hợp khí để thu CO2
PTHH: \(CO+\dfrac{1}{2}O_2\xrightarrow[]{t^o}CO_2\)
Dẫn hh khí qua Ca(OH)2 dư sau đó lọc lấy kết tủa CaCO3 rồi đem đi nung nóng thu được chất khí đó là CO2
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\\ CaCO_3\underrightarrow{t^o}CaO+CO_2\uparrow\)
Một hỗn hợp X gồm 8,8 gam CO2 và 19,2 gam SO2. Tính tỉ khối của X đối với:
a, Khí hydrogen.
b, Hỗn hợp khí Y gồm: 0,1 mol CH4 và 0,4 mol N2
Một hỗn hợp X gồm axetilen và vinyl axetilen. Tính số mol O 2 cần dùng để đốt cháy hoàn toàn 13 gam hỗn hợp trên thu được sản phẩm cháy gồm CO 2 và H 2 O .
A. 1,0 mol
B. 0,75 mol
C. 0,50 mol
D. 1,25 mol
Một hỗn hợp khí A gồm 0,5 mol O2; 0,1 mol CO2 và 1,4 mol CH4 . Tính khối lượng và thể tích của hỗn hợp A ?
\(\left\{{}\begin{matrix}V_{khí}=\left(0,5+0,1+1,4\right)\cdot22,4=44,8\left(l\right)\\m_{khí}=0,5\cdot32+0,1\cdot44+1,4\cdot16=42,8\left(g\right)\end{matrix}\right.\)
một hỗn hợp gồm Co2 và khí A. TRong hỗn hợp trên, Co2 chiếm 82,5% về khối lượng: A chiếm 25% về thể tích. Tính khối lượng mol của A. Viết CTHH của 3 chất có PTK như trên
Coi \(n_{hỗn\ hợp} = 1(mol)\)
Suy ra : \(n_A = 1.25\% = 0,25(mol) ; n_{CO_2} = 0,75(mol)\)
Trong đó, CO2 chiếm 82,5% về khối lượng :
\(\%m_{CO_2} = \dfrac{0,75.44}{0,75.44 + 0,25A}.100\% = 82,5\%\\ \Rightarrow A = 28(đvC)\)
CTHH của 3 chất có PTK như trên : \(N_2 , C_2H_4 , CO\)
một hỗn hợp khí gồm 0,25 mol H2 , 1,5 mol CO2 ; 0,75 mol SO2 Tính số nguyên tử O có mặt trong hỗn hợp trên
nO (H2O) = nH2O = 0,25 mol
nO (CO2) = 2nCO2 = 2 . 1,5 = 3 mol
nO (SO2) = 2nSO2 = 2 . 0,75 = 1,5 mol
\(\sum n_O=0,25+3+1,5=4,75\left(mol\right)\)
Số nguyên tử O = \(4,75\times6\times10^{23}=28,5\times10^{23}\)