cho Zn tác dụng với HCl biết khối lượng Zn phản ứng 6,5g
a, tính khối lượng HCl đã dùng
b, tính thể tích khí thu được
Cho 6,5g Zn tác dụng với axit HCl ( dư ). a/. Tính khối lượng muối ZnCl2 sinh ra. b/. Tính thể tích H2 sinh ra sau phản ứng. c/. Tính khối lượng HCl than gia phản ứng , khối lượng dd HCl cần dùng cho phản ứng , biết nồng độ CMHCL = 0,5M.
\(a) Zn + 2HCl \to ZnCl_2 + H_2\\ n_{ZnCl_2} = n_{Zn} = \dfrac{6,5}{65} = 0,1(mol)\\ m_{ZnCl_2} = 0,1.136 = 13,6(gam)\\ b) n_{H_2} = n_{Zn} = 0,1(mol) \Rightarrow V_{H_2} = 0,1.22,4 =2 ,24(lít)\\ c) n_{HCl} =2 n_{H_2} = 0,2(mol)\\ \Rightarrow m_{HCl} = 0,2.36,5 = 7,3(gam)\ ; V_{dd\ HCl} = \dfrac{0,2}{0,5} = 0,4(lít)\)
bài 1:Cho 6,5g Zn tác dụng vừa đủ với 200g dd HCl tạo thành dd ZnCl2 và khí H2.
a/Tính khối lượng HCl đã phản ứng?
b/ Tính thể tích khí H2 thoát ra(đktc)?
c/Tính khối lượng dd sau phản ứng?
Bài 2:Cho 4,8g Mg tác dụng vừa đủ với 100g dd HCl tạo thành dd MgCl2 và khí H2.
a/Tính khối lượng HCl đã phản ứng?
b/Tính thể tích khí H2 thoát ra(đktc)?
c/Tính nồng độ phần trăm của dd sau phản ứng?
MỌI NGƯỜI ƠI GIÚP VỚI Ạ!!! làm ơn SOS
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\\
V_{H_2}=0,1.22,4=2,24l\\
m_{\text{dd}}=6,5+200-\left(0,1.2\right)=206,3g\)
bài 2 :
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2 0,2
\(m_{HCl}=0,4.36,5=14,6g\\
V_{H_2}=0,2.22,4=4,48l\\
m\text{dd}=4,8+200-0,4=204,4g\\
C\%=\dfrac{0,2.136}{204,4}.100\%=13,3\%\)
Cho 6,5g Zn tác dụng với 200g dd HCl 17,8%. Sau phản ứng thu được V lít khí Hidro a) Tính khối lượng HCl cần dùng b) tính V c) Tính C% các chất còn lại sau phản ứng
\(a.n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{17,8\%.200}{36,5}=\dfrac{356}{365}\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,1}{1}< \dfrac{\dfrac{356}{365}}{2}\\ \Rightarrow Znhết,HCldư\\ n_{HCl\left(dùng\right)}=0,1.2=0,2\left(mol\right)\\ m_{HCl\left(dùng\right)}=0,2.36,5=7,3\left(g\right)\\ b.n_{H_2}=n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ c.n_{HCl\left(Dư\right)}=\dfrac{356}{365}-0,2=\dfrac{283}{365}\left(mol\right)\\ C\%_{ddZnCl_2}=\dfrac{0,1.136}{6,5+200}.100\approx6,586\%\)
\(C\%_{ddHCl\left(dư\right)}=\dfrac{\dfrac{283}{365}.36,5}{6,5+200}.100\approx13,705\%\)
Cho Zn tác dụng với axit clohiric theo phương trình phản ứng :
Zn + HCl → ZnCl2 + H2
Nếu cho 26g Zn tham gia phản ứng, hãy tính :
a) Thể tích khí H2 thu được ở đktc
b) Khối lượng axit đã dùng ?
\(n_{Zn}=0,4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,4-----0,8--------------------0,4 (mol)
\(V_{H_2}=0,4.22,4=8,96\left(l\right)\)
\(m_{HCl}=0,8.36,5=29,2\left(g\right)\)
Đây nè bạn. Chỗ nào mk làm bạn ko hiểu thì bạn bảo mk nhé!
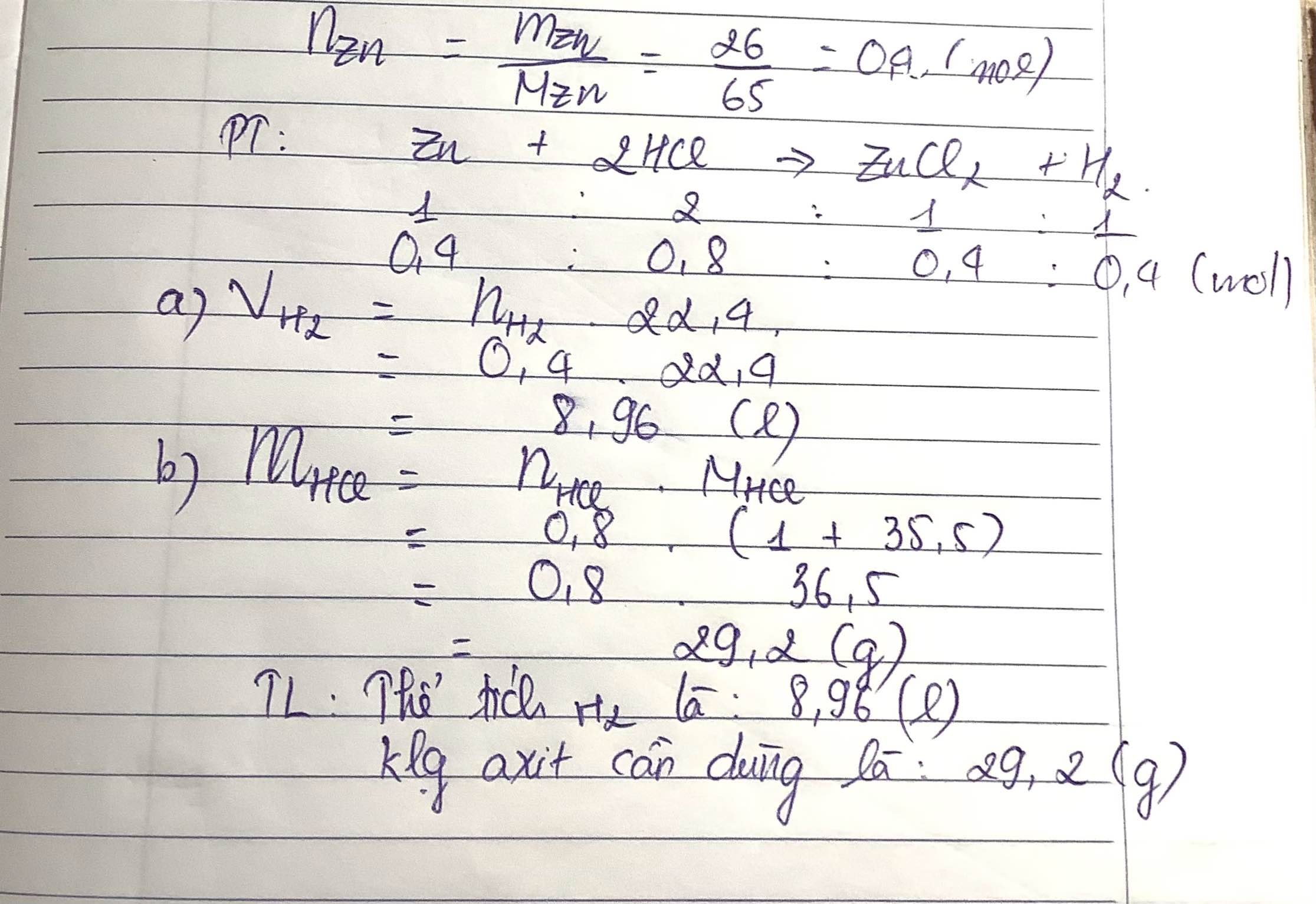
Bài 3: Cho 6,5g kẽm Zn tác dụng với dung dịch HCl 3,65%
(dtkc=24,79)
. a. Viết phương trình hóa học?
b. Tính thể tích khí H2 (đktc) sinh ra sau phản ứng?
c. Tính khối lượng dung dịch HCl cần dùng?
d. Tính khối lượng của muối sinh ra.
e. Tính nồng độ phần trăm của muối.
a,\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,1 0,2 0,1 0,1
b,\(V_{H_2}=0,1.24,79=2,479\left(l\right)\)
c,\(m_{ddHCl}=\dfrac{0,2.36,5.100}{3,65}=200\left(g\right)\)
d,\(m_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
e,mdd sau pứ = 6,5+200-0,1.2 = 206,3 (g)
\(C\%_{ddZnCl_2}=\dfrac{13,6.100\%}{206,3}=6,59\%\)
Bài 3 :
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1 0,1
b) \(n_{H2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
c) \(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(m_{ddHCl}=\dfrac{7,3.100}{3,65}=200\left(g\right)\)
d) \(n_{ZnCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,1.136=13,6\left(g\right)\)
e) \(m_{ddspu}=6,5+200-\left(0,1.2\right)=206,3\left(g\right)\)
\(C_{ZnCl2}=\dfrac{13,6.100}{206,3}=6,6\)0/0
Chúc bạn học tốt
Cho 6,5g kim loại kẽm ( Zn ) tác dụng với đ axit clohiđric ( HCl ) vừa đủ. Hãy tính a/ Thể tích khí hiđro thu được ở ( đktc ) b/ Khối lượng axit clohiđric cần dùng
TTĐ:
\(m_{Zn}=6,5\left(g\right)\)
_______________
\(V_{H_2}=?\left(l\right)\)
\(m_{HCl}=?\left(g\right)\)
Giải
Số mol của 6,5 gam Zn:
\(n_{Zn}=\dfrac{m}{M}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Tỉ lệ: 1 : 2 : 1 : 1
Số mol: 0,1-> 0,2 : 0,2 : 0,2(mol)
a/ thể tích khí hiđro thu được:
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
b/ Khối lượng của 0,2 mol HCl:
\(m_{HCl}=n.M=0,2.36,5=7,3\left(g\right)\)
a)Số mol của Zn là:
\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(PTHH:Zn+2HCl\xrightarrow[]{}ZnCl_2+H_2\)
tỉ lệ :1 2 1 1
số mol :0,1 0,2 0,1 0,1
Thể tích khí hiđro thu được là:
\(V_{H_2}=n_{H_2}.22,4=2,24\left(l\right)\)
b) Khối lượng axit clohiđric cần dùng là:
\(m_{HCl}=n_{HCl}.M_{HCl}=0,2.36,5=7,3\left(g\right)\)
Kẽm tác dụng với axit clohidric theo phương trình: Zn + 2HCl-ZnCl₂ + H₂ Nếu có 6,5g kẽm tham gia phản ứng, con hãy tìm: a/ Thể tích khí H2 thu được ở đktc b/ Khối lượng HCL cần dùng.
\(n_{Zn}=\dfrac{6,5}{65}=0,1(mol)\\ Zn+2HCl\to ZnCl_2+H_2\\ \Rightarrow n_{H_2}=0,1(mol);n_{HCl}=0,2(mol)\\ a,V_{H_2}=0,1.22,4=2,24(l)\\ b,m_{HCl}=0,2.36,5=7,3(g)\)
Cho 6,5g Zn tác dụng hết với dung dịch HCl 10%. Sau phản ứng thu được dụng dịch ZnCl2 và H2.
a/ Tính thể tích H2 thoát ra (đktc).
b/ Tính khối lượng dung dịch HCl tham gia phản ứng.
c/ Tính C% của dung dịch ZnCl2 thu được.
Cho 6,05 g hỗn hợp gồm Zn và Al tác dụng vừa đủ với dd HCl 10% cô cạn dd sau phản ứng thu được 13,15 g muối khan. a/ Tìm thể tích khí hidro thoát ra ở đktc b/ Tìm khối lượng dd HCl đã dùng biết lượng axit dùng dư 20% so với lượng phản ứng
Zn+2HCl→ZnCl2+H2
2Al+6HCl→2AlCl3+3H2
Gọi số mol HCllà x
n H2=\(\dfrac{1}{2}\)n HCl=0,5x
Bảo toàn khối lượng: mkl+mHCl=mmuối+mH2
6,05+36,5x=13,15+0,5x.2
→x=0,2 mol
mHCl=0,2.36,5=7,3 gam
=>m =mddHCl=\(\dfrac{7,3}{10\%}\)=73gam
Cho 42,15 g hỗn hợp Ag và Zn tác dụng vừa đủ với dung dịch HCl 2M thì thu được 3,7185 Lít khí (đkc). 6 a. Tính khối lượng mỗi kim loại trong hỗn hợp b. Tính thể tích dung dịch HCl 2M đã dùng . c. Cho dung dịch sau phản ứng tác dụng với dd AgNO3 dư. Tính khối lượng kết tủa trắng silver chloride thu được? (Zn =65, Ag = 108, Cl = 35,5)
giúp e đi mà :<