Đốt cháy hoàn toàn 11,2lít khí Hiđro ở đktc:
a/ Tính thể tích không khí cần dùng cho quá trình phản ứng trên
b/ Cần bao nhiêu gam kim loại kẽm phản ứng Axit Clohiđric để thu được lượng Hiđro trên
Cho 14 gam kim loại Fe tan hoàn toàn trong dd axit sunfuric (\(H_2SO_4\))
. a/Viết Phương trình phản ứng xảy ra?
b/Tính thể tích khí hido thoát ra (ở đktc)?
c/Tính khối lượng axit sunfuric cần dùng?
giúp mình với
a) nFe= 0,25(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
0,25______0,25______0,25__0,25(mol)
b) V(H2,đktc)=0,25.22,4=5,6(l)
c) mH2SO4= 0,25.98= 24,5(g)
Lời giải "chi tiết"
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)=n_{H_2SO_4}=n_{H_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{H_2SO_4}=0,25\cdot98=24,5\left(g\right)\\V_{H_2}=0,25\cdot22,4=5,6\left(l\right)\end{matrix}\right.\)
a,PTHH:Fe+H2SO4→FeSO4+H2↑
b, Ta có: nFe= \(\dfrac{14}{56}\)=0,25(mol)
Theo pt: nH2=nFe=0,25(mol)
⇒VH2=0,25.22,4=5,6(l)
c, Theo pt: nH2SO4=nFe=0,25(mol)
⇒mH2SO4=0,25.98=24,5(g)
/ Đốt cháy hoàn toàn 19,5g Zn trong khí oxi thu được ZnO.
a/ Viết PTHH. Phản ứng trên thuộc loại phản ứng nào?
b/ Tính khối lượng ZnO tạo thành
c/ Tính thể tích O2 PƯ
\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+\dfrac{1}{2}O_2\rightarrow\left(t^o\right)ZnO\)
1 1/2 1 (mol)
0,3 0,15 0,3 ( mol )
PƯ trên thuộc loại phản ứng hóa hợp
\(m_{ZnO}=n_{ZnO}.M_{ZnO}=0,3.81=24,3g\)
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)
a. \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH : 2Zn + O2 -> 2ZnO ( Phản ứng hóa hợp )
0,3 0,15 0,3
b. \(m_{ZnO}=0,3.81=24,3\left(g\right)\)
c. \(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
Câu 1: Đốt cháy hoàn toàn 6,5 gam Kẽm trong bình oxi dư
a. Tính thể tích oxi đã dùng(đktc)
b. Tính khối lượng sản phẩm tạo thành ?
c. nếu trong bình trên có chứa 0,8 gam khí oxi thì chất nào còn dư sau phản ứng? Tìm khối lượng sản phẩm tạo thành
2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=0,1 mol
nO2=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g
2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=6,5/65=0,1 mol
n O2=0,8/32=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g
Đốt cháy hoàn toàn 5,4 g al trong khí xoi thu đc nhôm axit A, viết pghh xảy ra B, tính thể tích khí xoi cần dùng C để điều chế đc lượng xoi trên cần dùng bao nhiêu cần kmno4
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\a, PTHH:4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ b,n_{O_2}=\dfrac{3}{4}.n_{Al}=\dfrac{3.0,2}{4}=0,15\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,15.22,4=3,36\left(l\right)\\ c,2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ n_{KMnO_4}=2.n_{O_2}=2.0,15=0,3\left(mol\right)\\ \Rightarrow m_{KMnO_4}=158.0,3=47,4\left(g\right)\)
đốt cháy hoàn toàn 13,8 g rượu etilic
a, tính thể tích khí co2 ở đktc
b, tính thể tích ko khí (đktc) cần dùng ở trên. biết oxi chiếm 20% thể tích ko khí
\(n_{C_2H_5OH}=\dfrac{13,8}{46}=0,3mol\)
\(C_2H_5OH+3O_2\rightarrow2CO_2+3H_2O\)
0,3 0,9 0,6 ( mol )
\(V_{CO_2}=0,6.22,4=13,44l\)
\(V_{kk}=\left(0,9.22,4\right).5=100,8l\)
C2H5OH+3O2-to>2CO2+3H2O
0,3------------0,9-----------0,6
n C2H5OH=0,3 mol
=>VCO2=0,6.22,4=13,44l
=>VO2=0,9.22,4.5=100,8l
\(n_{C_2H_5OH}=\dfrac{13,8}{46}=0,3mol\)
\(C_2H_5OH+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
0,3 0,9 0,6
\(V_{CO_2}=0,6\cdot22,4=13,44l\)
\(V_{O_2}=0,9\cdot22,4=20,16l\)
\(V_{kk}=5V_{O_2}=5\cdot20,16=100,8l\)
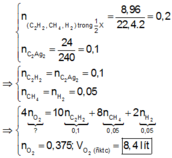
Cho hỗn hợp chất rắn gồm CaC 2 , Al 4 C 3 , Ca vào nước, thu được hỗn hợp X gồm 3 khí, trong đó có hai khí có cùng số mol. Lấy 8,96 lít hỗn hợp X (đktc) chia làm 2 phần bằng nhau. Phần 1 cho vào dung dịch AgNO 3 (dư) trong NH 3 , sau phản ứng hoàn toàn thấy tách ra 24 gam kết tủa. Phần 2 cho qua Ni, đun nóng thu được hỗn hợp khí Y. Thể tích O 2 vừa đủ (đktc) cần dùng để đốt cháy hoàn toàn Y là:
A. 5,6 lít
B. 8,4 lít
C. 8,96 lít
D. 16,8 lít
Đáp án B
Theo giả thiết, bảo toàn nguyên tố C và bảo toàn electron, ta có :
Bài 4. Cho 12g sắt (III) oxit phản ứng với khí Hiđro ta thu đc sắt và nước
a, Tính thể tích khí oxi (ở đktc) cần dùng
b, Tính khối lượng sắt thu đc sau phản ứng
Bài 5. Cho 19,5g Zn tác dụng với dung dịch axit sunfuric loãng thu đc kẽm sunfat và khí hiđro
a, Tính khối lượng kẽm sunfat thu đc sau phản ứng
b, Tính thể tích khí Hiđro thu đc ở (đktc)
Bài 4 câu a đề là thể tích H2 nha bạn
a)\(Fe2O3+3H2-->2Fe+3H2O\)
\(n_{Fe2O3}=\frac{12}{160}=0,075\left(mol\right)\)
\(n_{H2}=3n_{Fe2O3}=0,225\left(mol\right)\)
\(V_{H2}=0,225.22,4=5,04\left(l\right)\)
b)\(n_{Fe}=2n_{Fe2O3}=0,15\left(mol\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
Bài 6
a)\(Zn+H2SO4-->ZnSO4+H2\)
\(n_{Zn}=\frac{19,5}{65}=0,3\left(mol\right)\)
\(n_{ZnSO4}=n_{Zn}=0,3\left(mol\right)\)
\(m_{ZnSO4}=0,3.162=48,3\left(g\right)\)
b)\(n_{H2}=n_{Zn}=0,3\left(mol\right)\)
\(V_{H2}=0,3.22,4=6,72\left(l\right)\)
a)Fe2O3+3H2−−>2Fe+3H2O
0,075-------0,225---0,15 mol
nFe2O3=12/160=0,075(mol)
VH2=0,225.22,4=5,04(l)
b)
mFe=0,15.56=8,4(g)
Bài 6
a)Zn+H2SO4−−>ZnSO4+H2
0,3----------------------0,3---0,3
nZn=19,5/65=0,3(mol)
mZnSO4=0,3.162=48,3(g)
b)
=>VH2=0,3.22,4=6,72(l)
B5, Pthh: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Số mol của 19,5g Zn là:
\(n=\frac{m}{M}=\frac{19,5}{65}=0,3\left(mol\right)\)
KL \(ZnSO_4\) sau phản ứng là:
\(m=n\times M=0,3\times\left(65+32+16\times4\right)=48,3\left(g\right)\)
Thể tích khi \(H_2\)(đktc) là
\(V=n\times22,4=0,3\times22,4=6,72\)
Cho 19,5 gam kẽm tác dụng với axit sunfuric. Hãy:
a) Viết PTHH của phản ứng
b) Tính khối lượng axit sunfuric tham gia phản ứng và thể tích của khí hidro sinh ra (đktc)
c) Cho toàn bộ khí hidro sinh ra ở phản ứng trên khử đồng (2) oxit. Hãy tính khối lượng đồng kim loại thu được
Đốt cháy 5,4 g Aluminium trong bình đựng khí Oxygen tinh khiết, sau phản ứng thu được Aluminium oxide.
a) Viết PTHH. Tính khối lượng Aluminium oxide thu được
b) Để có được lượng oxygen dùng cho phản ứng trên thì cần nhiệt phân bao nhiêu gam KClO3?
\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,2 0,15 0,1
\(m_{Al_2O_3}=0,1\cdot102=10,2g\)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
0,1 0,15
\(m_{KClO_3}=0,1\cdot122,5=12,25g\)
\(PTHH:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(n_{Al}=5,4:27=0,2\left(mol\right)\)
\(\Rightarrow n_{Al_2O_3}=0,2.2:4=0,1\left(mol\right);n_{O_2}=0,2.3:4=0,15\left(mol\right)\)
\(m_{Al_2O_3}=0,1.102=10,2\left(g\right)\)
b)\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(n_{O_2}=0,15\left(mol\right)\)(câu a)
\(\Rightarrow n_{KClO_3}=0,15.2:3=0,1\left(mol\right)\)
\(m_{KClO_3}=0,1.123,5=12,35\left(g\right)\)