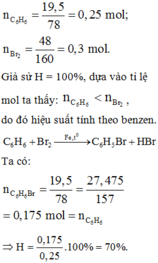Cho 15,6g benzen tác dụng với Brom thu được 14,8g brombenzen. tính hiệu suất của quá trình phản ứng

Những câu hỏi liên quan
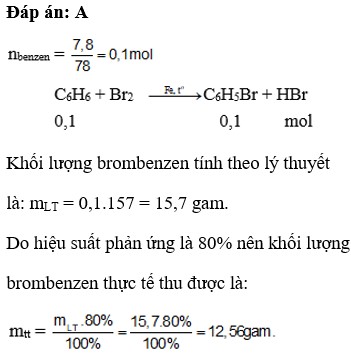
Cho brom phản ứng với benzen tạo ra brombenzen (bột sắt làm xúc tác). Tính khối lượng benzen cần dùng để điều chế 15,7 gam brombenzen. Biết hiệu suất của quá trình phản ứng là 80%.
A. 9,75 gam.
B. 6,24 gam.
C. 7,80 gam.
D. 10,53 gam
Cho 15,6g benzen phản ứng hoàn toàn với brom lỏng có bột sắt làm xúc tác. Sau phản ứng thu được 25,4g brombenzen. Tính hiệu suất của phản ứng.
C6H6 + Br2 --(Fe, nhiệt)--> C6H5Br + HBr
nC6H6 = 15,6\78 = 0,2 mol
nC6H5Br (lý thuyết) = 0,2 (mol)
mC6H5Br (lý thuyết) = 0,2.157 = 31,4 (g)
H = 25,4.100\31,4=80,89%
Cho 7,8 gam benzen phản ứng với brom dư (có bột sắt xúc tác) hiệu suất phản ứng là 80%. Khối lượng brombenzen thu được là
A. 12,56 gam
B. 15,7 gam
C. 19,625 gam
D. 23,8 gam
Cho 19,5 gam benzen tác dụng với 48 gam brom (lỏng), có bột sắt làm xúc tác, thu được 27,475 gam brom benzen. Hiệu suất của phản ứng brom hóa benzen trên là A. 40% B. 50% C. 60% D. 70%
Đọc tiếp
Cho 19,5 gam benzen tác dụng với 48 gam brom (lỏng), có bột sắt làm xúc tác, thu được 27,475 gam brom benzen. Hiệu suất của phản ứng brom hóa benzen trên là
A. 40%
B. 50%
C. 60%
D. 70%
Cho 19,5 gam benzen tác dụng với 48 gam brom (lỏng), có bột sắt làm chất xúc tác, thu được 27,475 gam brom benzen. Hiệu suất của phản ứng brom hóa benzen trên bằng:
A. 40%
B. 50%
C. 60%
D. 70%
B33: Biết rằng benzen cũng có phản ứng thế với Clo như với Brom. Cho clo dư tác dụng với 78 g Benzen có mặt bột sắt thu được 78 g clobenzen. Tính hiệu suất của phản ứng?
\(n_{C_6H_5Cl}=\dfrac{78}{112,5}=\dfrac{52}{75}\left(mol\right)\)
\(n_{C_6H_6}=\dfrac{78}{78}=1\left(mol\right)\)
PTHH:
\(C_6H_6+Cl_2\xrightarrow[t^o]{Fe}C_6H_5Cl\)
1------------------>1
\(\Rightarrow H=\dfrac{\dfrac{52}{75}}{1}.100\%=69,33\%\)
Đúng 1
Bình luận (0)
cho benzen tác dụng với brom có xúc tác bột sắt , thu được 3,925 g brombenzen. tính khối lượng các chất thâm gia phản ứng, biết hiệu suất của phản ứng là 75 phần trăm
nC6H5Br=\(\frac{3,925}{6.12+5+80}\)=0,025(mol)
PTHH: C6H6+Br2 \(\xrightarrow[t^o]{Fe}\) C6H5Br + HCl
(mol) 0,025 0,025 0,025
mC6H6=\(\frac{0,025.\left(12x6+6\right)}{75\%}\)=2,6 (g)
mBr2=\(\frac{0,025.160}{75\%}\)=5,3(g)
Đúng 0
Bình luận (0)
hãy tính lượng brombenzen thu được khi cho 23,4g benzen tác dụng với brom dư khi có mặt bột săt và đun nóng. biết hiệu suất phản ứng là 90%
nC6H6 = 0,3 mol
C6H6 + Br2 → C6H5Br + HBr
0,3........................0,3
⇒ mC6H5Br = 0,3.157.\(\dfrac{90}{100}\) = 42,39 (g)
Đúng 0
Bình luận (0)
Khi có mặt bột sắt, benzen phản ứng với clo tương tự như phản ứng với brom. Hãy tính lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng với clo dư khi có mặt bột Fe và đun nóng. Biết hiệu suất phản ứng đạt 80%.
Phương trình hoá học của phản ứng giữa benzen và clo
C 6 H 6 + Cl 2 → t ° C 6 H 5 Cl + HCl
Theo phương trình hoá học : số mol C 6 H 6 = số mol C 6 H 5 Cl
Vì hiệu suất 80% và clo dư nên số mol clobenzen thu được là :
n C 6 H 5 Cl = 15,6/78 x 80/100 = 0,16mol
=> m C 6 H 5 Cl = 0,16 x 112,5 = 18g
Đúng 0
Bình luận (0)