Trộn hỗn hợp khí hidro và oxi theo tỉ lệ khối lượng 3/16 rồi nạp vào bình khí có dung tích thực 4,48l (đktc). Bật tia lửa điện để phản ứng hóa hợp xảy ra hoàn toàn. Tính khối lượng từng chất có trong bình sau phản ứng
Giúp mình với![]()
Trộn hỗn hợp khí A gồm 3 hidrocacbon với hỗn hợp khí B gồm khí oxi và ozon theo tỉ lệ thể tích VA:VB = 3 : 6,4. Bật tia lửa điện để đốt cháy hoàn toàn thì hỗn hợp khí sau phản ứng chỉ gồm CO2 và H2O có VCO2:VH2O = 2,6:2,4. Tính dA/H2 biết dB/H2 = 19?
A. 6
B. 12
C. 8
D. 10
Đáp án B
Từ dB/H2 = 19 tính được nO2 : nO3 = 5 : 3
Giả sử nA =3; nB = 6,4 → nO2 = 4; nO3 = 2,4; → nO = 4.2+2,4.3=15,2
Đặt CTC 3 hidrocacbon là CxHy
CxHy + (2x+y/2)O → xCO2 + y/2H2O
Ta có 2x/y = 2,6/2,4 và 2x + y/2 = 15,2/3 → x = 26/15; y = 3,2
MA = 12.26/15 + 3,2 = 24; dA/H2 =12
1. Trong bình đốt khí người ta dung tia lửa điện để đốt một hỗn hợp gồm60 cm3 gồm khí hiđro và khí oxi.
a) Sau phản ứng còn thừa khí nào không? Thừa bao nhiêu cm3?
b) Tính thể tích và khối lượng hơi nước thu được? (Biết các thể tích khí và hơi đo ở đktc).
2. Để hòa tan hoàn toàn 4 gam hỗn hợp A gồm oxit của Đồng (II) và Sắt (III) cần vừa đủ 25,55 gam dung dịch HCl 20%.
a) Tính khối lượng từng chất trong hỗn hợp A.
b) Nếu đem hỗn hợp A nung nóng trong ống sứ rồi dẫn khí CO đi qua, trong điều kiện thí nghiệm thấy cứ 4 phân tử chất rắn mỗi loại tham gia phản ứng thì có 1 phân tử không tham gia phản ứng. Xác định thành phần và khối lượng chất rắn thu được sau phản ứng trong ống sứ?
Nung m gam hỗn hợp A gồm KMnO4 và KClO3 thu được chất rắn B và khí O2. Lúc đó KClO3 phân hủy hoàn toàn, còn KMnO4 phân hủy không hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn lượng O2 thu được ở trên với không khí (có phần trăm thể tích: 20% O2; 80% N2) theo tỉ lệ thể tích tương ứng là 1:3 tạo thành hỗn hợp khí C. Cho toàn bộ khí C vào bình chứa 0,528 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp khí D gồm 3 khí trong đó O2 chiếm 17,083% về thể tích.
a) Tính phần trăm khối lượng mỗi chất có trong A.
b) Thêm 74,5 gam KCl vào chất rắn B được hỗn hợp E. Cho E vào dung dịch H2SO4 loãng dư, đun nóng nhẹ cho đến phản ứng hoàn toàn. Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn.
Tiến hành thí nghiệm sau:
– Thí nghiệm 1: cho 1,74 gam MnO2 tác dụng với HCl đặc, dư, đun nóng thu được khí A màu vàng lục.
– Thí nghiệm 2: cho một lượng sắt vào dung dịch H2SO4 loãng đến khi khối lượng dung dịch tăng 167,4 gam thì thu được một lượng khí B.
– Thí nghiệm 3: thêm 3 gam MnO2 vào 197 gam hỗn hợp KCl và KClO3 thu được hỗn hợp X. Trộn kĩ và đun nóng hỗn hợp X đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn nặng 152 gam và một lượng khí D.
– Thí nghiệm 4: Nạp toàn bộ lượng khí A, khí B và khí D thu được ở các thí nghiệm trên vào một bình kín, nâng nhiệt độ cao để thực hiện hoàn toàn các phản ứng rồi đưa nhiệt độ về 250C thu được dung dịch Y chỉ chứa một chất tan duy nhất.
Viết các phương trình hóa học xảy ra và tính nồng độ % của chất tan có trong dung dịch Y
1/ Hỗn hợp khí A gồm N2 và H2 có tỉ khối đối với hidro là 8.
a) Tính % thể tích mỗi khí trong hỗn hợp.
b) Người ta cho 11,2 lít A vào bình thép rồi bật tia lửa điện để thực hiện phản ứng giữa N2 và H2, tạo khí NH3. Sau một thời gian, hỗn hợp thu được có tỉ khối đối với hiđro là 6,5. Tính hiệu suất của phản ứng trên.
Một bình cầu dung tích 448 ml được nạp oxi rồi cân. Phóng điện để ozon hoá, sau đó lại nạp oxi rồi cân. Khối lượng trong 2 trường hợp chênh lộch nhau 0,03 gam.
Tính phần trăm về khối lượng của ozon trong hỗn hợp sau phản ứng. Biết các thể tích khí nạp vào bình đều đo ở đktc.
448 ml ở đktc là 0,02 mol.
Số mol ozon có trong oxi đã được ozon hoá : 0,03/16 = 0,001875 (mol) hay 0,09 (g).
Số mol oxi có trong bình : 0,02 - 0,001875 = 0,018125 (mol) hay 0,58 g.
Khối lượng của hỗn hợp : 0,09 + 0,58 = 0,67 (g).
Phẩn trăm khối lượng cua ozon trong hỗn hợp : 0,09 x 100/0,67 = 13,43%
Một hỗn hợp gồm amin đơn chức X và O2 theo tỉ lệ mol 2:9. Bật tia lửa điện để phản ứng đốt cháy xảy ra hoàn toàn, sau đó dẫn sản phẩm cháy qua dung dịch NaOH đặc dư thu được hỗn hợp khí Y có tỉ khối so với H2 là 15,2. X là:
A. C3H9N.
B. CH5N.
C.C2H5N.
D. C2H7N.
Đáp án D
Phân tích: Nhìn vào đáp án thấy có 3 đáp án đều là amin no, 1 amin không no. Vì vậy trong giải nhanh ta hoàn toàn có quyền giả sử đó là amin no để tìm. Nếu không có trường hợp nào thỏa mãn thì amin không no ở đáp án C sẽ là chính xác.
Giả sử amin X có công thức: CnH2n+3N và giả sử có 1 mol X tham gia phản ứng (không mất tính tổng quát theo phưong pháp tự chọn lượng chất). Phưong trình cháy:
![]()
Khí thu được sau khi cho phản cháy đi qua NaOH đặc dư chứa:
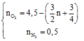
Mặt khác theo khối lượng mol trung bình của hỗn hợp khí. Sử dụng phương pháp đường chéo dễ dàng suy ra 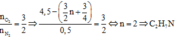
Hỗn hợp khí X gồm hidro và một hidrocacbon. Nung nóng 24,64 lít hỗn hợp X (đktc), có Ni xúc tác, để phản ứng xảy ra hoàn toàn, biết rằng có hidrocacbon dư. Sau phản ứng thu được 20,4 gam hỗn hợp khí Y. Tỉ khối hỗn hợp so với hidro bằng 17. Khối lượng hidro có trong hỗn hợp X là?
A. 3 g
B. 2 g
C. 1 g
D. 0,5 g
Đây là một ví dụ rất đơn giản nhưng đặc trưng về quan hệ số mol trong phản ứng cộng hidro của hidrocacbon chưa no
Dễ tính đươc
![]()
Trong phản ứng hidro hóa hidrocacbon chưa no thì số mol khí giảm chính bằng số mol hidro phản ứng suy ra ![]()
Mặt khác đề cho hidrocacbon dư, phản ứng hoàn toàn nên
![]()
suy ra ![]()
Hỗn hợp khí B có thể tích 22,4 lít (đktc) gồm H2 và O2. Tỉ khối của B so với H2 bằng 5,5. Đốt nóng hỗn hợp khí B để phản ứng xảy ra hoàn toàn. Tính khối lượng chất thu được sau phản ứng
Gọi số mol H2, O2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{22,4}{22,4}=1\\M_B=\dfrac{2a+32b}{a+b}=5,5.2=11\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,7 (mol); b = 0,3 (mol)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,7}{2}>\dfrac{0,3}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
0,6<--0,3------->0,6
=> \(\left\{{}\begin{matrix}m_{H_2O}=0,6.18=10,8\left(g\right)\\m_{H_2\left(dư\right)}=\left(0,7-0,6\right).2=0,2\left(g\right)\end{matrix}\right.\)