Hỗn hợp X gồm 8,1 gam Al và 10,8 gam FeO. Hòa tan hết X trong dung dịch axit sunfuric loãng dư, sau khi kết thúc phản ứng thu được V lít khí (đktc). Giá trị của V là:
A. 10,08.
B. 6,72.
C. 11,2.
D. 22,4.
Hòa tan 30,5 gam hỗn hợp X gồm Al và Fe cần dùng 400 gam dung dịch axit sunfuric loãng nồng độ 20,825% vừa đủ. Sau khi phản ứng kết thúc thu được dung dịch A và khí B (đktc). a. Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp X? b. Tính khối lượng muối khan thu được. c. Lượng khí Hidro ở trên vừa đủ 49,3 gam oxit của kim loại M. Xác định công thức hóa học của oxit đó?
Hòa tan hết hỗn hợp gồm Mg, Al, và Al(NO3) trong dịch chứa NaHSO4 và 0,06 mol NaNO3 kết thúc phản ứng thu được dung dịch X chứa các muối trung hòa có khối lượng 115,28 gam và V lít (đktc) hỗn hợp khí T gồm N2O và H2 ( tỉ lệ 1:1). Cho dung dịch NaOH dư vào X thấy lượng dư NaOH phản ứng là 36,8 gam, đồng thời thu được 13,92 gam kết tura. Giá trị của V là:
A. 1,344
B. 1,792
C. 2,24
D. 2,016
Đáp án B
Đặt nN2O = nH2 = a (mol)
nNH4+ = b (mol)
=> nH+ = 10nN2O + 2nH2 + 10 nNH4+ = 12a + 10b
=> nNa+ = 12a + 10b + 0,06 ; nSO42- = 12a + 10b
nMg = nMg(OH)2 = 0,24 (mol)
Bảo toàn electron: 2nMg + 3nAl = 8nN2O + 2nH2 + 8nNH4+
=> nAl = (10a + 8b – 0,48)/3
BTNT N => 3nAl(NO3)3 + nNaNO3 = 2n N2O + nNH4+
=> nAl(NO3)3 = (2a + b – 0,06)/3
BTNT Al => nAl3+ trong X = nAl + nAl(NO3) = 4a + 3b – 0,18
Khối lượng muối trong X( Na+ ; Al3+; Mg2+; NH4+ ; SO42- ):
23( 12a + 10b + 0,06) + 27 ( 4a + 3b – 0,18) + 0,24.24 + 18b + 96 ( 12a + 10b) = 115, 28 (1)
nNaOH = 4nAl3+ + 2nMg2+ + nNH4+
=> 0,92 = 4 ( 4a + 3b – 0,18 ) + 2.024 + b (2)
Từ (1) và (2) => a = b = 0,04 (mol)
=> nT = 2a = 0,08 (mol)
=> V= 1,792 (lít)
Hoà tan hoàn toàn 11 gam hỗn hợp X gồm Al và Fe bằng dung dịch axit sunfuric loãng dư. Sau khi phản ứng phản ứng kết thúc thu được 8,96 lít khí (đktc).
a) Tính thành phần phần trăm về khối lượng mỗi kim loại trong hỗn hợp X.
b) Tính khối lượng muối khan thu được.
c) Lượng khí hiđro ở trên khử vừa đủ 23,2 gam oxit của kim loại M. Xác định CTHH của oxit đó.
Gọi x,y lần lượt là số mol của Al, Fe
nH2 = \(\dfrac{8,96}{22,4}\)=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt:
{27x+56y=11
1,5x+y=0,4
⇔x=0,2, y=0,1
% mAl = \(\dfrac{0,2.27}{11}\).100%=49,1%
% mFe = \(\dfrac{0,1.56}{11}\).100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
\(\dfrac{0,4}{y}\)<-------0,4
Ta có: 232,2=\(\dfrac{0,4}{y}\)(56x+16y)
⇔23,2=\(\dfrac{22,4x}{y}\)+6,4
⇔\(\dfrac{22,4x}{y}\)=16,8
⇔22,4x=16,8y
⇔x:y=3:4
Vậy CTHH của oxit: Fe3O4
b) Xác định công thức phân tử của X, biết tỉ khối của X đối với H2 bằng 16.
Câu 6: Hòa tan hoàn toàn 11 gam hỗn hợp X gồm Al và Fe bằng dung dịch axit sunfuric loãng dư. Sau khi phản ứng kết thúc thu được 8,96 lít khí (đktc)
a) Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp X?
b) Tính khối lượng muối khan thu được?
c) Lượng khí Hiđro ở trên khử vừa đủ 23,2 gam oxit của kim loại M. Xác định công thức hóa học của oxit đó?
Câu 7: Hòa tan hết 4,8 gam hỗn hợp A gồm MgO, Fe2O3, CuO cần vừa đủ một lượng dung dịch chứa 5,84 gam HCl. Mặt khác, dẫn khí H2 dư qua 0,09 mol hỗn hợp A nung nóng thì sau phản ứng thu được 1,62 gam nước. Tính khối lượng mỗi chất trong 4,8 gam hỗn hợp A.
câu 7
MgO + 2HCl -> MgCl2 + H2O
x 2x
Fe2O3 + 6HCl -> 2FeCl3 + 3H2O
y 6y
CuO + 2HCl -> CuCl2 + H2O
z 2z
A--H2 dư----> MgO + H2O
Fe
Cu
Fe2O3 + 3H2 -> 2Fe + 3H2O
ky
CuO + H2 -> Cu + H2O
kz
nH2O=\(\dfrac{16,2}{18}\)0,09mol
Gọi nMgO=x, nFe2O3=y, nCuO=z (trong 4,8g hh A)
nMgO=kx, nFe2O3=ky, nCuO=kz (trong 0,09mol A)
=> kx+ky+kz =4,8
3ky + kz= 0,09=> 2ky = kx =>\(\left\{{}\begin{matrix}2y=x\\40x+160y+80z=4,8\\2x+6y+2z=\dfrac{5,84}{36,5}=0,16\end{matrix}\right.\)
+ x=0,02
=> mMgO= 0,8g
+y=0,01
=> mFe2O3=1,6g
+ z=0,03
=> mCuO=2,4g
Gọi x,y lần lượt là số mol của Al, Fe
nH2 = 0,2×2711.100%=49,1%0,2×2711.100%=49,1%
% mFe = 0,4y0,4y<-------0,4
Ta có: ⇔23,2=22,4xy+6,4⇔23,2=22,4xy+6,4
⇔xy=16,822,4=34⇔xy=16,822,4=34
Vậy CTHH của oxit: Fe3O4
Hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3. Đem hòa tan 14,4 gam hỗn hợp X trong lượng dư dung dịch H2SO4 đậm đặc, nóng, có 6,72 lít khí SO2 duy nhất thoát ra (đktc). Sau khi kết thúc phản ứng, đem cô cạn dung dịch, thu được m gam muối khan. Trị số của m là:
A. 48.
B. 44.
C. 40.
D. 5
Đáp án A
Quy hỗn hợp X về dạng Fe và O.
=> mX = 56nFe + 16nO = 14,4g (1)
- Khi X + H2SO4: Bảo toàn e: 3nFe = 2nO + 2nSO2
=> 3nFe – 2nO = 2.6,72: 22,4 = 0,6 mol (2)
Từ (1,2) => nFe = 0,24; nO = 0,06 mol
Vậy muối trong dung dịch sau phản ứng sẽ là: 0,12 mol Fe2(SO4)3
=> mFe2(SO4)3 = 0,12.400 = 48g
Hòa tan hết hỗn hợp gồm Mg, Al và Al(NO3)3 trong dung dịch chứa NaHSO4 và 0,06 mol NaNO3 kết thúc phản ứng thu được dung dịch X chứa các muối trung hòa có khối lượng 115,28 gam và V lít (đktc) hỗn hợp khí T gồm N2O và H2 (tỉ lệ 1 : 1). Cho dung dịch NaOH dư vào X, lượng NaOH phản ứng là 0,92 mol và thu được 13,92 gam kết tủa. Giá trị của V là
A. 1,344
B. 1,792
C. 2,24
D. 2,016
Hòa tan hết hỗn hợp gồm Mg, Al và Al(NO3)3 trong dung dịch chứa NaHSO4 và 0,06 mol NaNO3. Kết thúc phản ứng thu được dung dịch X chứa các muối trung hòa có khối lượng 115,28 gam và V lít (đktc) hỗn hợp khí T gồm N2O và H2 (tỉ lệ 1:1). Cho dung dịch NaOH dư và X thấy lượng NaOH phản ứng là 36,8 gam, đồng thời thu được 13,92 gam kết tủa. Giá trị của V là
A. 2,240.
B. 2,016.
C. 1,344.
D. 1,792.
Chọn D.
Hỗn hợp Mg, Al và Al(NO)3 tác dụng với dung dịch chứa NaHSO4 (x mol) và 0,06 mol NaNO3.
Dung dịch X gồm
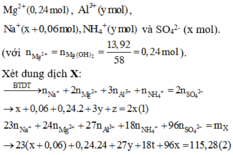
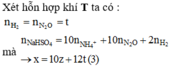
Xét dung dịch thu được sau khi cho X tác dụng với dung dịch chứa 0,92 mol NaOH, ta có:
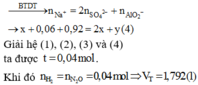
Hòa tan hết hỗn hợp gồm Mg, Al và Al(NO3)3 trong dung dịch chứa NaHSO4 và 0,06 mol NaNO3 kết thúc phản ứng thu được dung dịch X chứa các muối trung hòa có khối lượng 115,28 gam và V lít (đktc) hỗn hợp khí T gồm N2O và H2 (tỉ lệ 1:1). Cho dung dịch NaOH dư và X thấy lượng NaOH phản ứng là 36,8 gam, đồng thời thu được 13,92 gam kết tủa. Giá trị của V là:
A. 1,344
B. 2,24
C. 1,792
D. 2,016
Đáp án C
Gọi số mol N2O và H2 là a mol, NH4+ có thể tạo ra là b mol.
Bảo toàn H+:

Cho m gam hỗn hợp X gồm Fe, FeO, Fe2O3 có tỉ lệ khối lượng tương ứng là 7 : 18 : 40. Hỗn hợp X tan vừa hết trong 500 ml dung dịch H2SO4 loãng 0,68M thu được dung dịch B và thoát ra V lít khí H2 (đktc). Cho dung dịch B tác dụng NaOH dư, lọc bỏ kết tủa nung trong không khí thu được 22,4 gam chất rắn. Giá trị của V là
A. 2,24
B. 0,448
C. 1,12
D. 0,896