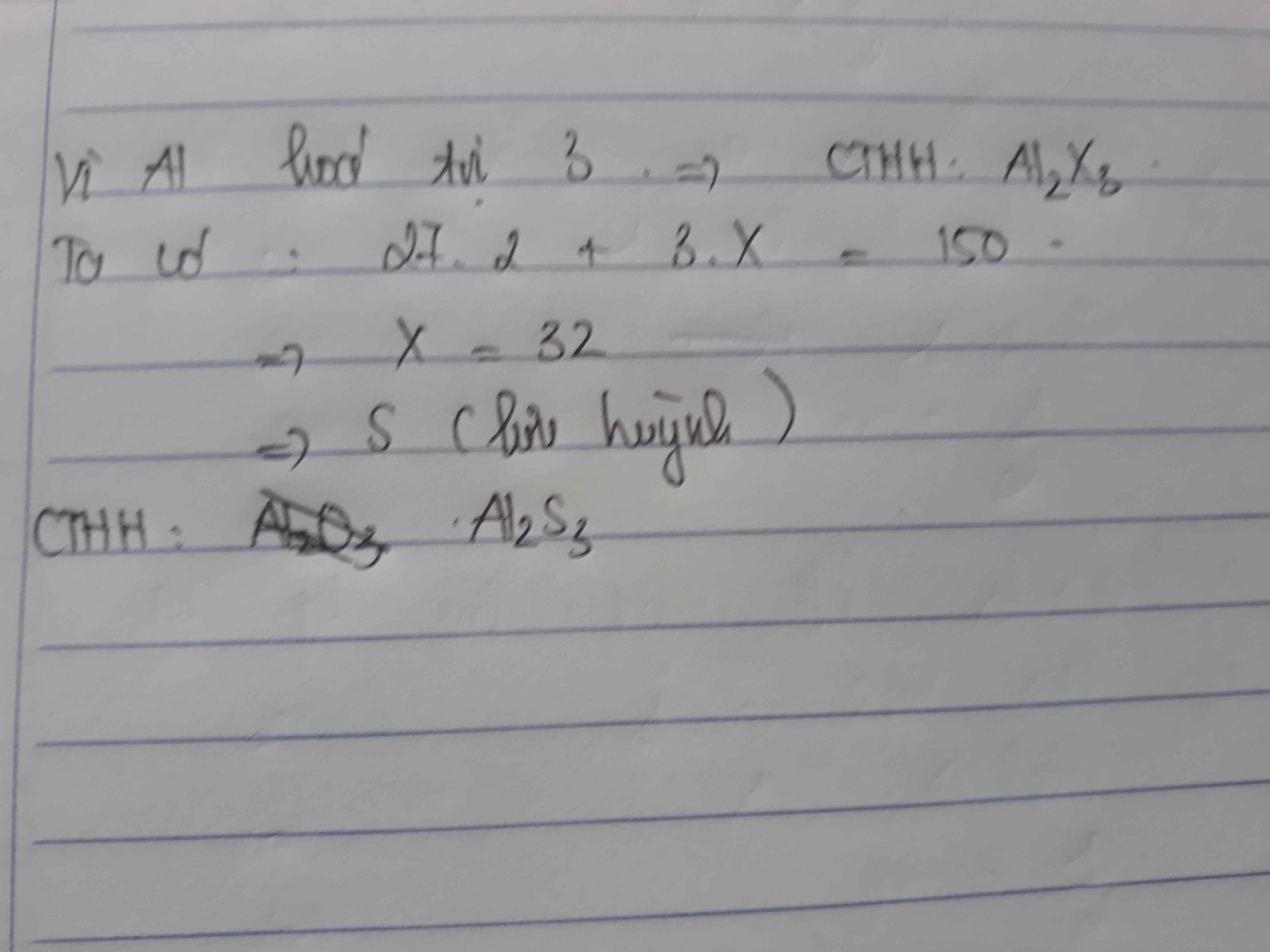mọt nguyên tố X có thể tạo thành với Al hợp chất kiểu AlaXb : một phân tử gồm 5 nguyên tử ,khối lượng phân tử là 150đvC .xác đinh x ,ghi CTHH của hợp chất

Những câu hỏi liên quan
nguyên tố X có thể tạo thành với Al hợp chất kiểu AlaXb mỗi phân tử gồm 5 nguyên tử, khối lượng phân tử 150. Xác định X
1 nguyên tố X có thể tạo thành với Al hợp chất AlaXb ; một phân tử gồm 5 nguyên tử ,khối lượng của phân tử là150 đvC
Al luôn hóa trị 3, các NTHH có hóa trị từ 1->7
+ TH1: X(I)=> có 4 nguyên tử (loại)
+TH2:X(II)=> có 5 nguyên tử(chọn)
+TH3:X(III)=>có 2 nguyên tử (loại)
+TH4:X(IV)=>có 7 nguyên tử(loại)
+TH5:X(V)=> có 8 nguyên tử (loại)
+TH6:X(VI)=> có 3 nguyên tử (loại)
+TH7LX(VII)=>có 10 nguyên tử(loại)
=> Al2X3
ta có:
150=2.27+3.X=54+3X
=>X=32=>X là S
Đúng 0
Bình luận (0)
nguyên tố R phản ứng với lưu huỳnh tạo thành hợp chất RaSb : một phân tử có 5 nguyên tử ,khối lượng phân tử là 150đvC .xác đinh x
Theo đề ta có a+b = 5
Lưu huỳnh có 3 hoá trị II, IV và VI
Nếu S(VI) => a + b > 5 (loại)
Nếu S(IV)
=> công thức hoá học có dạng R4S
Theo cách tính PTK ta có:
4MR + 32 = 150
=> MR = 29,5 (ko có)
Vậy S(II)
=> công thức hoá học có dạng R2S3
Theo cách tính PTK ta có:
2MR + 32.3 = 150
=> MR = 27 (Al)
Vậy công thức hoá học hợp chất là Al2S3
Đúng 0
Bình luận (0)
Nguyên tố X có thể tạo thành với Al hợp chất kiểu AlaXb,mỗi phân tử gồm 5 nguyên tử,phân tử khối 150.Hỏi X là nguyên tố gì?
Trả lời
Ta thấy:
a + b = 5
Đặt trường hợp thôi
1. Với a = 1 => b = 4 => Mx = 30.75
2. Với a = 2 => b = 3 => Mx = 32
3. Với a = 3 => b = 2 => Mx = 13.8
4. Với a = 4 => b = 1 => Mx = 42.
Trong 4 trường hợp thì trường hợp 2 có M = 32 là của Lưu huỳnh (S)
=> Hợp chất có công thức Al2S3.
Đúng 0
Bình luận (0)
Nguyên tố X có thể tạo thành với Al hợp chất kiểu \(Al_aX_b\) mỗi phân tử gồm 5 nguyên tử , phân tử khối 150. Hỏi X là nguyên tố gì ?
Công thức hh dạng AlaXb mà 1 phân tử có 5 nguyên tử
Ta có:
Al hóa trị 3 nên tối đa 2 nguyên tử Al trong AlaXb
Theo đề bài ta có:
27 . 2 + 3 . x = 150
=> x = 32 = S(lưu huỳnh)
Cthh là Al2S3
Đúng 0
Bình luận (0)
Một hợp chất có phân tử gồm 2 nguyên tử nguyên tố X liên kết với 3 nguyên tử O và nặng hơn phân tử hidro 76 lần. a. Tính phân tử khối hợp chất. b. Tìm nguyên tố X và viết CTHH của hợp chất. c. Tính thành phần phần trăm theo khối lượng của X trong hợp chất. Biết: O =16, H = 1, Al =27, Cr = 52, Cu =64
a)Gọi hợp chất cần tìm là \(X_2O_3\)
Theo bài ta có: \(PTK_{X_2O_3}=76M_{H_2}=76\cdot2=152\left(đvC\right)\)
b)Mà \(2M_X+3M_O=152\Rightarrow M_X=\dfrac{152-3\cdot16}{2}=52\left(đvC\right)\)
X là nguyên tố Crom(Cr).
Vậy CTHH là \(Cr_2O_3\).
c)\(\%X=\dfrac{2\cdot52}{2\cdot52+3\cdot16}\cdot100\%=68,42\%\)
Đúng 0
Bình luận (0)
Một hợp chất A có phân tử gồm 2 nguyên tử nguyên tố Kali liên kết với 1 nguyên tử nguyên tố X . Biết phân tử hợp chất A nặng hơn và bằng 47 lần phân tử Hidro
a/ Xác định và công thức tổng quát của hợp chất A
b/ Phân tử khối của hợp chất A , CTHH A
c/ Nguyên tử khối của X , tên , KHHH X
a) Công thức tồng quát của hợp chất A : K2X
b) Ta có : MA=47MH2
=> MA=47.2=94
c) Ta có : 39.2 + X=94
=> X= 16
=> X là Oxi (O)
Đúng 3
Bình luận (1)
$a/CTTQ : K_2X$
`b)PTK=2.47=94`
`c)2.39+X=94`
`=>78+X=94`
`=>X=16đvC`
`->X:`$Oxi(O)$
Đúng 0
Bình luận (0)
Bài 5: Hợp chất A có phân tử gồm 1 nguyên tử của nguyên tố X kết hợp với 2 nguyên tử O. Biết phân tử hợp chất A nặng hơn phân tử khí oxi là 1,375 lần. Xác định CTHH của hợp chất A.
biết \(M_{O_2}=2.16=32\left(đvC\right)\)
vậy \(M_A=32.1,375=44\left(đvC\right)\)
\(1X+2O=44\)
\(X+2.16=44\)
\(X+32=44\)
\(X=44-32=12\left(đvC\right)\)
\(\rightarrow X\) là \(C\left(Cacbon\right)\)
\(\rightarrow CTHH:CO_2\)
Đúng 4
Bình luận (0)
Hai nguyên tử R kết hợp với 1 nguyên tử oxi tạo ra phân tử X. Trong phân tử X, nguyên tố oxi chiếm 25,8% về khối lượng. Xác định CTHH X và vẽ CTCT của hợp chất
X có dạng R2O.
Có: Nguyên tử oxi chiếm 25,8% khối lượng.
\(\Rightarrow\dfrac{16}{2M_R+16}=0,258\Rightarrow M_R=23\left(g/mol\right)\)
→ X là Na.
CTHH: Na2O
CTCT: Na - O - Na.
Đúng 2
Bình luận (0)