1) Cho 10,4 gam hỗn hợp Mg và MgO tác dụng vừa đủ với 300ml dung dịch H2SO4 1M
Tính % Khố lượng mỗi hỗn hợp và H2 tạo ra ( đktc)
Cho 10,4g hỗn hợp Mg và MgO tác dụng vừa đủ với 300ml dung dịch H2So4 tạo ra 2,24 lít khí H2 (đktc)
Tính % mỗi kim loại và C m của dung dịch axit
nH2 = 2,24 : 22,4 = 0,1 mol
gọi x , y lần lượt là số mol Mg và MgO
PTHH : Mg + H2SO4 → MgSO4 + H2
0,1 mol 0,1 mol 0,1 mol
=> mMg = 0,1 . 24 = 2,4 g
%mMg = \(\frac{2,4.100\%}{10,4}=23,08\text{%}\)
Ta có : mhh = mMg + mMgO
=> mMgO = 10,4 - 2,4 = 8g
=> nMgO = 8 : 40 = 0,2 mol
%mMgO = \(\frac{8.100\%}{10,4}=76,92\%\)
MgO + H2SO4 → MgSO4 + H2O
0,2 mol 0,2 mol
Số mol H2SO4 là : nH2SO4 = 0,1 + 0,2 = 0,3 mol
Nồng độ mol dd H2SO4 là
CM H2SO4 = \(\frac{0,3}{0,3}=1M\)
nH2 = 2,24 : 22,4 = 0,1 mol
PTHH : Mg + H2SO4 → MgSO4 + H2
0,1 mol 0,1 mol 0,1 mol
=> mMg = 0,1 . 24 = 2,4 g
%mMg = 2,4.100%10,4=23,08%2,4.100%10,4=23,08%
Ta có : mhh = mMg + mMgO
=> mMgO = 10,4 - 2,4 = 8g
=> nMgO = 8 : 40 = 0,2 mol
%mMgO = 8.100%10,4=76,92%8.100%10,4=76,92%
MgO + H2SO4 → MgSO4 + H2O
0,2 mol 0,2 mol
Số mol H2SO4 là : nH2SO4 = 0,1 + 0,2 = 0,3 mol
Nồng độ mol dd H2SO4 là
CM H2SO4 = 0,3.0,3=1M
#Không có gọi x,y nảy viết nhầm
Câu 1: Cho 2,58 gam hỗn hợp Mg, Al tác dụng vừa đủ với V dung dịch H2SO4 0,5M loãng thu được 2,91362 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị V
Câu 2: Cho 4,96 gam hỗn hợp Fe, Mg tác dụng vừa đủ với 200 gam dung dịch H2SO4 loãng a% thu được 3,136 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị a
Câu 3: Cho 3,94 gam hỗn hợp Ba, Mg tác dụng vừa đủ với 100ml dung dịch H2SO4 xM loãng thu được 1,568 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị x
Câu 1:
\(n_{H_2}=\dfrac{2.91362}{22.4}=0.13mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2b 3b b 3b
Ta có: \(\left\{{}\begin{matrix}24a+54b=2.58\\a+3b=0.13\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.04\\b=0.03\end{matrix}\right.\)
\(m_{Mg}=0.04\times24=0.96g\)
\(m_{Al}=0.03\times2\times27=1.62g\)
\(V_{H_2SO_4}=\dfrac{0.04+3\times0.03}{0.5}=0.26l\)
Câu 2:
\(n_{H_2}=\dfrac{3.136}{22.4}=0.14mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}24a+56b=4.96\\a+b=0.14\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.09\\b=0.05\end{matrix}\right.\)
\(m_{Mg}=0.09\times24=2.16g\)
\(m_{Fe}=0.05\times56=2.8g\)
\(C\%_{H_2SO_4}=\dfrac{0.14\times98\times100}{200}=6.86\%\)
Câu 3:
\(n_{H_2}=\dfrac{1.568}{22.4}=0.07mol\)
\(Ba+H_2SO_4\rightarrow BaSO_4+H_2\)
a a a a
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}137a+24b=3.94\\a+b=0.07\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.02\\b=0.05\end{matrix}\right.\)
\(m_{Ba}=0.02\times137=2.74g\)
\(m_{Mg}=0.05\times24=1.2g\)
\(CM_{H_2SO_4}=\dfrac{0.07}{0.1}=0.7M\)
Cho một lượng hỗn hợp MgO và CuO tác dụng vừa đủ với 300ml dung dịch H2SO4 1M tạo ra 2 muối có tỉ lệ số mol là 1:1. Khối lượng MgO trong hỗn hợp ban đầu là:
Đặt \((n_{MgO};n_{CuO})=(a;b)\)
\(MgO+H_2SO_4\to MgSO_4+H_2O\\ CuO+H_2SO_4\to CuSO_4+H_2O\\ \Rightarrow n_{MgSO_4}:n_{CuSO_4}=1:1=a:b\\ \Rightarrow a=b\)
Mà \(a+b=n_{H_2SO_4}=1.0,3=0,3(mol)\)
\(\Rightarrow a=b=0,15(mol)\\ \Rightarrow m_{MgO}=0,15.40=6(g)\)
cho 16,32g hỗn hợp (x) gồm al,mg,ba tác dụng vừa đủ với dung dịch h2so4 loãng thì thu được 10,08 lít khí h2 (đktc), dung dịch (y) và tạo ra 13,98g kết tủa. a)tính khối lượng mỗi kim loại trong hỗn hợp (x) b) cho từ từ dd koh 2mol/lít vào dd (y). tính thể tích dd koh cần dùng để tạo ra kết tủa duy nhất
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của FeSO4 trong dung dịch Z là
A. 22,4 gam.
B. 30,4 gam.
C. 26,8 gam.
D. 30,0 gam.
Đáp án B
Dùng phương pháp đường chéo tính được mol CO2 là 0,2 mol và H2 là 0,15 mol.
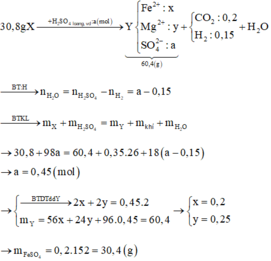
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của MgSO4 có trong dung dịch Z là
A. 38,0 gam.
B. 33,6 gam.
C. 36,0 gam.
D. 30,0 gam.
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của MgSO4 có trong dung dịch Z là:
A. 38,0 gam.
B. 33,6 gam.
C. 36,0 gam.
D. 30,0 gam.
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của MgSO4 có trong dung dịch Z là
A. 30,0 gam.
B. 33,6 gam.
C. 36,0 gam.
D. 38,0 gam.
Đáp án A
+ n C O 2 + n H 2 = 0 , 35 44 n C O 2 + 2 n H 2 = 4 . 6 , 5 . 0 , 35 = 9 , 1 ⇒ n C O 2 = 0 , 2 n H 2 = 0 , 15 + F e , F e C O 3 F e O , M g O M g , M g C O 3 → q u y đ ổ i F e ( x m o l ) M g ( y m o l ) O ( z m o l ) , C O 2 → H 2 S O 4 M g S O 4 F e S O 4 + H 2 C O 2 ⇒ 56 x + 24 y + 16 z = 30 , 8 - 0 , 2 . 44 = 22 152 x + 120 y = 60 , 4 B T E : 2 x + 2 y = 2 z + 0 , 15 . 2 ⇒ x = 0 , 2 y = 0 , 25 z = 0 , 3 ⇒ m M g S O 4 = 30 g a m
Hòa tan hoàn toàn 8,66 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 bằng dung dịch chứa hỗn hợp gồm 0,52 mol HCl và 0,04 mol HNO3 (vừa đủ), thu được dung dịch Y và 1,12 lít (đktc) hỗn hợp khí Z gồm NO và H2 có tỉ khối hơi đối với H2 là 10,8. Cho dung dịch Y tác dụng với một lượng vừa đủ dung dịch AgNO3 thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng vừa đủ dung dịch NaOH, lọc kết tủa nung đến khối lượng không đổi thu được 10,4 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 73.
B. 79.
C. 77.
D. 75.