Cho 5,6 gam kali hiđroxit phản ứng vừa đủ với axit nitric. Sau phản ứng thu được sản phẩm gồm kali nitrat và nước. Khối lượng muối thu được là
a,6,3 g b,10,1 g c,8,5 g d,1,8 g
Cho kim loại K phản ứng vừa đủ với 7,2 gam nước, sau phản ứng thu được 18,4 gam kali hidroxit (KOH) và giải phóng 0,4 gam khí hidro H2. Tính khối lượng kim loại kali dã phản ứng.
Áp dụng định luật bảo toàn khối lượng, ta có:
\(m_K+m_{H_2O}=m_{KOH}+m_{H_2}\)
\(\Leftrightarrow m_K=m_{KOH}+m_{H_2}-m_{H_2O}=18,4+0,4-7,2=11,6\left(g\right)\)
áp dụng định luật bảo toàn khối lượng, ta có:
\(m_K+m_{H_2O}=m_{KOH}+m_{H_2}\)
\(m_K+7,2=18,4+0,4\)
\(m_K+7,2=18,8\)
\(m_K=18,8-7,2=11,6g\)
vậy khối lượng Kali đã phản ứng là \(11,6g\)
Cho 7,8 g kim loại kali vào nước (dư) đến khi phản ứng xảy ra hoàn toàn.
a.Viết PTHH và nêu hiện tượng xảy ra.
b.Tính thể tích khí hiđro thu được (ở đktc)
c.Tính khối lượng kali hiđroxit thu được khi cô cạn dung dịch sau phản ứng.
\(n_K=\dfrac{m_K}{M_k}=\dfrac{7,8}{39}=0,2mol\)
\(2K+H_2O\rightarrow2KOH+H_2\)
0,2 0,2 0,1 ( mol )
\(V_{H_2}=n_{H_2}.22,4=0,1.22,4=2,24l\)
\(m_{KOH}=n_{KOH}.M_{KOH}=0,2.56=11,2g\)
Cho 59,9 gam hỗn hợp X gồm bari và kali oxit tác dụng vừa đủ với nước, sau phản ứng thu được 6,72 lít khí (đktc)
a. Tính phần trăm khối lượng mỗi chất trong hỗn hợp.
b. Tính khối lượng các chất tan trong dung dịch thu được sau phản ứng.
\(a,n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Ba + 2H2O ---> Ba(OH)2 + H2
0,3<-------------0,3<---------0,3
=> mBa = 0,3.137 = 41,1 (g)
=> mK2O = 59,9 - 41,1 = 18,8 (g)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Ba}=\dfrac{41,1}{59,9}.100\%=68,61\%\\\%m_{K_2O}=100\%-68,61\%=31,39\%\end{matrix}\right.\)
\(b,n_{K_2O}=\dfrac{18,8}{94}=0,2\left(mol\right)\)
PTHH: K2O + H2O ---> 2KOH
0,2----------------->0,4
Các chất tan trong dd sau phản ứng: KOH, Ba(OH)2
\(\rightarrow\left\{{}\begin{matrix}m_{KOH}=0,4.56=22,4\left(g\right)\\m_{Ba\left(OH\right)_2}=0,3.171=51,3\left(g\right)\end{matrix}\right.\)
Cho đi photpho penta oxit (P2O5) phản ứng vừa đủ với 3,6 gam nước thu được axit photphoric (H3PO4)
a. Tính khối lượng đi photpho penta oxit đã phản ứng ?
b. Tính khối lượng sản phẩm thu được sau phản ứng.
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\\ a,n_{P_2O_5}=n_{H_2O}:3=0,2:3=\dfrac{1}{15}\left(mol\right)\\ \Rightarrow m_{P_2O_5}=\dfrac{142.1}{15}=\dfrac{142}{15}\left(g\right)\\ b,n_{H_3PO_4}=\dfrac{2}{3}.0,2=\dfrac{2}{15}\left(mol\right)\\ \Rightarrow m_{H_3PO_4}=98.\dfrac{2}{15}=\dfrac{196}{15}\left(g\right)\)
Cho 7,8 gam Kali tác dụng hết với khí Oxi vừa đủ. Toàn bộ sản phẩm cho tác dụng với nước thu được Kali hidroxit
a) Viết PTHH minh họa phản ứng xảy ra?
b) Tính thể tích khí Oxi ( ở đktc ) cần dùng?
c) Tính khói lượng Kali hidroxit thu được?
Giúp tui vs !!!!!
\(n_K=\dfrac{m}{M}=\dfrac{7,8}{39}=0,2\left(mol\right)\)
\(a,PTHH:4K+O_2\rightarrow2K_2O\)
\(0,2:0,05:0,1\left(mol\right)\)
\(K_2O+H_2O\rightarrow2KOH\)
\(0,1:0,1:0,2\left(mol\right)\)
\(b,V_{O_2}=n.22,4=0,05.22,4=1,12\left(l\right)\)
\(c,m_{KOH}=n.M=0,2.\left(39+16+1\right)=0,2.56=11,2\left(g\right)\)
Cho 8,3 g hỗn hợp gồm Al và Fe phản ứng vừa đủ với 500 gam dung dịch HCl a% sau phản ứng thu được dung dịch chứa m gam muối và có 5,6 lít khí H2 thoát ra(dktc). Tính khối lượng mỗi kim loại, tính a và C% của các chất tan trong dung dịch sau phản ứng
Em đăng sang môn Hoá nha
Cho 8,3 g hỗn hợp gồm Al và Fe phản ứng vừa đủ với 500 gam dung dịch HCl a% sau phản ứng thu được dung dịch chứa m gam muối và có 5,6 lít khí H2 thoát ra(dktc). Tính khối lượng mỗi kim loại, tính a và C% của các chất tan trong dung dịch sau phản ứng
\(2Al+6HCl->2AlCl_3+3H_2\\ Fe+2HCl->FeCl_2+H_2\\ n_{Al}=a;n_{Fe}=b\\ 27a+56b=8,3\\ 1,5a+b=\dfrac{5,6}{22,4}=0,25\\ a=b=0,1\\ m_{Al}=27\cdot0,1=2,7g\\ m_{Fe}=8,3-2,7=5,6g\\ a=\dfrac{3a+2b}{500}\cdot36,5=3,65\%\\ m_{ddsau}=508,3-0,25\cdot2=507,8g\\ C\%_{AlCl_3}=\dfrac{133,5a}{507,8}=2,63\%\\ C\%_{FeCl_2}=\dfrac{127b}{507,8}=2,50\%\)
Có hỗn hợp X gồm 2 chất A và B chỉ chứa chức este (MA<MB). Cho a gam hỗn hợp X tác dụng vừa đủ với dung dịch KOH, sau phản ứng thu được b gam một ancol M và 13,44 gam hỗn hợp muối kali của 2 axit hữu cơ đơn chức liên tiếp nhau trong dãy đồng đẳng. Đem nung tất cả lượng hỗn hợp muối trên với vôi tôi xút dư đến phản ứng hoàn toàn thì nhận được 3,36 lit hỗn hợp khí E (đktc). Đem đốt cháy toàn bộ lượng ancol M , thu được sản phẩm cháy gồm CO2 và hơi nước có tỷ lệ về số mol CO2:H2O= 2:3. Mặt khác khi cho tất cả lượng sản phẩm cháy trên hấp thụ hết với 225 ml dung dịch Ba(OH)2 0,5M thì nhận được 14,775 g kết tủa. Nếu tỉ lệ số mol của A: B là 1:4 thì % về khối lượng của A trong hỗn hợp X là:
A. 55,78
B. 20,07
C. 54,80
D. 18,27
Đáp án D
Vì 2 muối đều của axit đơn chức
![]()
Gọi công thức trung bình của muối là RCOOK ⇒ n RCOOK = 0 , 15 mol
=> Mtb muối = 89,6g
=> 2 muối là HCOOK và CH3COOK với số mol lần lượt là x ; y
=> x + y = nmuoi = 0,15 mol và mmuối = 84x + 98y = 13,44g
=> x = 0,09 ; y = 0,06 mol
Ancol B đốt cháy có:
![]()
=2:6 =1:3
=> ancol thỏa mãn là C2H6Ox
Cho sản phẩm cháy vào 0,1125 mol Ba(OH)2 ta có :
+) TH1:OH− dư
![]()
![]()
=> ancol có 4 nhóm OH => Loại vì M chỉ có 2C
+) TH2: có tan 1 phần kết tủa
![]()
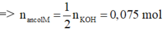
=> ancol M là C2H6O2(C2H4(OH)2)
=> các este trong X đều là este 2 chức
Vì MA<MB => A chắc chắn có 1 nhóm HCOO và B chắc chắn có 1 nhóm CH3COO
Mà nA:nB = 1 : 4 và nHCOO=0,09>nCH3COO=0,06
=> A là (HCOO)2C2H4 và B là HCOOC2H4OOCCH3
=> nA = 0,015 ; nB = 0,06 mol
=> %mA=18,27%
Có hỗn hợp X gồm 2 chất A và B chỉ chứa chức este (MA<MB). Cho a gam hỗn hợp X tác dụng vừa đủ với dung dịch KOH, sau phản ứng thu được b gam một ancol M và 13,44 gam hỗn hợp muối kali của 2 axit hữu cơ đơn chức liên tiếp nhau trong dãy đồng đẳng. Đem nung tất cả lượng hỗn hợp muối trên với vôi tôi xút dư đến phản ứng hoàn toàn thì nhận được 3,36 lit hỗn hợp khí E (đktc). Đem đốt cháy toàn bộ lượng ancol M , thu được sản phẩm cháy gồm CO2 và hơi nước có tỷ lệ về số mol CO2:H2O= 2:3. Mặt khác khi cho tất cả lượng sản phẩm cháy trên hấp thụ hết với 225 ml dung dịch Ba(OH)2 0,5M thì nhận được 14,775 g kết tủa. Nếu tỉ lệ số mol của A: B là 1:4 thì % về khối lượng của A trong hỗn hợp X là:
A. 55,78
B. 20,07
C. 54,80
D. 18,27