Nguyên tử X có điện tích hạt nhân là +2,7234.10-18 C. Trong ngtử X số hạt mag điện nhiều hơn số hạt không mang điện là 16. Kí hiệu ngtử của X là

Những câu hỏi liên quan
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là A.
C
17
37
l
B.
K
19
40
C.
C
17
35
l
D.
K...
Đọc tiếp
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
A. C 17 37 l
B. K 19 40
C. C 17 35 l
D. K 19 39
Có số p = số e=
2
,
7234
.
10
-
18
1
,
6
.
10
-
19
= 17
Số hạt mang đinẹ nhiều hơn số hạt không mang điện là 16 → n = 17.2 - 16 = 18
Vậy số khối của X là A= n + p = 18 + 17 = 35
Số hiệu nguyên tử của X là Z= p = 17
Vậy kí hiệu của X là
C
17
35
l
.
Đáp án C.
Đúng 0
Bình luận (0)
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là: A.
C
17
37
l
B.
K
19
39
C.
K
19
40
D.
C
17...
Đọc tiếp
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là:
A. C 17 37 l
B. K 19 39
C. K 19 40
D. C 17 35 l
Đáp án A
Điện tích hạt nhân = số p . (+1,602.10-19) = +2,7234.10-18C.
=> Số p = 17, số n = 17 + 16 = 33
Đúng 0
Bình luận (0)
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
Đọc tiếp
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
![]()
![]()
![]()
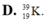
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là A.
C
17
37
l
B.
K
19
39
C.
K
19
40
D....
Đọc tiếp
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
A. C 17 37 l
B. K 19 39
C. K 19 40
D. C 17 35 l
Đáp án D
1 hạt proton có điện tích là +1,602.10-19C.
=> Số hạt proton trong X = 17
Trong X số hạt mang điện nhiều hơn số hạt không mang điện là 16:
2p – n = 16 => n = 18
Số khối của X = p + n = 35
Đúng 0
Bình luận (0)
tổng số hạt cơ bản ngtử trong hạt nhân ngtử x là 27 . trong hạt nhân ng tử x có hạt mag điện ít hơn hạt ko mag điện là 1 hạt , xác định số p,n,e giúp em vs ạ
Bài 4.Viết kí hiệu nguyên tử các trường hợp sau: a. Tổng số hạt của 1 nguyên tử là 58. Biết số khối nhỏ hơn 40 b. Tổng số hạt của 1 ngtử là 52. Số hạt không mang điện nhiều hơn số hạt mang điện âm là 1 hạt. c. Tổng số hạt là 60. số hạt mang điện gấp 2 lần số hạt không mang điện. d. Tổng số hạt là 126. Số nơtron nhiều hơn số e là 12 hạt.
\(a,^{39}_{19}K\\ b,^{35}_{17}Cl\\ c,^{40}_{20}Ca\\ d,^{88}_{38}Sr\)
Đúng 0
Bình luận (0)
a) Tổng số hạt mang điện trong nguyên tử X là 18, nguyên tử X có tổng số hạt mang điện gấp đôi số hạt không mang điện. Hãy viết kí hiệu nguyên tử X b) Tổng số hạt P,E,N trong nguyên tử X là 156, số hạt mang điện nhiều hơn số hạt không mang điện là 32. Tìm số hạt P,E,N, số khối của X.
a) Ta có : \(\left\{{}\begin{matrix}2Z=18\\2Z=2N\end{matrix}\right.\)
=> Z=N=9
Vậy X là Flo (F)
b) Ta có : \(\left\{{}\begin{matrix}2Z+N=156\\2Z-N=32\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}Z=47=P=E\\N=62\end{matrix}\right.\)
A=Z+N=47+62=109
Đúng 2
Bình luận (2)
Một nguyên tử X có tổng số hạt là 155, số hạt mang điện nhiều hơn số hạt không mang điện là 33. Xác định điện tích hạt nhân, nguyên tử khối và viết kí hiệu của nguyên tử X
Ta có: \(\left\{{}\begin{matrix}2Z+N=155\\2Z-N=33\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}Z=47\\N=61\end{matrix}\right.\)
Điện tích hạt nhân: 47+
Nguyên tử khối: 108
Kí hiệu: Ag
Đúng 2
Bình luận (0)
\(X(2p, n) \begin{cases} 2p+n=155\\ 2p-n=33 \end{cases}\Leftrightarrow \begin{cases} p=e=47\\ n=61 \end{cases} \to: Ag\)
Đúng 1
Bình luận (0)
1. Nguyên tử của nguyên tố X có tổng số hạt là 28. Trong HẠT NHÂN, số hạt không mang điện nhiều hơn số hạt mang điện là 1. Tìm X? Viết kí hiệu nguyên tử của X?
Gọi số hạt proton = số hạt electron = p
Gọi số hạt notron = n
Ta có :
$2p + n = 28$ và $n - p = 1$
Suy ra p = 9 ; n = 10
Vậy X là nguyên tố Flo, KHHH : F
Đúng 0
Bình luận (0)


















