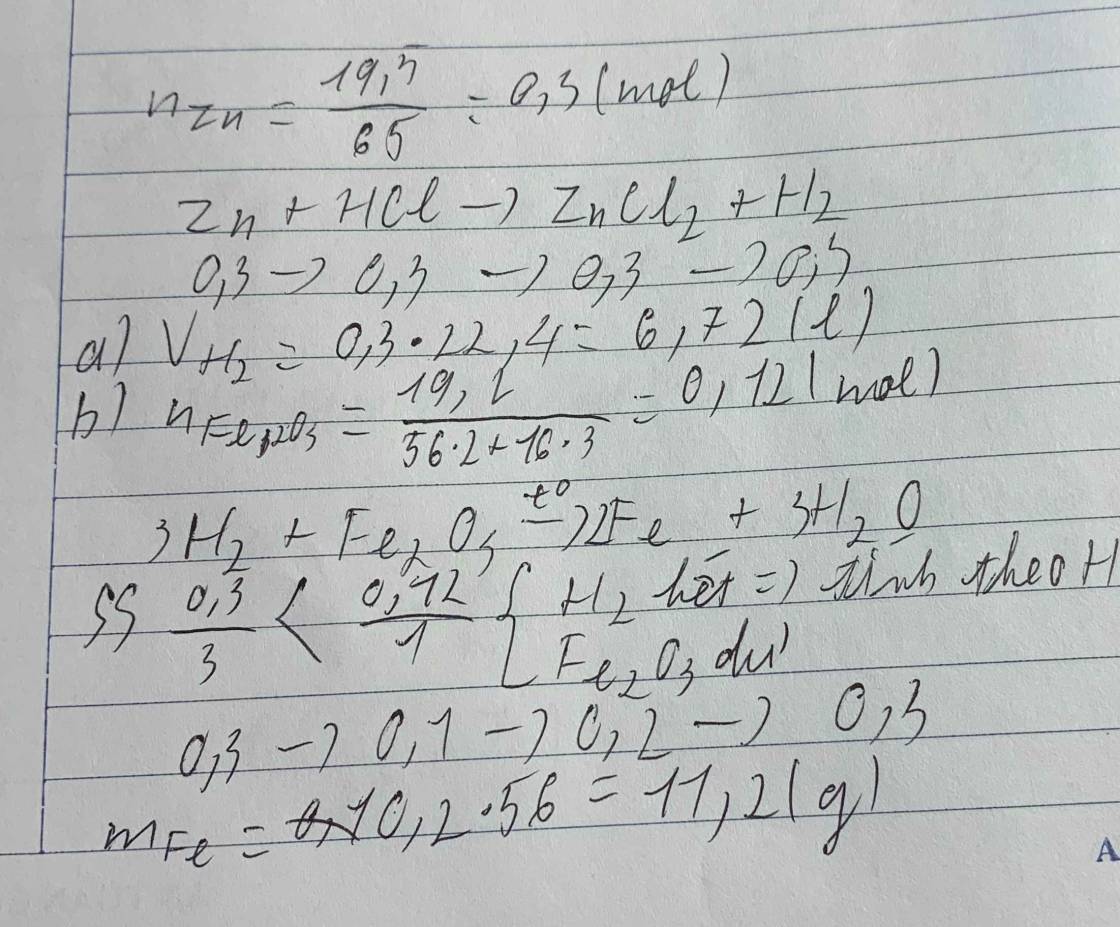Tính thể tích H2 (đktc) khi khử 3,6g Fe(ll) bằng khí H2 ở nhiệt độ cao

Những câu hỏi liên quan
khử 4,64g fe3o4 ở nhiệt độ cao bằng 8,96 lit h2 ở đktc.
b tính khối lượng các chất sau phản ứng.
c toàn bộ lượng fe tạo thành cho tác dụng với 0,5 mol hcl. tính thể tích khí h2 thu được ở đktc
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
0,02 0,4 0 0
0,02 0,08 0,06 0,08
0 0,32 0,06 0,08
b)\(m_{Fe}=0,06\cdot56=3,36g\)
\(m_{H_2O}=0,08\cdot18=1,44g\)
c)\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,06 0,5 0 0
\(\Rightarrow\)Tính theo \(Fe\)
\(\Rightarrow V_{H_2}=0,06\cdot22,4=1,344l\)
Đúng 2
Bình luận (0)
Người ta điều chế 3,6138.1023 nguyên tử Fe bằng cách cho khí H2 khử Fe2O3 nhiệt độ cao. Tính thể tích khí H2 và khối lượng Fe2O3 cần dùng để thực hiện quá trình điều chế trên (đktc).
Theo gt ta có: $n_{Fe}=0,6(mol)$
$Fe_2O_3+3H_2\rightarrow 2Fe+3H_2O$
Ta có: $n_{H_2}=0,6.3=1,8(mol)\Rightarrow V_{H_2}=40,32(l)$
$n_{Fe_2O_3}=0,3(mol)\Rightarrow m_{Fe_2O_3}=48(g)$
Đúng 2
Bình luận (0)
Bài 2(2 điểm)Dùng H2 để khử 16 g Fe2O3 ở nhiệt độ cao a/ Viết phương trình hóa học của phản ứng?
b/ Tính khối lượng Fe và thể tích khí H2 (đktc) cần dùng.
a) Fe2O3 + 3H2 --to--> 2Fe + 3H2O
b) \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1--->0,3--------->0,2
=> mFe = 0,2.56 = 11,2 (g)
VH2 = 0,3.22,4 = 6,72 (l)
Đúng 1
Bình luận (0)
: Khử hoàn toàn 12,8 gam Fe2O3 bằng khí hiđro ở nhiệt độ cao. a. Tính thể tích hiđro cần dùng ở đktc?b. Tính khối lượng Fe thu được sau phản ứng?c. Nếu đem toàn bộ lượng Fe thu được ở trên tác dụng với 14,6 gam axit HCl thì thu được bao nhiêu lít H2 (đktc)?
Đọc tiếp
: Khử hoàn toàn 12,8 gam Fe2O3 bằng khí hiđro ở nhiệt độ cao.
a. Tính thể tích hiđro cần dùng ở đktc?
b. Tính khối lượng Fe thu được sau phản ứng?
c. Nếu đem toàn bộ lượng Fe thu được ở trên tác dụng với 14,6 gam axit HCl thì thu được bao nhiêu lít H2 (đktc)?
Để giải bài toán này, ta cần biết phương trình phản ứng giữa oxit sắt (Fe2O3) và khí hidro (H2):
Fe2O3 + 3H2 → 2Fe + 3H2O
Theo đó, mỗi mol Fe2O3 cần 3 mol H2 để khử hoàn toàn thành Fe.
a) Thể tích khí hiđro cần dùng:
Ta cần tìm số mol khí hidro cần dùng để khử hoàn toàn 12,8 gam Fe2O3.Khối lượng mol của Fe2O3 là:M(Fe2O3) = 2x56 + 3x16 = 160 (g/mol)
Số mol Fe2O3 là:n(Fe2O3) = m/M = 12.8/160 = 0.08 (mol)
Theo phương trình phản ứng, mỗi mol Fe2O3 cần 3 mol H2 để khử hoàn toàn thành Fe.Vậy số mol H2 cần dùng là:n(H2) = 3*n(Fe2O3) = 0.24 (mol)
Thể tích khí hidro cần dùng ở đktc là:V(H2) = n(H2)22.4 = 0.2422.4 = 5.376 (lít)
Vậy thể tích khí hiđro cần dùng ở đktc là 5.376 lít.
b) Khối lượng Fe thu được sau phản ứng:
Theo phương trình phản ứng, mỗi mol Fe2O3 tạo ra 2 mol Fe.Vậy số mol Fe thu được là:n(Fe) = 2*n(Fe2O3) = 0.16 (mol)
Khối lượng Fe thu được là:m(Fe) = n(Fe)M(Fe) = 0.1656 = 8.96 (gam)
Vậy khối lượng Fe thu được sau phản ứng là 8.96 gam.
c) Thể tích khí hiđro thu được khi Fe tác dụng với HCl:
Ta cần tìm số mol H2 thu được khi Fe tác dụng với HCl.Theo phương trình phản ứng, mỗi mol Fe tác dụng với 2 mol HCl để tạo ra H2 và muối sắt (FeCl2).Số mol HCl cần dùng để tác dụng với Fe là:n(HCl) = m(HCl)/M(HCl) = 14.6/36.5 = 0.4 (mol)
Vậy số mol H2 thu được là:n(H2) = 2n(Fe) = 2(m(Fe)/M(Fe)) = 2*(8.96/56) = 0.16 (mol)
Thể tích khí hiđro thu được ở đktc là:V(H2) = n(H2)22.4 = 0.1622.4 = 3.584 (lít)
Vậy thể tích khí hiđro thu được ở đktc là 3.584 lít.

Đúng 0
Bình luận (0)
Dùng H2 để khử Fe2O3 ở nhiệt độ cao
a/ Viết phương trình hóa học của phản ứng?
b/ Sau pư thu được 16,8g Fe. Tính khối lượng Fe2O3 và thể tích khí H2 (đktc) cần dùng.
nFe2O3 = 16,8/56 = 0,3 (mol)
PTHH: Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
MOL: 0,15 <--- 0,45 <--- 0,3
VH2 = 0,45 . 22,4 = 10,08 (l)
mFe2O3 = 0,45 . 160 = 72 (g)
a ) Fe2O3 + 3H2 ---> 2Fe + 3H2O
nFe = 16,8 :56 =0,3
Fe2O3 + 3H2--> 2Fe +3H2O
0,15<------0,45<---- 0,3
VH2 = 0,45.22,4=10,08(l)
mFe2O3 = 0,15.160 =24(g)
Đúng 1
Bình luận (0)
dùng khí h2 vừa đủ để khử hoàn toàn 34,8g một oxit sắt ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được 25,2g sắt, làm lạnh hơi nước thu được sau phản ứng. a. tính thể tích khí H2 đã phản ứng ở đktc b. xác định CTHH của oxit sắt đó c. tính thể tích nước thu đc ở thể lỏng ( giải thích các bước làm )
a) \(n_O=\dfrac{34,8-25,2}{16}=0,6\left(mol\right)\)
=> \(n_{H_2O}=0,6\left(mol\right)\) (bảo toàn O)
=> \(n_{H_2}=0,6\left(mol\right)\) (bảo toàn H)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b) \(n_{Fe}=\dfrac{25,2}{56}=0,45\left(mol\right)\)
nFe : nO = 0,45 : 0,6 = 3 : 4
=> CTHH: Fe3O4
c) \(m_{H_2O}=0,6.18=10,8\left(g\right)\)
Mà \(d_{H_2O}=1\left(g/ml\right)\)
=> \(V_{H_2O}=10,8\left(ml\right)\)
Đúng 2
Bình luận (0)
Cho 19,5 g kẽm tác dụng hết với dung dịch axit clohiđric. a. Tính thể tích khí H2 sinh ra (ở đktc). b. Nếu dùng thể tích H2 trên để khử 19,2 g sắt (III) oxit ở nhiệt độ cao thì thu được bao nhiêu gam sắt
Cho 13g Fe phản ứng hoàn toàn với dung dịch HCL 1/ Vt PTHH 2/ Tính thể tích khí hidro ở đktc 3/ Nếu dùng toàn bộ lượng H2 bay ra ở trên đem khử 12g bột CuO ở nhiệt độ cao thì chất nào còn dư bao nhiêu gam?
a) Nhiệt phân m gam KMnO4 thu được 11,2 lít khí oxi (đktc). Tính m. (K 39; Mn 55; O 16)b) Khử hoàn toàn 80 gam Fe2O3 bằng V lít (đktc) khí hiđro ở nhiệt độ cao. Tính V. ( Fe 56; O 16)c) Cho 8 gam bột CuO tác dụng với 1,12 lít khí H2 (đktc) ở nhiệt độ cao. (O 16; Cu 64)- Chất nào còn dư sau phản ứng và dư là bao nhiêu mol?- Tính khối lượng chất rắn và thể tích chất khí (đktc) thu được sau phản ứng.
Đọc tiếp
a) Nhiệt phân m gam KMnO4 thu được 11,2 lít khí oxi (đktc). Tính m. (K = 39; Mn = 55; O = 16)
b) Khử hoàn toàn 80 gam Fe2O3 bằng V lít (đktc) khí hiđro ở nhiệt độ cao. Tính V. ( Fe = 56; O = 16)
c) Cho 8 gam bột CuO tác dụng với 1,12 lít khí H2 (đktc) ở nhiệt độ cao. (O = 16; Cu = 64)
- Chất nào còn dư sau phản ứng và dư là bao nhiêu mol?
- Tính khối lượng chất rắn và thể tích chất khí (đktc) thu được sau phản ứng.
a) \(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
1<-----------------------------0,5
=> \(m_{KMnO_4}=1.158=158\left(g\right)\)
b) \(n_{Fe_2O_3}=\dfrac{80}{160}=0,5\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,5--->1,5
=> \(V_{H_2}=1,5.22,4=33,6\left(l\right)\)
c) \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,05}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,05<-0,05---->0,05-->0,05
=> \(n_{Cu\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\)
mCu = 0,05.64 = 3,2 (g)
VH2O = 0,05.22,4 = 1,12 (l)
Đúng 2
Bình luận (0)
a)\(n_{O_2}=\dfrac{11,2}{22,4}=0,5mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
1 0,5
\(M_{KMnO_4}=1\cdot158=158g\)
b)\(n_{Fe_2O_3}=\dfrac{80}{160}=0,5mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,5 1,5
\(V_{H_2}=1,15\cdot22,4=25,76l\)
Đúng 0
Bình luận (0)