Trong tinh thể hidrat của muối NO3 kim loại hóa trị 3,H2O kết tinh chiếm 40,099% về khối lượng.Hãy xác định công thức biết N chiếm 10.396% về khối lượng
P/s: giúp mk nha!! mk đang cần bài giải gấp...ths mấy bn!!
Ta có :
\(\%H_2O = \dfrac{18n}{M + 62.3 + 18n}.100\% = 40,099\%\\ \Rightarrow M + 62.3 = \dfrac{242}{9}n(1)\\ %N = \dfrac{14.3}{M + 62.3 + 18n}.100\% = 10,4\%\\ \Rightarrow M + 18n = \dfrac{2832}{13}(2)\\ (1)(2)\Rightarrow M = 56(Sắt) ; n = 9\)
CTHH cần tìm : \(Fe(NO_3)_3.9H_2O\)
\(\%H_2O= \dfrac{18n}{M + 62.3+18n}.100\% = 40,099\%\\ \Rightarrow M + 62.3 = \dfrac{242}{9}n(1)\\ \%N = \dfrac{14.3}{M + 62.3 + 18n}.100\% = 10,4\%\\ \Rightarrow M + 18n = \dfrac{2832}{13}(2)\\ (1)(2) \Rightarrow M = 56(Sắt) ; n = 9\\ \)
CTHH cần tìm : \(Fe(NO_3)_3.9H_2O\)
Trong tinh thể hyrat của 1 muối nitrat kim loại hóa trị III, nước kết tinh chiếm 40,099% về khối lượng. Hãy xác định công thức tinh thể. Biết nitơ chiếm 10,396% về khối lượng
bài này nếu 9h tốiko ai làm thì mk sẽ làm cho nha
chuẩn bị ăn cơm
thôi,làm liều!!!
Gọi CTHH của tinht thể là \(R\left(NO_3\right)_3.nH_2O_{ }\)
ta có %mH2O=40,099%
=> \(\dfrac{18n}{18n+M_R+186}=0,40099\)
Mặt khác %mN= 10,396%
=> \(\dfrac{14.3}{18n+M_R+186}=\dfrac{2599}{25000}\)
=> \(18n+M_R+186\approx404\)
=> \(18n=404.0,40099\approx162=>n=9\)
\(18.9+M_R+186=404=>M_R=56\left(Fe\right)\)
vậy CTHH là \(Fe\left(NO_3\right)_3.9H_2O\)
trong thành phần tinh thể hidrat của 1 hidroxit kim loại hóa trị II thfi khối lượng nước tinh thể kết tinh=24% khối lượng kim loại =60,88% xác định tinh thể
CTHH: R(OH)2.xH2O
\(\%m_{OH}=100\%-24\%-60,88\%=15,12\%\)
Xét \(\dfrac{m_R}{m_{OH}}=\dfrac{60,88\%}{15,12\%}=\dfrac{761}{189}\)
=> \(\dfrac{1.M_R}{2.17}=\dfrac{761}{189}\)
=> MR = 137 (g/mol)
=> R là Ba
=> CTHH: Ba(OH)2.xH2O
Có: \(\%H_2O=\dfrac{18x}{171+18x}.100\%=24\%\)
=> x = 3
=> CTHH: Ba(OH)2.3H2O
trong tinh thể hidrat hóa của muối sunfat kim loại có hóa trị 2, thành phần nước tinh khiết chiếm 20,93%, S chiếm 18,61%. hãy xác định công thức hóa học
CTHH dạng TQ là BSO4.xH2O
* Có : %S/muối tinh thể = \(\dfrac{1.M_S}{M_{BSO4.xH2O}}.100\%=18,61\%\)
=> \(\dfrac{32}{M_{BSO4.xH2O}}=0,1861\)
=> MBSO4.xH2O =172(g)
* Có : %H2O/muối tinh thể = \(\dfrac{x.M_{H2O}}{M_{BSO4.xH2O}}.100\%=20,93\%\)
=> \(\dfrac{x.18}{172}=0,2093\)
=> x = 2
* Lại có : MBSO4.xH2O = 172(g)
mà x =2
=> MB + 96 + 2 .18 =172 => MB = 40(g) => B là Canxi(Ca)
=> CTHH là CaSO4.2H2O
Một muối sunfat của kim loại hóa trị II ngậm nước có phân tử khối 278 gam và khối lượng nước kết tinh chiếm 45,324%. Tìm công thức hóa học của muối trên.
Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
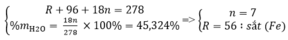
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O
Kim loại R tạo ra 2 muối RCln và RClm biết clorua ở mức hóa trị thấp Cl chiếm 55,91% về khối lượng , muối clorua ở mức hóa trị cao Cl chiếm 65,539% về khối lượng . Xác định kim loại R
Giả sử n < m
- Với RCln: \(\%Cl=\dfrac{35,5n}{M_R+35,5n}.100\%=55,91\%\)
=> MR = 28n (g/mol)
- Với RClm: \(\%Cl=\dfrac{35,5m}{M_R+35,5m}.100\%=65,539\%\)
=> MR = 18,66m (g/mol)
TH1: n = 1 => MR = 28 => Loại
TH2: n = 2 => MR = 56 (g/mol) => R là Fe => m = 3 (thỏa mãn)
Thế gọi n là hoá trị thấp, m là hoá trị cao. (m,n:nguyên, dương)
\(\Rightarrow\left\{{}\begin{matrix}\dfrac{35,5n}{M_R+35,5n}.100\%=55,91\%\\\dfrac{35,5m}{M_R+35,5m}.100\%=65,539\%\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}\dfrac{M_R}{35,5n}=\dfrac{44,09\%}{55,91\%}=0,789\\\dfrac{M_R}{35,5m}=\dfrac{34,461\%}{65,539\%}=0,526\end{matrix}\right.\)
Xét các giá trị từ 1 đến 3 (m>n) ta nhận giá trị n=2 và m=3 => MR=56(g/mol)
=> R là Sắt (Fe=56)
Mừng năm mới 2022!
Chúc mọi người một năm vui vẻ, bình an, nhiều thành công trong công việc và cuộc sống
Kim loại (có hóa trị không đổi) trong muối sunfat chứa 40% về khối lượng.Không cần xác định tên kim loại, hãy tính phần trăm theo khối lượng của kim loại đó trong hợp chất với oxi.
giúp vs ạ, mk cần gấp
c1 : trong thành phần muối photphat của kim loại M (II), nguyên tố P chiếm 20% về khối lượng .xác định kim loại M và côngg thức của muối
c2: trong thành phần muối photphat của kim loai M hóa trị (II) không đổi .nguyên tố M chiếm khoảng 38,7% khối lượng trong thành phần muối cacbonat kim loại đó chiếm bao nhiêu phần trăm về khối lượng
c3: trong thành phần muối photphat của kim loai M hóa trị n không đổi ,nguyên tố M chiếm khoảng 40% khối lượng thì trong thành phần muối photphat kim loai đó chiếm baoo nhiêu phần trăm về khối lượng
\
Câu 1 :
Gọi CTHH muối là $M_3(PO_4)_2$
$\%P = \dfrac{31.2}{3M + 95.2}.100\% = 20\%$
$\Rightarrow M = 40(Ca)$
Vậy muối là $Ca_3(PO_4)_2$
Câu 2 :
Gọi CTHH muối là $M_3(PO_4)_2$
$\%M = \dfrac{3M}{3M + 95.2}.100\% = 38,7\%$
$\Rightarrow M = 40(Ca)$
Trong $CaCO_3$, $\%Ca = \dfrac{40}{100}.100\% = 40\%$
Xác định công thức của hợp chất C biết chất C là hợp chất của kim loại Q (hóa trị n; n = 1; 2 hoặc 3) với nhóm SO4, trong đó Q chiếm 15,79% về khối lượng.
- Nếu n = 1
CTHH: Q2SO4
Có: \(\%Q=\dfrac{2.M_Q}{2.M_Q+96}.100\%=15,79\%\)
=> MQ = 9 (Loại)
- Nếu n = 2
CTHH: QSO4
\(\%Q=\dfrac{M_Q}{M_Q+96}.100\%=15,79\%\)
=> MQ = 18 (Loại)
- Nếu n = 3
CTHH: Q2(SO4)3
\(\%Q=\dfrac{2.M_Q}{2.M_Q+288}.100\%=15,79\%\)
=> MQ = 27 (g/mol)
=> Q là Al
Vậy C là Al2(SO4)3