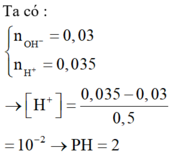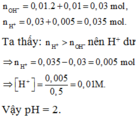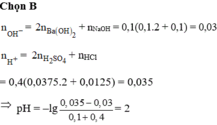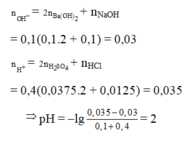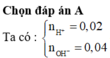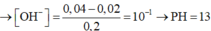Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch gồm H2SO4 0,0375 M và HCl 0,0125 M thu được dung dịch X. Tính pH của dung dịch X .

Những câu hỏi liên quan
Trộn 100 ml dung dịch (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch (gồm H2SO4 0,0375M và HCl 0,0125M), thu được dung dịch X. Giá trị pH của dung dịch X là A. 7 B. 2 C. 1. D. 6
Đọc tiếp
Trộn 100 ml dung dịch (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch (gồm H2SO4 0,0375M và HCl 0,0125M), thu được dung dịch X. Giá trị pH của dung dịch X là
A. 7
B. 2
C. 1.
D. 6
Đáp án B
nOH- = 0,1.2.0,1 + 0,1.0,1 = 0,03
nH+ = 0,4.2.0,0375 + 0,4.0,0125 = 0,035
⇒ Trong X có H+ dư
⇒ nH+/X =0,035 – 0,03 = 0,005; VX = 100 + 400 = 500ml
⇒ [H+] = 0,01 ⇒ pH = 2.
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch gồm: H2SO4 0,0375M và HCl 0,0125M thu được dung dịch X. Giá trị pH của X là A. 1 B. 2 C. 6 D. 7
Đọc tiếp
Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch gồm: H2SO4 0,0375M và HCl 0,0125M thu được dung dịch X. Giá trị pH của X là
A. 1
B. 2
C. 6
D. 7
Trộn 100 ml dung dịch A (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch B (gồm H2SO4 0,0375M và HCl 0,0125M), thu được dung dịch X. Giá trị pH của dung dịch X là
A. 1
B. 2
C. 12
D. 13
Trộn 100 ml dung dịch (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch X có giá trị pH của X là: A. 1. B. 2. C. 7. D. 6.
Đọc tiếp
Trộn 100 ml dung dịch (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch X có giá trị pH của X là:
A. 1.
B. 2.
C. 7.
D. 6.
Trộn 100 ml dung dịch X (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch Y (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch Z. Giá trị pH của dung dịch Z là: A. 1. B. 2. C. 6. D. 7
Đọc tiếp
Trộn 100 ml dung dịch X (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch Y (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch Z. Giá trị pH của dung dịch Z là:
A. 1.
B. 2.
C. 6.
D. 7
Trộn 100 ml dung dịch X (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch Y (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch Z. Giá trị pH của dung dịch Z là:
A. 1.
B. 2.
C. 6.
D. 7.
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là: A. 13,0 B. 1,2 C. 1,0 D. 12,8
Đọc tiếp
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là:
A. 13,0
B. 1,2
C. 1,0
D. 12,8
Đáp án A
nH+ = 0,02 mol; nOH-= 0,04 mol
H+ + OH- → H2O
0,02 0,04
nOH- dư = 0,02 mol; [OH-] dư = 0,02/0,2 = 0,1M suy ra [H+] = 10-13 M suy ra pH = 13
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là
A. 13,0
B. 1,0
C. 1,2
D. 12,8
Đáp án A
nH+ = 0,02 mol; nOH-= 0,04 mol
H+ + OH- → H2O
0,02 0,04
nOH- dư = 0,02 mol; [OH-] dư = 0,02/0,2 = 0,1M suy ra [H+] = 10-13 M suy ra pH = 13
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là A. 13,0 B. 1,0 C. 1,2 D. 12,8
Đọc tiếp
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là
A. 13,0
B. 1,0
C. 1,2
D. 12,8
Đáp án A
nH+ = 0,02 mol; nOH-= 0,04 mol
H+ + OH- → H2O
0,02 0,04
nOH- dư = 0,02 mol; [OH-] dư = 0,02/0,2 = 0,1M suy ra [H+] = 10-13 M suy ra pH = 13
Đúng 0
Bình luận (0)