X là 1 muối vô cơ trong phòng thi nghiệm Nung nóng 2 khí Y và Z trong đó khí Y không màu không mùi.Còn Z là 1 chất tao bởi 2 nguyên tố hidro và oxi xác định CTHH của X

Những câu hỏi liên quan
X, Y, Z là 3 hợp chất của 1 kim loại hoá trị I, khi đốt nóng ở nhiệt độ cao cho ngọn lửa màu vàng. X tác dụng với Y tạo thành Z. Nung nóng Y thu được chất Z và 1 chất khí làm đục nước vôi trong, nhưng không làm mất màu dung dịch nước Br2. X, Y, Z là: A. X là NaHCO3; Y là NaOH; Z là Na2CO3. B. X là K2CO3; Y là KOH; Z là KHCO3. C. X là Na2CO3; Y là NaHCO3; Z là NaOH. D. X là NaOH; Y là NaHCO3; Z là Na2CO3.
Đọc tiếp
X, Y, Z là 3 hợp chất của 1 kim loại hoá trị I, khi đốt nóng ở nhiệt độ cao cho ngọn lửa màu vàng. X tác dụng với Y tạo thành Z. Nung nóng Y thu được chất Z và 1 chất khí làm đục nước vôi trong, nhưng không làm mất màu dung dịch nước Br2. X, Y, Z là:
A. X là NaHCO3; Y là NaOH; Z là Na2CO3.
B. X là K2CO3; Y là KOH; Z là KHCO3.
C. X là Na2CO3; Y là NaHCO3; Z là NaOH.
D. X là NaOH; Y là NaHCO3; Z là Na2CO3.
Đáp án D
+ Đốt cháy X, Y, Z cho ngọn lửa màu vàng, chứng tỏ chúng là hợp chất của Na.
+ Phương trình phản ứng:
NaHCO 3 ⏟ X + NaHCO 3 ⏟ Y → Na 2 CO 3 ⏟ Z + H 2 O 2 NaHCO 3 ⏟ Y → Na 2 CO 3 ⏟ Z + CO 2 ↑ ⏟ khí làm đục nước vôi trong CO 2 + Ca ( OH ) 2 → CaCO 3 ↓ + H 2 O
Đúng 0
Bình luận (0)
X, Y, Z là 3 hợp chất của 1 kim loại hoá trị I, khi đốt nóng ở nhiệt độ cao cho ngọn lửa màu vàng. X tác dụng với Y tạo thành Z. Nung nóng Y thu được chất Z và 1 chất khí làm đục nước vôi trong, nhưng không làm mất màu dung dịch nước Br2. X, Y, Z là: A. X là K2CO3; Y là KOH; Z là KHCO3 B. X là NaHCO3; Y là NaOH; Z là Na2CO3 C. X là Na2CO3; Y là NaHCO3; Z là NaOH D. X là NaOH; Y là NaHCO3; Z là Na2CO3
Đọc tiếp
X, Y, Z là 3 hợp chất của 1 kim loại hoá trị I, khi đốt nóng ở nhiệt độ cao cho ngọn lửa màu vàng. X tác dụng với Y tạo thành Z. Nung nóng Y thu được chất Z và 1 chất khí làm đục nước vôi trong, nhưng không làm mất màu dung dịch nước Br2. X, Y, Z là:
A. X là K2CO3; Y là KOH; Z là KHCO3
B. X là NaHCO3; Y là NaOH; Z là Na2CO3
C. X là Na2CO3; Y là NaHCO3; Z là NaOH
D. X là NaOH; Y là NaHCO3; Z là Na2CO3
Tiến hành thí nghiệm như hình vẽ bên : cho viên kẽm vào dung dịch HCl thấy có khí X thoát ra; dẫn khí X đi qua chất rắn Y nung nóng thu được khí Z; sục khí Z vào dung dịch muối T thấy xuất hiện kết tủa màu đen. Biết rằng: Y là đơn chất rắn, màu vàng; dung dịch muối T có màu xanh và T có khối lượng mol là 160 gam. Xác định các chất X, Y, Z, T. Viết các phương trình hóa học minh họa.
Đọc tiếp
Tiến hành thí nghiệm như hình vẽ bên : cho viên kẽm vào dung dịch HCl thấy có khí X thoát ra; dẫn khí X đi qua chất rắn Y nung nóng thu được khí Z; sục khí Z vào dung dịch muối T thấy xuất hiện kết tủa màu đen.
Biết rằng: Y là đơn chất rắn, màu vàng; dung dịch muối T có màu xanh và T có khối lượng mol là 160 gam. Xác định các chất X, Y, Z, T. Viết các phương trình hóa học minh họa.
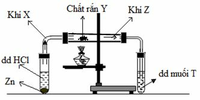
+ X là khí hiđro, kí hiệu H2
+ Y là đơn chất rắn màu vàng => Y là lưu huỳnh, kí hiệu S
+ Z là khí hiđro sunfua, kí hiệu H2S
+ Dung dịch T có màu xanh lam => T là dung dịch muối của đồng
Mà khối lượng mol của Y là 160 => T là muối đồng (II) sunfat, kí hiệu CuSO4
Đúng 0
Bình luận (0)
Cho 2,16 gam hỗn hợp gồm Al và Mg tan hết trong dung dịch axit HNO3 loãng, đun nóng nhẹ tạo ra dung dịch X và 448 ml (đo ở 354,90K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỉ khối của Y so với oxi bằng 0,716 lần tỉ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi thu được 3,84 gam chất rắn T. Giá trị của m là: A. 15,18 C. 16,68 B. 17,92 D. 15,48
Đọc tiếp
Cho 2,16 gam hỗn hợp gồm Al và Mg tan hết trong dung dịch axit HNO3 loãng, đun nóng nhẹ tạo ra dung dịch X và 448 ml (đo ở 354,90K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỉ khối của Y so với oxi bằng 0,716 lần tỉ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi thu được 3,84 gam chất rắn T. Giá trị của m là:
A. 15,18
C. 16,68
B. 17,92
D. 15,48
Đáp án D

=> m = 2,16 + 62.0,21 + 80.0,00375 = 15,48
Đúng 0
Bình luận (0)
Cho 2,16 gam hỗn họp gồm Al và Mg tan hết trong dung dịch axit HNO3 loãng, đun nóng nhẹ tạo ra dung dịch X và 448 ml (đo ở 354,9°K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỷ khối của Y so vói oxi bằng 0,716 lần tỷ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi thu được 3,84 gam chất rắn T. Giá trị của m là A. 15,18. B. 17,92. C. 16,68. D. 15,48.
Đọc tiếp
Cho 2,16 gam hỗn họp gồm Al và Mg tan hết trong dung dịch axit HNO3 loãng, đun nóng nhẹ tạo ra dung dịch X và 448 ml (đo ở 354,9°K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỷ khối của Y so vói oxi bằng 0,716 lần tỷ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi thu được 3,84 gam chất rắn T. Giá trị của m là
A. 15,18.
B. 17,92.
C. 16,68.
D. 15,48.
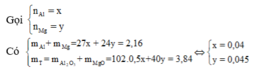
![]()
=> 2 khí đó là N 2 v à N 2 O
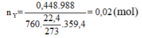
Áp dụng phương pháp đường chéo ta được:
n N 2 = n N 2 O = 0,01 mol
Ta thấy:
![]()
Suy ra phản ứng sinh muối N H 4 N O 3 :
![]()
Áp dụng định luật bảo toàn e, ta có:
![]()
m Z = m A l 2 ( N O 3 ) 3 + m M g ( N O 3 ) 2 + m N H 4 N O 3 = 213.0,04 + 148.0,045 + 80 . 3 , 75 . 10 - 3 = 15 , 48
Đáp án D
Đúng 0
Bình luận (0)
Cho 2,16 gam hỗn hợp gồm Al và Mg tan hết trong dung dịch axit HNO3 loãng, đun nóng nhẹ tạo ra dung dịch X và 448 ml (đo ở 354,90K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỉ khối của Y so với oxi bằng 0,716 lần tỉ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi thu được 3,84 gam chất rắn T. Giá trị của m là: A. 15,18. B. 17,92. C. 16,68. D. 15,48.
Đọc tiếp
Cho 2,16 gam hỗn hợp gồm Al và Mg tan hết trong dung dịch axit HNO3 loãng, đun nóng nhẹ tạo ra dung dịch X và 448 ml (đo ở 354,90K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỉ khối của Y so với oxi bằng 0,716 lần tỉ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi thu được 3,84 gam chất rắn T. Giá trị của m là:
A. 15,18.
B. 17,92.
C. 16,68.
D. 15,48.
Cho 2,16 gam hỗn hợp gồm Al và Mg tan hết trong dung dịch axit HNO3 loăng, đun nóng nhẹ tạo ra dung dịch X và 448 ml ( đo ở 354,90 K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỷ khối của Y so với oxi bằng 0,716 lần tỷ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi được 3,84 gam chất rắn T. Giá trị của m là A. 15,48 B. 15,18 C. 17,92 D. 16,68.
Đọc tiếp
Cho 2,16 gam hỗn hợp gồm Al và Mg tan hết trong dung dịch axit HNO3 loăng, đun nóng nhẹ tạo ra dung dịch X và 448 ml ( đo ở 354,90 K và 988 mmHg) hỗn hợp khí Y khô gồm 2 khí không màu, không đổi màu trong không khí. Tỷ khối của Y so với oxi bằng 0,716 lần tỷ khối của khí cacbonic so với nitơ. Làm khan X một cách cẩn thận thu được m gam chất rắn Z, nung Z đến khối lượng không đổi được 3,84 gam chất rắn T.
Giá trị của m là
A. 15,48
B. 15,18
C. 17,92
D. 16,68.
Theo giả thiết, ta có Y gồm N2 và N2O
Dễ tính được số mol nN2 = nNO2 = 0,01 mol
=> Số mol e để tạo ra 2 khí này là 0,01.10 + 0,01.8 = 0,18 mol (I)
Gọi x và y là số mol của Al và Mg, ta có hệ:
27x + 24y = 2,16 và 102.x/2 + 40y = 3,84
=> x = 0,04, y = 0,045 => số mol e cho là 021 mol (II)
Từ I và II suy ra phải có NH4NO3, từ đây dễ dàng tính được
Hỗn hợp Z gồm: Al(NO3)3 với 8,52gam ; Mg(NO3)2 với 6,66 gam và ; NH4NO3 với 0,3 gam
=> tổng Z = 15,48gam.
=> Đáp án A
Đúng 0
Bình luận (0)
X, Y, Z là các hợp chất vô cơ của một kim loại, khi đốt nóng trong đèn khí ở nhiệt độ cao đều cho ngọn lửa màu vàng tươi. X tác dụng với Y thành Z. Nung nóng Y ở nhiệt độ cao thu được Z, hơi nước và khí E. Biết E là hợp chất của cacbon, E tác dụng với X cho Y hoặc Z. X, Y, Z, E lần lượt là các chất nào dưới đây? A. NaOH, Na2CO3, NaHCO3, CO2. B. NaOH, Na2CO3, CO2, NaHCO3. C. KOH. KHCO3, CO2, K2CO3. D. NaOH, NaHCO3, Na2CO3, CO2.
Đọc tiếp
X, Y, Z là các hợp chất vô cơ của một kim loại, khi đốt nóng trong đèn khí ở nhiệt độ cao đều cho ngọn lửa màu vàng tươi. X tác dụng với Y thành Z. Nung nóng Y ở nhiệt độ cao thu được Z, hơi nước và khí E. Biết E là hợp chất của cacbon, E tác dụng với X cho Y hoặc Z. X, Y, Z, E lần lượt là các chất nào dưới đây?
A. NaOH, Na2CO3, NaHCO3, CO2.
B. NaOH, Na2CO3, CO2, NaHCO3.
C. KOH. KHCO3, CO2, K2CO3.
D. NaOH, NaHCO3, Na2CO3, CO2.
Đáp án D
Khi đốt nóng trong đèn khí ở nhiệt độ cao đều cho ngọn lửa màu vàng tươi => hợp chất của Na
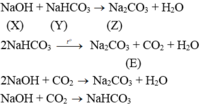
Đúng 0
Bình luận (0)
Chất vô cơ X trong thành phần chỉ có 2 nguyên tố. X không tan được vào H2O và dung dịch HCl. Đốt cháy X trong O2 ở nhiệt độ cao được khí Y. Khí Y tác dụng với dung dịch brom được chất Z. Z phản ứng với dung dịch BaCl2 thu được chất Q. Q không tan được vào dung dịch HNO3. Các chất X, Y, Z theo thứ tự tương ứng là: A. Fe3C, CO, BaCO3 B. CuS, H2S, H2SO4 C. CuS, SO2, H2SO4 D. MgS, SO2, H2SO4
Đọc tiếp
Chất vô cơ X trong thành phần chỉ có 2 nguyên tố. X không tan được vào H2O và dung dịch HCl. Đốt cháy X trong O2 ở nhiệt độ cao được khí Y. Khí Y tác dụng với dung dịch brom được chất Z. Z phản ứng với dung dịch BaCl2 thu được chất Q. Q không tan được vào dung dịch HNO3. Các chất X, Y, Z theo thứ tự tương ứng là:
A. Fe3C, CO, BaCO3
B. CuS, H2S, H2SO4
C. CuS, SO2, H2SO4
D. MgS, SO2, H2SO4
Đáp án C
X, Y, Z lần lượt là CuS, SO2, H2SO4. Phương trình phản ứng :
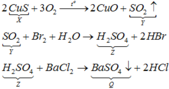
Đúng 0
Bình luận (0)