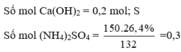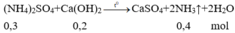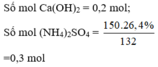B1: nhiệt phân m(g) KClO3 thu đcV(l) khí O2 (đktc) đủ để đốt cháy hết 4,48 l khí CH4 (đktc) .Tìm m ,V

Những câu hỏi liên quan
Cho 14,8 gam
Ca
OH
2
vào 150 gam dung dịch
NH
4
2
S
O
4
26,4% rồi đun nóng nhẹ thu được V lít khí (đktc). Để đốt cháy hết V lít khí trên cần vừa đủ lượng
O
2
thu được khi nung m gam
KClO
3
(có xúc tác). Giá tr...
Đọc tiếp
Cho 14,8 gam Ca OH 2 vào 150 gam dung dịch NH 4 2 S O 4 26,4% rồi đun nóng nhẹ thu được V lít khí (đktc). Để đốt cháy hết V lít khí trên cần vừa đủ lượng O 2 thu được khi nung m gam KClO 3 (có xúc tác). Giá trị của m là
A. 73,5.
B. 49.
C. 24,5.
D. 12,25.
: Khí metan(CH4) được dung làm nhiên liệu, khi đốt cháy trong không khí tỏa nhiều nhiệt. Tính thể tích O2 và thể tích không khí cần để đốt cháy hoàn toàn 4,48 lít khí CH4. Biết rằng thể tích các khí đo ở đktc
CH4 + 2O2 ---to--> CO2 + 2H2O
nCH4 = 4,48 : 22,4 = 0,2 (mol)
--> VO2 = 0,2 x 2 x 22,4 = 8,96 (l)
--> Vkk = 8,96 x 5 = 44,8 (l)
nhá
Cho 14,8 gam
C
a
O
H
2
vào 150 gam dung dịch
N
H
4
2
S
O
4
26,4% rồi đun nóng nhẹ thu được V lít (đktc) khí X (giả sử toàn bộ khí sinh ra thoát ra khí dung dịch). Để đốt cháy hết V lít khí X trên cần vừa đủ lượng...
Đọc tiếp
Cho 14,8 gam C a O H 2 vào 150 gam dung dịch N H 4 2 S O 4 26,4% rồi đun nóng nhẹ thu được V lít (đktc) khí X (giả sử toàn bộ khí sinh ra thoát ra khí dung dịch). Để đốt cháy hết V lít khí X trên cần vừa đủ lượng O 2 sinh ra khi nung m gam K C l O 3 (có xúc tác). Giá trị của m là
A. 24,5.
B. 49.
C. 36,75.
D. 12,25.
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy 5,6 l khí CH4 trong 8,72 l O2. Các khí đo ở đktc
a,Sau p/ứ , khí nào còn dư và dư mấy l(đã bt làm)
b,Tính thể tích CO2 thu đc Đktc\
c, Sau khi đốt đưa các khí về nhiệt độ 100 độ C. Tính thể tích hỗn hợp khí thu đc
Bài 1: Tính theo thể tích O2 cần dùng để đốt cháy hết 6,72 lít khí A(đktc)
Biết rằng:
- Khí A có tỉ khối đối với Hidro là 42
- Trong khí A có chứa 85,72% là C còn lại là Hidro
Bài 2: Phương trình phản ứng nhiệt phân KClO3:KClO3->KCl+O2
Nếu thu được 13,44 lít khí O2 thì cần dùng bao nhiêu gam KClO3?Tạo thành bao nhiêu gam KCl
Bài 1:
MA = 42.2 = 84 (g/mol)
\(m_C=\dfrac{84.85,72}{100}=72\left(g\right)=>n_C=\dfrac{72}{12}=6\left(mol\right)\)
\(m_H=84-72=12\left(g\right)=>n_H=\dfrac{12}{1}=12\left(mol\right)\)
=> A là C6H12
\(n_{C_6H_{12}}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(C_6H_{12}+6O_2\underrightarrow{t^o}6CO_2+6H_2O\)
______0,3----->1,8_______________________(mol)
=> \(V_{O_2}=1,8.22,4=40,32\left(l\right)\)
Bài 2
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
________0,4<-------------------------0,6___________(mol)
=> \(m_{KClO_3}=0,4.122,5=49\left(g\right)\)
Đúng 2
Bình luận (0)
Tính thể tích khí ôxy vừa đủ để đốt cháy hết:
a) 64 gam lưu huỳnh?
b) 4,48 lít khí metan (CH4)?
Cho biết các chất khí được đo ở đktc
`a)n_S=64/32=2(mol)`
`S + O_2` $\xrightarrow{t^o}$ `SO_2`
`2` `2` `(mol)`
`=>V_[O_2]=2.22,4=44,8(l)`
`b)n_[CH_4]=[4,48]/[22,4]=0,2(mol)`
`CH_4 + 2O_2` $\xrightarrow{t^o}$ `CO_2 + 2H_2 O`
`0,2` `0,4` `(mol)`
`=>V_[O_2]=0,4.22,4=8,96(l)`
Đúng 7
Bình luận (0)
m gam hỗn hợp gồm C3H6, C2H4 và C2H2 cháy hoàn toàn thu được 4,48 lít khí CO2 (đktc). Nếu hiđro hoá hoàn toàn m gam hỗn hợp trên rồi đốt cháy hết hỗn hợp thu được V(l) CO2 (đktc). Giá trị của V là: A. 3,36. B. 2,24. C. 4,48. D. 1,12.
Đọc tiếp
m gam hỗn hợp gồm C3H6, C2H4 và C2H2 cháy hoàn toàn thu được 4,48 lít khí CO2 (đktc). Nếu hiđro hoá hoàn toàn m gam hỗn hợp trên rồi đốt cháy hết hỗn hợp thu được V(l) CO2 (đktc). Giá trị của V là:
A. 3,36.
B. 2,24.
C. 4,48.
D. 1,12.
Hiđro hóa không làm thay đổi C trong hỗn hợp
Áp dụng định luật bảo toàn C ⇒ V = VCO2 khi đốt cháy hỗn hợp = 4,48
Đáp án C.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn V (l) hỗn hợp khí A gồm CO và H2 (ở đktc) cần vừa đủ 3,2 gam khí O2.
Mặt khác nếu dùng V(l) hỗn hợp khí A ở trên thì tác dụng vừa hết với a (g) Fe3O4 (ở nhiệt độ cao).
Tính giá trị V và a?
làm ơn giúp với