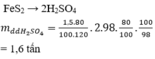từ 2,4 tấn quặng pirit sắt chứa 60% fes2.Điều chế được bao nhiêu lít dd h2so4 70%.(Ddd=1,8g/ml),biết H đạt 80%

Những câu hỏi liên quan
Từ 1 tấn quặng pirit sắt chứa 80% FeS2 có thể điều chế được bao nhiêu tấn H2SO4 60%. Biết rằng sự hao hụt trong sản phẩm là 5%
trong công nghiệp người ta điều chế H2SO4 từ quặng pirit sắt có thành phần chính là FeS2 theo sơ đồ sau FeS2->SO2->SO3->H2SO4.tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2 .Biết hiệu của cả quá trình là 80%
\(m_{FeS_2}=\dfrac{1.60}{100}=0,6\left(tấn\right)\)
=> \(m_{FeS_2\left(pư\right)}=\dfrac{0,6.80}{100}=0,48\left(tấn\right)\)
Cứ 1 mol FeS2 điều chế được 2 mol H2SO4
=> 120g FeS2 điều chế được 196g H2SO4
=> 0,48 tấn FeS2 điều chế được 0,784 tấn H2SO4
=> \(m_{ddH_2SO_4}=\dfrac{0,784.100}{98}=0,8\left(tấn\right)\)
Đúng 1
Bình luận (2)
\(m_{FeS_2}=0.6\left(tấn\right)=0.6\cdot10^3\left(kg\right)\)
\(n_{FeS_2}=\dfrac{0.6\cdot10^3}{120}=\dfrac{10^3}{200}\left(kmol\right)\)
Dựa vào sơ đồ phản ứng :
\(n_{H_2SO_4}=2n_{FeS_2}=2\cdot\dfrac{10^3}{200}=\dfrac{10^3}{100}=10\left(kmol\right)\)
\(m_{H_2SO_4\left(tt\right)}=10\cdot\dfrac{98}{80\%}=1225\left(kg\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{1225}{98\%}=1250\left(kg\right)=12.5\left(tấn\right)\)
Đúng 1
Bình luận (0)
Từ 1 tấn quặng pirit sắt chứa 80% FeS2 có thể điều chế được bao nhiêu tấn H2SO4 60%. Biết rằng sự hao hụt trong sản phẩm là 5%
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch
H
2
S
O
4
98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80%
F
e
S
2
(hiệu suất toàn quá trình là 80%) là A. 0,80 tấn B. 1,60 tấn C. 1,25 tấn D. 2,00 tấn
Đọc tiếp
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch H 2 S O 4 98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% F e S 2 (hiệu suất toàn quá trình là 80%) là
A. 0,80 tấn
B. 1,60 tấn
C. 1,25 tấn
D. 2,00 tấn
Từ 3 tấn quặng pirit sắt FeS2 (chứa 5% tạp chất) người ta điều chế được bao nhiêu tấn dung dịch H2SO4 98%. Biết hiệu suất của cả quá trình là 80%
ôi t làm nhầm....kq là
3,8 tấn ( cân bằng thêm 2 vào h2so4 là okok)
Đúng 0
Bình luận (2)
FeS2 ==> H2SO4
120g 98g
2,85( vì 5% tạp chất) 2,3275 (tấn)
vì H=80% ====> m H2SO4=1,3965( tấn). nhưng có C% H2SO4= 98%
VẬY mdd H2S04 là 1,425 tấn
Đúng 0
Bình luận (5)
Trong công nghiệp, axit sunfuric được điều chế từ quang pirit sắt. Khối lượng H2SO4 điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% FeS2 ( hiệu suất toàn quá trình là 80%) là:
A. 1,568 tấn
B. 1,96 tấn
C. 1,25 tấn
D. 2,00 tấn
Đáp án A.
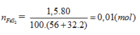
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
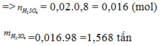
Đúng 0
Bình luận (0)
Từ 1 tấn quặng pirit sắt chứa 90% FeS2 có thể đ/c được bao nhiêu lít H2SO4 đặc 98% (D =1,84g/ml) có hiệu suất điều chế là 80%
m FeS2 = 0,9 tấn = 900 kg
4 FeS2 + 11 O2 -> 2 Fe2O3 + 8 SO2
2 SO2 + O2 -> 2 SO3
SO3 + H2O -> H2SO4
ta có 120 g FeS2 điều chế được 196 g H2SO4
=> 900 kg FeS2 điều chế được 1470 kg H2SO4
do H = 80% (Nếu là hiệu suất phản ứng ta phải tính hiệu suất điều chế = 80%. 80% . 80% = 51,2 %)
nên thực thế chỉ thu được 1470 . 80% = 1176 (kg) H2SO4
m dd H2SO4 = 1176 : 98% = 1200 (kg) = 1 200000 g
V dd H2SO4 = 1 200 000 : 1,84 = 652173 ml = 652 l
Đúng 0
Bình luận (1)
Cần bao nhiêu tấn quặng pirit sắt chứa 80% FeS2 để snar xuất 700 tấn dd H2SO4 70% biết rằng hao hụt trong sản xuất là 10%
Cần bao nhiêu tấn quặng pirit sắt chứa 80% FeS2 để snar xuất 700 tấn dd H2SO4 70% biết rằng hao hụt trong sản xuất là 10%
---
mH2SO4= 700. 70%= 490(tấn)
PTHH: 4 FeS2 + 11 O2 -to,xt-> 2 Fe2O3 + 8 SO2
300_________________________________320(TẤN)
SO2+ 1/2 O2 -to-> SO3
320____________400(TẤN)
SO3 + H2O -> H2SO4
400_________490(TẤN)
mFeS2(LT)= 300(tấn)
-> mFeS2(TT)= (300.100)/90=1000/3 (tấn) (Do dư 10%)
=> m(quặng)= mFeS2(TT)/ 80% = 1000/3 : 80% \(\approx416,7\left(tấn\right)\)
Đúng 0
Bình luận (0)
Câu 1. Dùng 100 tấn quặng pirit sắt chứa 72% FeS2 để điều chế H2SO4. Cho toàn bộ axit thu được tác dụng vs Cu điều chế CuSO4.5H2O sau đó pha thành dd CuSO4 để trừ nấm thực vật. Tính m (tấn) CuSO4.5H2O thu được. biết hiệu suất cả quá trình là 80%.