Từ 1 tấn quặng Lưu huỳnh có 2% tạp chất cho người ta có thể sản xuất bao nhiêu tấn dung dịch h2so4 98% với hiệu suất chung của quá trình sản suất là 80%

Những câu hỏi liên quan
.Từ 1 tấn lưu quỳnh có 2% tập chất trơ người ta có thể sản xuất bao nhiêu tấn dung dịch H2SO4 98% với hiệu suất của quá tình sản xuất là 98%
\(m_S=1000\cdot98\%=980\left(kg\right)\)
\(n_S=\dfrac{980}{32}=30.625\left(kmol\right)\)
\(S\rightarrow SO_2\rightarrow SO_3\rightarrow H_2SO_4\)
\(30.625.........................30.625\)
\(m_{dd_{H_2SO_4}}=\dfrac{30.625\cdot98}{98\%}=3062.5\left(kg\right)\)
\(m_{dd_{H_2SO_4\left(tt\right)}}=3062.5\cdot98\%=3001.25\left(kg\right)\)
Đúng 2
Bình luận (1)
Từ 1,2 tấn quặng pillit sắt (FeS2) có thể sản xuất được bao nhiêu tấn dung dịch H2SO4 50%, biết hiệu suất của quá trình sản xuất là 80%.
Đổi 1,2 tấn = 1200 kg
Ta có: \(n_{FeS_2}=\dfrac{1200}{120}=10\left(kmol\right)\)
Bảo toàn Lưu huỳnh: \(n_{H_2SO_4\left(lý.thuyết\right)}=2n_{FeS_2}=20\left(kmol\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(thực\right)}=\dfrac{20\cdot98}{50\%}\cdot80\%=3136\left(kg\right)=3,136\left(tấn\right)\)
Đúng 0
Bình luận (1)
Từ 3 tấn quặng pirit sắt FeS2 (chứa 5% tạp chất) người ta điều chế được bao nhiêu tấn dung dịch H2SO4 98%. Biết hiệu suất của cả quá trình là 80%
ôi t làm nhầm....kq là
3,8 tấn ( cân bằng thêm 2 vào h2so4 là okok)
Đúng 0
Bình luận (2)
FeS2 ==> H2SO4
120g 98g
2,85( vì 5% tạp chất) 2,3275 (tấn)
vì H=80% ====> m H2SO4=1,3965( tấn). nhưng có C% H2SO4= 98%
VẬY mdd H2S04 là 1,425 tấn
Đúng 0
Bình luận (5)
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2
→
SO2
→
SO3
→
H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là: A. 40% B. 60% C. 80% D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là:
A. 40%
B. 60%
C. 80%
D. 62,5%
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4. Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là: A. 40%. B. 60%. C. 80%. D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4.
Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là:
A. 40%.
B. 60%.
C. 80%.
D. 62,5%
Đáp án C.
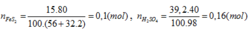
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Đúng 0
Bình luận (0)
Từ 80 tấn quặng pirit chứa 40% lưu huỳnh, người ta sản xuất được 73,5 tấn axit sunfuric. Tính hiệu suất của quá trình sản xuất axit sunfuric.
Khối lượng lưu huỳnh chứa trong 80 tấn quặng:
m S = 80x40/100 = 32 tấn
Điều chế H 2 SO 4 theo sơ đồ sau
S → SO 2 → SO 3 → H 2 SO 4
Ta thấy: Cứ 32g S thì sản xuất được 98g H 2 SO 4
⇒ m H 2 SO 4 = 32x98/32 = 98 tấn
Hiệu ứng phản ứng: H = 73,5/98 x 100 = 75%
Đúng 0
Bình luận (0)
Từ 800 tấn quặng pirit sắt chứa 25% tạp chất trơ có thể sản xuất được a
m
3
dung dịch
H
2
S
O
4
93
%
D
1
,
83
g
/
c...
Đọc tiếp
Từ 800 tấn quặng pirit sắt chứa 25% tạp chất trơ có thể sản xuất được a m 3 dung dịch H 2 S O 4 93 % D = 1 , 83 g / c m 3 , hiệu suất quá trình là 95%. Giá trị của a là
A. 547
B. 800
C. 1200
D. 547000
Từ 1 tấn tinh bột chứa 20% tạp chất trơ có thể sản xuất được bao nhiêu kg glucozơ nếu hiệu suất của quá trình sản xuất là 80% ?
A. 1777 kg
B. 711 kg
C. 666 kg
D. 71 kg
Câu 1 : Một loại quặng pyrite sắt chứa 80% FeS2 nguyên chất. Tính khối lượng dung dịch H2SO4 98% được sản xuất từ 4,5 tấn quặng trên. Biết hiệu suất của cả quá trình là 90%.
Câu 2 : Từ 200 tấn lưu huỳnh lấy từ mỏ có lẫn 20% tạp chất, điều chế được bao nhiêu tấn axit H2SO4 ? Biết hiệu suất của cả quá trình là 75%.
Các bạn giúp mình nha. Cảm ơn ạ
quá trình sản xuất
FeS2-----> 2SO2------>2SO3--------->2H2SO4 (bảo toàn nguyên tố S )
120 196
4,5.80/100 ------------> x tấn H2SO4
====> x=2,88 tấn
H=90/100 ===> mH2SO4=90/100. 2,88=2,592 tấn
===> mđH2SO4= 2,592/98/100=2,65 tấn
Đúng 0
Bình luận (0)
















