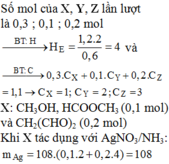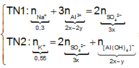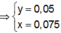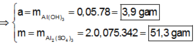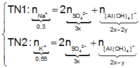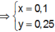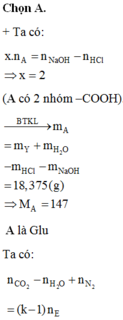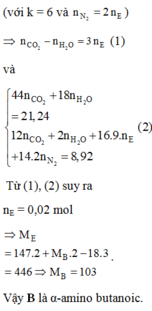Cho 8g SO3 tác dụng hết với 92ml H2O thu được dung dịch A. Cho 6,2g Na2O hòa tan hết vào 93,8 ml H2O thu được dung dịch B. (khối lượng riêng của H2O là 1g/ml). Trộn nửa dung dịch A với nửa dung dịch B thu được 100ml dung dịch C.
a) Tính C% của dung dịch A và dung dịch B
b) Tính CM của dung dịch C.