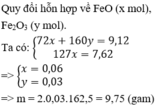Đốt cháy fe trong oxi thu được 9,12 g hỗn hợp X gồm feo fe2o3 fe3o4 .Cho X tác dụng với hcl dư thu được 7,62g fecl2 .Thể tích 02 phản ứng ?

Những câu hỏi liên quan
Cho 9,12 gam hỗn hợp gồm
F
e
O
,
F
e
2
O
3
,
F
e
3
O
4
tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Cô cạn Y thu được 7,62 gam
F
e
C
l
2
và m gam
F...
Đọc tiếp
Cho 9,12 gam hỗn hợp gồm F e O , F e 2 O 3 , F e 3 O 4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Cô cạn Y thu được 7,62 gam F e C l 2 và m gam F e C l 3 . Giá trị của m là
A. 7,80
B. 8,75
C. 6,50
D. 9,75
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là A. 9,75 B. 8,75 C. 7,80 D. 6,50
Đọc tiếp
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là
A. 9,75
B. 8,75
C. 7,80
D. 6,50
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y ; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là A. 6,50. B. 7,80. C. 9,75. D. 8,75.
Đọc tiếp
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y ; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là
A. 6,50.
B. 7,80.
C. 9,75.
D. 8,75.
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là A. 6,50. B. 7,80. C. 9,75. D. 8,75.
Đọc tiếp
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là
A. 6,50.
B. 7,80.
C. 9,75.
D. 8,75.
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là A. 6,50. B. 7,80. C. 9,75. D. 8,75.
Đọc tiếp
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, được dung dịch Y; cô cạn Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là
A. 6,50.
B. 7,80.
C. 9,75.
D. 8,75.
16. Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HCl dư. Sau phản ứng xảy ra hoàn toàn, được dung dịch A; cô cạn dung dịch A thu được 7,62 gam FeCl2 và m gam FeCl3. Tính giá trị của m.
Quy đổi Fe3O4 thành FeO, Fe2O3
\(n_{FeCl_2}=\dfrac{7,62}{127}=0,06\left(mol\right)\)
PTHH: FeO + 2HCl --> FeCl2 + H2O
0,06<------------0,06
=> \(n_{Fe_2O_3}=\dfrac{9,12-0,06.72}{160}=0,03\left(mol\right)\)
PTHH: Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
0,03-------------->0,06
=> \(m_{FeCl_3}=0,06.162,5=9,75\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 9,12 gam hỗn hợp gồm FeO Fe2O3 Fe3O4 tác dụng với dung dịch HCl dư sau khi các phản ứng xảy ra hoàn toàn được dung dịch Y Cô cạn dung dịch Y thu được 7,62 gam FeCl2 và m gam FeCl3 giá trị của m là
Xem chi tiết
FeO + 2HCl => FeCl2 + H2O
Fe2O3 + 6HCl => 2FeCl3 + 3H2O
Quy đổi hỗn hợp chỉ gồm : FeO , Fe2O3
nFeCl2 = 7.62/127 = 0.06 (mol)
=> nFeO = nFeCl2 = 0.06 (mol)
mFeO = 0.06*72 = 4.32 (g)
mFe2O3 = 9.12 - 4.32 = 4.8 (g)
nFe2O3 = 4.8/160 = 0.03 (mol)
nFeCl3 = 2nFe2O3 = 0.06 (mol)
mFeCl3 = 0.06*162.5 = 9.75 (g)
Đúng 2
Bình luận (0)
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HC1 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Cô cạn dung dịch Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là A. 9,75 B. 8,75 C. 7,80 D. 6,50
Đọc tiếp
Cho 9,12 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 tác dụng với dung dịch HC1 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Cô cạn dung dịch Y thu được 7,62 gam FeCl2 và m gam FeCl3. Giá trị của m là
A. 9,75
B. 8,75
C. 7,80
D. 6,50
Đốt cháy 8,6(g) bột Fe trong bình chứa Oxi thu được 7,36g hỗn hợp a gồm Fe2O3, Fe3O4, FeO, Fe cho A tác dụng với HNO3 dư thu được V lít hỗn hợp B gồm NO, NO2 tỉ khối của V so với H2=19. Tính V ở điều kiện chuẩn.
Mong mọi người giải chi tiết. Cảm ơn!!
Bạn xem lại đề: 8,6 g Fe sao đốt ra chỉ thu được 7,36 g hỗn hợp
Đúng 0
Bình luận (1)