Đốt 1 lượng nhôm(Al) trong 6,72 lít O2. Chất rắn thu được sau phản ứng cho hoà tan hoàn toàn vào dung dịch HCl thấy bay ra 6,72 lít H2 (các thể tích khí đo ở đkc). Khối lượng nhôm đã dùng là ?

Những câu hỏi liên quan
Đốt một lượng nhôm (Al) trong 6,72 lít O2. Chất rắn thu được sau phản ứng cho hoà tan hoàn toàn vào dung dịch HCl thấy bay ra 6,72 lít H2 (các thể tích khí đo ở đktc). Khối lượng nhôm đã dùng là: A. 8,1 gam. B. 16,2 gam. C. 18,4 gam. D. 24,3 gam.
Đọc tiếp
Đốt một lượng nhôm (Al) trong 6,72 lít O2. Chất rắn thu được sau phản ứng cho hoà tan hoàn toàn vào dung dịch HCl thấy bay ra 6,72 lít H2 (các thể tích khí đo ở đktc). Khối lượng nhôm đã dùng là:
A. 8,1 gam.
B. 16,2 gam.
C. 18,4 gam.
D. 24,3 gam.
Đốt một lượng nhôm trong 6,72 lít O2(đktc). Sau khi kết thúc phản ứng cho chất rắn thu đc hoà ta hoàn toàn vào dd H2SO4 loãng dư , thấy giải phóng ra 6,72lit H2(đktc) .Khối lượng nhôm đã dùng là:
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
0,4 0,3 0,2 ( mol )
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\) ( không giải phóng H2)
=> Chất rắn tạo ra H2 là Al
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 ( mol )
\(\Rightarrow m_{Al}=\left(0,2.27\right)+\left(0,4.27\right)=16,2g\)
Đúng 2
Bình luận (0)
Một hỗn hợp gồm Al và Fe2O3, thực hiện phản ứng nhiệt nhôm ở nơi không có không khí. Hỗn hợp sản phẩm rắn thu được sau phản ứng trộn đều rồi chia thành hai phần. Cho phần 1 vào dung dịch NaOH lấy dư thì thu được 6,72 lít hiđro và chất rắn không tan trong NaOH có khối lượng bằng 34,783% khối lượng của phần 1. Hòa tan hết phần 2 vào dung dịch HCl thì thu được 26,88 lít hiđro (các thể tích ở đktc), các phản ứng đều hoàn toàn. Khối lượng từng chất rắn trong hỗn hợp ban đầu là: A. 10,8 gam Al; 64,0 g...
Đọc tiếp
Một hỗn hợp gồm Al và Fe2O3, thực hiện phản ứng nhiệt nhôm ở nơi không có không khí. Hỗn hợp sản phẩm rắn thu được sau phản ứng trộn đều rồi chia thành hai phần. Cho phần 1 vào dung dịch NaOH lấy dư thì thu được 6,72 lít hiđro và chất rắn không tan trong NaOH có khối lượng bằng 34,783% khối lượng của phần 1. Hòa tan hết phần 2 vào dung dịch HCl thì thu được 26,88 lít hiđro (các thể tích ở đktc), các phản ứng đều hoàn toàn. Khối lượng từng chất rắn trong hỗn hợp ban đầu là:
A. 10,8 gam Al; 64,0 gam Fe2O3.
B. 27,0 gam Al; 32,0 gam Fe2O3.
C. 32,4 gam Al; 32,0 gam Fe2O3.
D. 45,0 gam Al; 80,0 gam Fe2O3.
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là A. 112 B. 84 C. 168 D. 56
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là
A. 112
B. 84
C. 168
D. 56
Đáp án A
Hỗn hợp rắn gồm Al, Al2O3, Fe với n Fe = 2 n Al 2 O 3 . Chia thành 2 phần không bằng nhau:
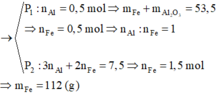
Đúng 0
Bình luận (0)
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là A. 112. B. 84. C. 168. D. 56.
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là
A. 112.
B. 84.
C. 168.
D. 56.
Một hỗn hợp X gồm Al và
Fe
2
O
3
. Thực hiện phản ứng nhiệt nhôm hoàn toàn X thu được chất rắn A. A tác dụng với dung dịch NaOH dư thu được 6,72 lít
H
2
(đktc) và chất rắn B. Cho B tác dụng với
H
2
SO
4
loãng dư sinh ra 6,72 lít khí (đktc). Khối lượng hỗn hợp X đã dùng là A. 29,50 gam B. 45,50 ga...
Đọc tiếp
Một hỗn hợp X gồm Al và Fe 2 O 3 . Thực hiện phản ứng nhiệt nhôm hoàn toàn X thu được chất rắn A. A tác dụng với dung dịch NaOH dư thu được 6,72 lít H 2 (đktc) và chất rắn B. Cho B tác dụng với H 2 SO 4 loãng dư sinh ra 6,72 lít khí (đktc). Khối lượng hỗn hợp X đã dùng là
A. 29,50 gam
B. 45,50 gam
C. 37,5 gam
D. 26,80 gam
Hòa tan hoàn toàn Al bằng dung dịch HCl vừa đủ, thu được 6,72 lít khí(đktc). Khối lượng nhôm đã tham gia phản ứng là
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(\Rightarrow n_{Al}=0,2\left(mol\right)\) \(\Rightarrow m_{Al}=0,2\cdot27=5,4\left(g\right)\)
Đúng 3
Bình luận (0)
\(n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ n_{Al} = \dfrac{2}{3}n_{H_2} = 0,2(mol)\\ \Rightarrow m_{Al} =0,2.27 = 5,4\ gam\)
Đúng 2
Bình luận (0)
Tiến hành phản ứng nhiệt nhôm 20,4 gam hỗn hợp Al, Fe3O4 (tỉ lệ số mol 4:1), sau một thời gian thu được hỗn hợp rắn X. Hoà tan hoàn tan X trong dung dịch HCl loãng, dư thu được 7,616 lít H2 và dung dịch Y. Cho dung dịch AgNO3 dư vào Y, thấy thoát ra V ml khí NO và 184,51 gam kết tủa. Biết các phản ứng xảy ra trong môi trường khí trơ và thể tích các khí được đo ở đktc. Giá trị của V gần nhất vớ A. 450 B. 550 C. 650 D. 750
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm 20,4 gam hỗn hợp Al, Fe3O4 (tỉ lệ số mol 4:1), sau một thời gian thu được hỗn hợp rắn X. Hoà tan hoàn tan X trong dung dịch HCl loãng, dư thu được 7,616 lít H2 và dung dịch Y. Cho dung dịch AgNO3 dư vào Y, thấy thoát ra V ml khí NO và 184,51 gam kết tủa. Biết các phản ứng xảy ra trong môi trường khí trơ và thể tích các khí được đo ở đktc. Giá trị của V gần nhất vớ
A. 450
B. 550
C. 650
D. 750
Chọn đáp án C.
Từ tỉ lệ nAl: nFe3O4 = 4 : 1 => Đặt nAl = 4x và nFe3O4 = x => 27×4x + 232x = 20,4 => x = 0,06
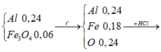

Đặt nNO = x => nHCl dư trong Y = 4x
nHCl phản ứng = 2×0,24 + 2×0,34 = 1,16 => nAgCl = 1,16 + 4x
BTE => 0,24×3 + 0,06 = 2×0,34 + 3x + nAg => nAg = 0,1 - 3x
=> 184,51 = 143,5×(l,16 + 4x) + 108×(0,l - 3x) =>x = 0,029
Vậy V = 1000×0,029×22,4 = 649,6.
Đúng 0
Bình luận (0)
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp thu được sau phản ứng (đã trộn đều) thành 2 phần không bằng nhau. Phần 2 có khối lượng nhiều hơn phần 1 là 134 gam. Cho phần 1 tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít khí H2 bay ra. Hòa tan phần 2 bằng lượng dư dung dịch H2SO4 loãng thấy có 84 lít khí H2 bay ra. Các phản ứng đều xảy ra với hiệu suất 100%. Các khí đo ở đktc. Khối lượng Fe tạo thành trong phản ứng nhiệt nhôm gần nhất là A. 186,0...
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp thu được sau phản ứng (đã trộn đều) thành 2 phần không bằng nhau. Phần 2 có khối lượng nhiều hơn phần 1 là 134 gam. Cho phần 1 tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít khí H2 bay ra. Hòa tan phần 2 bằng lượng dư dung dịch H2SO4 loãng thấy có 84 lít khí H2 bay ra. Các phản ứng đều xảy ra với hiệu suất 100%. Các khí đo ở đktc. Khối lượng Fe tạo thành trong phản ứng nhiệt nhôm gần nhất là
A. 186,0 gam.
B. 112,0 gam.
C. 192,2 gam.
D. 117,6 gam.
Đáp án B
![]()
· Phần 1 + NaOH → 0,75 mol H2
=> Al dư, Fe2O3 phản ứng hết.
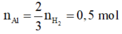
· Đặt số mol Fe, A l 2 O 3 trong phần 1 lần lượt là 2x, x.
Giả sử phần 2 có khối lượng gấp k lần phần 1.
![]() (1)
(1)
Phần 2:
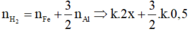
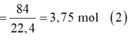
· Từ (1) và (2) suy ra:
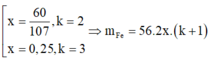
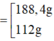
Kết hợp đáp án suy ra m F e = 112 g
Đúng 0
Bình luận (0)














