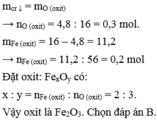Chất không khử được sắt oxit (ở nhiệt độ cao) là ?

Những câu hỏi liên quan
Chất nào sau đây không khử được sắt oxit ở nhiệt độ cao?
A. H2
B. Cu
C. CO
D. Al
Chất nào sau đây không khử được sắt (III) oxit (ở nhiệt độ cao)? A. CO2 B. Al C. CO D. H2
Đọc tiếp
Chất nào sau đây không khử được sắt (III) oxit (ở nhiệt độ cao)?
A. CO2
B. Al
C. CO
D. H2
Đáp án A
CO2 không khử được Fe(III) oxit ở nhiệt độ cao; Al, CO, H2 đều khử được sắt(III) oxit ở nhiệt độ cao tạo thành sắt và các sản phẩm tương ứng
Đúng 0
Bình luận (0)
Hai chất đều không khử được sắt oxit (ở nhiêt độ cao) là
A. Al, Cu
B. Al, CO
C. CO2, Cu
D. H2, C
Khử hoàn toàn 16g bột oxit sắt nguyên chất bằng CO ở nhiệt độ cao. Sau khi phản ứng kết thúc, khối lượng chất rắn giảm 4,8g. Oxit sắt đã dùng là A.
F
e
2
O
B.
F
e
2
O
3
C. FeO D.
F
e
3
O
4
Đọc tiếp
Khử hoàn toàn 16g bột oxit sắt nguyên chất bằng CO ở nhiệt độ cao. Sau khi phản ứng kết thúc, khối lượng chất rắn giảm 4,8g. Oxit sắt đã dùng là
A. F e 2 O
B. F e 2 O 3
C. FeO
D. F e 3 O 4
Người ta điều chế sắt bằng cách dùng Hidro khử sắt(lll) oxit ở nhiệt độ cao a.Tính thể tích H2 cần dùng để khử 16 sắt(lll) oxit nguyên liệu? b.Đem đốt hoàn toàn lượng sắt thu được trong lọ đựng 2,24 lít khí Oxi (ở DKTC). Chất nào dư,dư bao nhiêu gam? [GIÚP MÌNH VỚI Ạ MAI KIỂM TRA RỒI]
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1 0,3 0,2
\(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
LTL: \(\dfrac{0,2}{3}>\dfrac{0,1}{2}\rightarrow\) Fe dư
Theo pthh: \(n_{Fe\left(pư\right)}=\dfrac{3}{2}n_{O_2}=\dfrac{3}{2}.0,1=0,15\left(mol\right)\)
\(\rightarrow m_{Fe\left(dư\right)}=\left(0,2-0,15\right).56=2,8\left(g\right)\)
Đúng 3
Bình luận (2)
a.\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,1 0,3 0,2 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_{O_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(\dfrac{0,2}{3}\) > \(\dfrac{0,1}{2}\) ( mol )
0,15 0,1 ( mol )
Chất dư là Fe
\(m_{Fe\left(dư\right)}=\left(0,2-0,15\right).56=2,8g\)
Đúng 2
Bình luận (1)
Fe2O3+3H2-to>2Fe+3H2O
0,1--------0,3------0,2
n Fe2O3=0,1 mol
=>VH2=0,3.22,4=6,72l
b)
3Fe+2O2-to>Fe3O4
0,15---0,1
n O2=0,1 mol
=>Fe dư :
=>m Fe du =0,05.56=2,8g
Đúng 2
Bình luận (1)
Xem thêm câu trả lời
Khử hoàn toàn 16 gam bột oxit sắt bằng CO ở nhiệt độ cao, sau khi phản ứng kết thúc, khối lượng chất rắn giảm 4,8 gam. Công thức oxit sắt đã dùng là:
A. FeO
B. Fe3O4
C. Fe2O3
D. Tất cả đều sai.
Đáp án C
Phản ứng của oxit + CO thực chất là:
CO + [O] → CO2
=> mchất rắn giảm = mO pứ = 4,8g => nO = 4,8 : 16 = 0,3 mol
=> mFe = mOxit – mO = 16 – 4,8 = 11,2 => nFe = 11,2 : 56 = 0,2 mol
=> nFe : nO = 0,2 : 0,3 = 2 : 3
=> Oxit là Fe2O3
Đúng 0
Bình luận (0)
Khử hoàn toàn 1,6 g sắt (III) oxit ở nhiệt độ cao bằng khí Hidro
a. Viết PTHH xảy ra. Tính thể tích chất khí đã dùng ở đktc
b. Tính m của sắt thu được
\(m_{Fe}=\dfrac{1,6}{160}=0,01\left(mol\right)\\ pthh:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,01 0,03 0,02
=> \(V_{H_2}=0,03.22,4=0,672\left(l\right)\\
m_{Fe}=0,02.56=1,12\left(g\right)\)
Đúng 1
Bình luận (1)
\(n_{Fe_2O_3}=\dfrac{1,6}{160}=0,01\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,01---->0,03------->0,02
\(\rightarrow\left\{{}\begin{matrix}a,V_{H_2}=0,03.22,4=0,672\left(l\right)\\b,m_{Fe}=0,02.56=1,12\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
8, Khử oxit sắt từ ( Fe3O4 ) bằng khí hidro ở nhiệt độ cao thu được 30,24g sắt. Tính khối lượng oxit sắt từ cần dùng
\(PTHH:Fe_3O_4+4H_2\rightarrow^{t^o}3Fe+4H_2O\\ n_{Fe}=\dfrac{30,24}{56}=0,54\left(mol\right)\\ \Rightarrow n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,18\left(mol\right)\\ \Rightarrow m_{Fe_3O_4}=0,18\cdot232=41,76\left(g\right)\)
Đúng 3
Bình luận (0)
khử hoàn toàn 16g một oxit sắt nguyên chất bằng khí CO ở nhiệt độ cao. Sau đó dẫn toàn bộ khí thu được qua bình đựng nước vôi trong dư, kết thúc phản ứng thu được 10g kết tủa. Xác định công thức oxit sắt