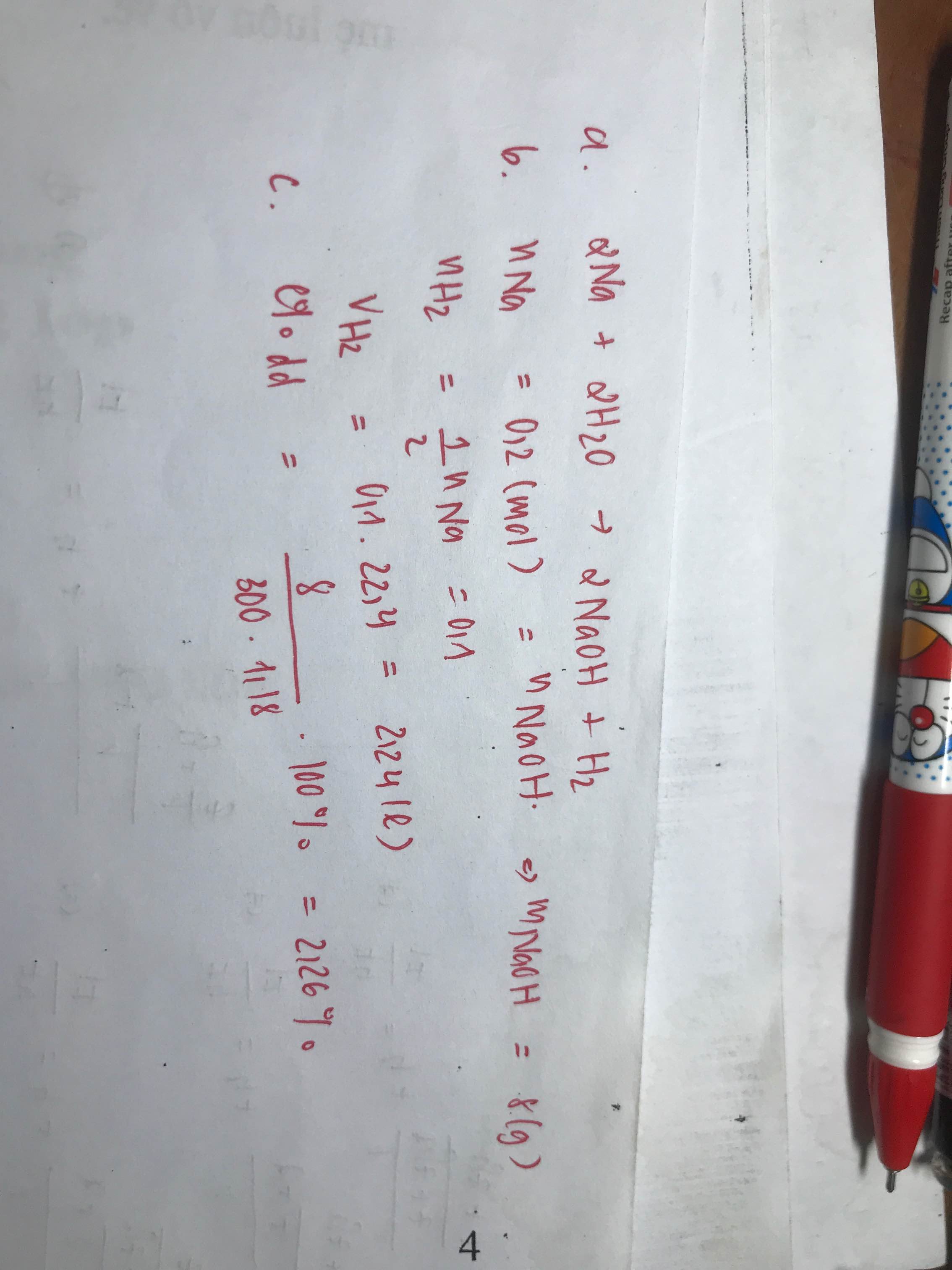Cho 4,6g Na vào 90g nước lấy dư,sau phản ứng hoàn toàn,viết phương trình hóa học của phản ứng và tính nồng độ phần trăm C% của dung dịch thu đc

Những câu hỏi liên quan
hòa tan 4,6g Na vào cốc chứa 54g nước
a, viết phương trình hóa học,dd thu dc là dd gì
b,hãy tính nồng độ phần trăm của dd sau phản ứng
a)
Na + H2O → NaOH + 1/2H2
Dung dịch thu được là dung dịch NaOH
b)
nNa = 4,6 : 23 = 0,2 mol
nH2O = 54 : 18 = 3 mol
=> Na phản ứng hết, nNaOH = nNa = 0,2 mol
<=> mNaOH = 0,2.40 = 8 gam
m dung dịch sau phản ứng = mNa + mH2O - mH2 = 4,6 + 54 - 0,1.2 = 58,4 gam
C% NaOH = \(\dfrac{8}{58,4}.100\)% = 13,7 %
Đúng 1
Bình luận (0)
BÀI TẬP TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC Bài 1: Cho 4,6 gam Na vào nước dư, sau phản ứng thu được V lít khí H2 (đktc) và 500ml dung dịch NaOH. Tìm V Xác định nồng độ mol của dung dịch naOH sau phản ứng Bài 2: Hòa tan hoàn toàn 35 gam CaCO3 bằng 300ml dung dịch HCl. Tìm thể tích khí thoát ra ở đktc. Xác định nồng độ mol của dung dịch axit HCl đã dùng. Bài 3: Cho m gam Fe vào 500 ml dung dịch HCl 0,5M sau phản ứng thu được dung dịch X. Để trung hòa dung dịch X cần vừa đủ 50 ml dung dịch KOH 1M. Tín...
Đọc tiếp
BÀI TẬP TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC
Bài 1: Cho 4,6 gam Na vào nước dư, sau phản ứng thu được V lít khí H2 (đktc) và 500ml dung dịch NaOH.
Tìm V
Xác định nồng độ mol của dung dịch naOH sau phản ứng
Bài 2: Hòa tan hoàn toàn 35 gam CaCO3 bằng 300ml dung dịch HCl.
Tìm thể tích khí thoát ra ở đktc.
Xác định nồng độ mol của dung dịch axit HCl đã dùng.
Bài 3: Cho m gam Fe vào 500 ml dung dịch HCl 0,5M sau phản ứng thu được dung dịch X. Để trung hòa dung dịch X cần vừa đủ 50 ml dung dịch KOH 1M. Tính giá trị của m?
Bài 4: Cho 150 ml dung dịch NaOH 0,5M vào 150 ml dung dịch HCl 1M
a. Nếu cho giấy quỳ tím vào dung dịch sau phản ứng thì màu của giấy quỳ tím thay đổi như thế nào? Tại sao?
b. Tính khối lượng muối tạo thành sau phản ứng?
c. Tính nồng độ mol các chất tan trong dung dịch sau phản ứng?
Bài 5: Cho 100 gam dung dịch BaCl2 20,8% vào 150 gam dung dịch Na2SO4 14,2% thu được dung dịch X và m gam kết tủa.
a. Tính khối lượng kết tủa. b. Tính C% của các chất tan trong dung dịch X.
Bài 6: Cho 250 gam dung dịch CuCl2 13,5% tác dụng với 200 gam dung dịch KOH 11,2%
a. Tính khối lượng kết tủa tạo thành.
b. Tính C% của các chất trong dung dịch sau phản ứng?
Bài 7: Cho 200 ml dung dịch H2SO4 1M tác dụng với 6,5 gam kẽm. Tính thể tích khí thu được và khối lượng các chất thu được trong dung dịch sau phản ứng?
Bài 8: Cho 12,4 gam oxit của kim loại hóa trị I vào nước thu được 200 ml dung dịch bazơ có nồng độ 2M. Hãy xác định công thức của oxit trên.
Bài 9: Hòa tan hoàn toàn 8,4 gam một kim loại hóa trị II cần dùng 150 ml dung dịch HCl 2M. Tìm tên kim loại trên.
Bài 10: Hòa tan hoàn toàn 3,2 gam một oxit của một kim loại hóa trị III cần dùng vừa đủ 60 gam dung dịch H2SO4 9,8%. Tìm công thức của oxit trên.
Bài 3:
nKOH = 1.0,05 = 0,05 (mol);nHCl=0,5.0,5=0,25 (mol)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,0125 0,0125
PTHH: 2KOH + FeCl2 → 2KCl + Fe(OH)2
Mol: 0,05 0,025
Ta có:\(\dfrac{0,25}{2}>\dfrac{0,0125}{1}\) ⇒ HCl dư, FeCl3 pứ hết
⇒ m=0,0125.56 = 0,7 (g)
Đúng 2
Bình luận (1)
Bài 4:
a,Nếu cho giấy quỳ tím vào dung dịch sau phản ứng thì màu của giấy quỳ tím sẽ không thay đổi màu sắc
b,\(n_{NaOH}=0,5.0,15=0,075\left(mol\right);n_{HCl}=1.0,15=0,15\left(mol\right)\)
PTHH: NaOH + HCl → NaCl + H2O
Mol: 0,075 0,075 0,075
Ta có:\(\dfrac{0,075}{1}< \dfrac{0,15}{1}\) ⇒ NaOH pứ hết , HCl dư
mNaCl = 0,075.58,5 = 4,3875 (g)
c, Vdd sau pứ = 0,15 + 0,15 = 0,3 (l)
\(C_{M_{ddNaCl}}=\dfrac{0,075}{0,3}=0,25M;C_{M_{ddHCldư}}=\dfrac{0,15-0,075}{0,3}=0,25M\)
Bài 5:
a,\(n_{BaCl_2}=\dfrac{100.20,8\%}{208}=0,1\left(mol\right);n_{Na_2SO_4}=\dfrac{150.14,2\%}{142}=0,15\left(mol\right)\)
PTHH: BaCl2 + Na2SO4 → BaSO4 + 2NaCl
Mol: 0,1 0,1 0,1
Ta có: \(\dfrac{0,1}{1}< \dfrac{0,15}{1}\)⇒ BaCl2 pứ hết, Na2SO4 dư
\(\Rightarrow m_{BaSO_4}=0,1.233=23,3\left(g\right)\)
b,mdd sau pứ = 100+150 = 250 (g)
\(C\%_{ddNaCl}=\dfrac{0,2.58,5.100\%}{250}=4,68\%\)
\(C\%_{ddNa_2SO_4dư}=\dfrac{\left(0,15-0,1\right).142.100\%}{250}=2,84\%\)
Đúng 3
Bình luận (0)
Bài 2:
a,\(n_{CaCO_3}=\dfrac{35}{100}=0,35\left(mol\right)\)
PTHH: CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Mol: 0,35 0,7 0,35
\(\Rightarrow V_{CO_2}=0,35.22,4=7,84\left(l\right)\)
b,\(C_{M_{ddHCl}}=\dfrac{0,7}{0,5}=1,4M\)
Đúng 1
Bình luận (1)
Cho 2,3 gam Na vào 100g nước thu được dung dịch A.
1)Viết phương trình hóa học
2)Tính khối lượng sản phẩm
3)Tính nồng độ phần trăm dung dịch sau phản ứng
\(1)2Na+2H_2O\rightarrow2NaOH+H_2\\ 2)n_{Na}=\dfrac{2,3}{23}=0,1mol\\ 2Na+2H_2O\rightarrow2NaOH+H_2\)
0,1 0,1 0,1 0,05
\(m_{NaOH}=0,1.40=4g\\ m_{H_2}=0,05.2=0,1g\\ c)C_{\%NaOH}=\dfrac{4}{2,3+100-0,1}\cdot100=3,91\%\)
Đúng 3
Bình luận (0)
đốt cháy hoàn toàn 6,2 gam photpho trong oxi dư . cho sản phẩm tạo thành tác dụng vừa đủ với dung dịch NaOH 32% tạo ra muối Na2HPO4 .
a) viết phương trình hóa học của các phản ứng xảy ra .
b) tính khối lượng dung dịch NaOH đã dùng .
c) tính nồng độ phần trăm của muối trong dung dịch thu được sau phản ứng .
a, (1) 4P+5.O2->2.P2O5
(2) P2O5+4.NaOH->2.Na2HPO4+H2O
b, photpho có n=6,2:31=0,2 mol.dựa theo pt (1) thấy nP2O5=0,1mol.theo pt (2) thấy nNaOH=0,4mol vậy mNaOH=0,4.40=16 g vậy m(dd NaOH)=16:32%=50 g
c, theo pt (2) nNa2HPO4 =0,2 mol vậy mNa2HPO4=0,2.142=28,4 g
m(dd sau pư)=mP+m(dd NaOH)=6,2+50=56,2 g
=> C%(dd Na2HPO4)=28,4:56,2=50,53%
Đúng 0
Bình luận (2)
đốt cháy hoàn toàn 6,2 gam photpho trong oxi dư . cho sản phẩm tạo thành tác dụng vừa đủ với dung dịch NaOH 32% tạo ra muối Na2HPO4 .
a) viết phương trình hóa học của các phản ứng xảy ra .
b) tính khối lượng dung dịch NaOH đã dùng .
c) tính nồng độ phần trăm của muối trong dung dịch thu được sau phản ứng .
Cho 8 g kim loại canxi phản ứng hoàn toàn với 92g nước. Sau phản ứng thu được dung dịch canxi hiđrôxit và khí hiđrôa/ Lập PTHH? Nêu tính chất hóa học của phản ứng vừa viết?b/ Tính khối lượng của Khí hiđrô thoát ra ?c/ Tính nồng độ phần trăm của dung dịch canxi hiđrôxit tạo thành sau phản ứng ?giúp mk vs ạ
Đọc tiếp
Cho 8 g kim loại canxi phản ứng hoàn toàn với 92g nước. Sau phản ứng thu được dung dịch canxi hiđrôxit và khí hiđrô
a/ Lập PTHH? Nêu tính chất hóa học của phản ứng vừa viết?
b/ Tính khối lượng của Khí hiđrô thoát ra ?
c/ Tính nồng độ phần trăm của dung dịch canxi hiđrôxit tạo thành sau phản ứng ?
giúp mk vs ạ
Hoà tan hoàn toàn m gam Na trong 500g nước (lấy dư), sau phản ứng thu đc dung dịch X và lượng khí hiđro đúng bằng lượng khí hiđro dùng cho phản ứng trên a) Tính m? b) Tính nồng độ % của dung dịch X thu đc ở trên?
Cho 1,6g đồng (II) oxit tác dụng với 100g dung dịch axit sunfuric có nồng độ 20%. a) Viết phương trình phản ứng hóa học. b) Tính nồng độ phần trăm các chất có trong dung dịch sau khi phản ứng kết thúc. Phần b tính C% của H2SO4 dư tại sao không lấy m dư của H2SO4 chia cho 100 ạ. Mà phải tính mdung dịch spu. Khi nào thì mới lấy mH2SO4/100
Hòa tan hoàn toàn 4,6g Natri vào nước thu được 300ml dd NaOH
a. Viết phương trình của phản ứng
b. Tính thể tích khí hidro tạo thành ở đktc
c. Tính nồng độ % của dd NaOH thu đc sau phản ứng
\(n_{Na}=\dfrac{4,6}{23}=0,2mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,2 0,2 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{NaOH}=0,2\cdot40=8g\)
\(m_{ddNaOH}=4,6+0,2\cdot18-0,1\cdot2=8g\)
\(\Rightarrow C\%=\dfrac{m_{NaOH}}{m_{ddNaOH}}\cdot100\%=\dfrac{8}{8}\cdot100\%=100\%???\)
Sửa đề: Tính nồng độ mol của dung dịch NaOH???
\(C_{M_{NaOH}}=\dfrac{0,2}{0,3}=\dfrac{2}{3}M\)
Đúng 4
Bình luận (0)
vì đề không cho \(D_{NaOH}=???\) nên không tính được dung dịch NaOH
Đúng 1
Bình luận (1)
Xem thêm câu trả lời