phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 ⇔ 2NH3
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .
phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 tạo thành 2NH3 (phản ứng thuận nghịch)
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 ⇔ 2NH3
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .
phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 tạo thành 2NH3 (phản ứng thuận nghịch)
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
phản ứng trong bình kín giữa các chất khí sau đây : N2 + H2 \(\Leftrightarrow\) 2NH3
Hỏi tốc độ phản ứng thay đổi như thế nào khi áp suất tăng 2 lần ? biết nhiệt độ của hệ không đổi .
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Phản ứng tổng hợp amoniac là phản ứng thuận nghịch:
N 2 (k) + 3 H 2 (k) ↔ 2 N H 3 (k)
ΔH = -92 kJ
Cân bằng của phản ứng này chuyển dịch như thế nào khi thay đổi một trong các điều kiện sau đây ? Giải thích.
1. Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống.
2. Giảm nhiệt độ.
3. Thêm khí nitơ.
4. Dùng chất xúc tác thích hợp.
N 2 (k) + 3 H 2 (k) ↔ 2 N H 3 (k)
ΔH = -92 kJ
1. Khi tăng áp suất chung, cân bằng chuyển dịch theo chiều từ trái sang phải là chiều tạo ra số mol khí ít hơn.
2. Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiéu từ trái sang phải là chiều của phản ứng toả nhiệt.
Nén 2 mol N2 và 8 mol H2 vào bình kín có thể tích 2 lít (chứa sẵn chất xúc tác với thể tích không đáng kể) và giữ cho nhiệt độ không đổi. Khi phản ứng trong bình đạt tới trạng thái cân bằng, áp suất các khí trong bình bằng 0,8 lần áp suất lúc đầu (khi mới cho vào bình, chưa xảy ra phản ứng).
Nồng độ của khí NH3 tại thời điểm cân bằng là giá trị nào trong số các giá trị sau?
A. 0,5M
B. 1M
C. 2M
D. 4M
Hỗn hợp N 2 và H 2 trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol N 2 đã phản ứng là 10%. Thành phần phần trăm số mol N 2 trong hỗn hợp ban đầu là
A. 20%.
B. 25%.
C. 10%.
D. 5%.
Hỗn hợp N 2 và H 2 trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol N 2 đã phản ứng là 10%. Thành phần phần trăm số mol N 2 trong hỗn hợp ban đầu là
A. 20%.
B. 25%.
C. 10%.
D. 5%.
Chọn B
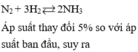
Áp suất thay đổi 5% so với áp suất ban đầu => n s a u n t r ư ớ c = 95 100
Giả sử trước phản ứng có 1 mol => sau phản ứng có 0,95 mol
ntrước – nsau = 2nN2 pư = 0,05 mol
è nN2 ban đầu = 0,025:10% = 0,25 =>%nN2 = 25%
Cho cân bẳng hóa học ( trong bình kín) sau: N2(khí) + 3H2(khí) <-> 2NH3 ΔH= -92kJ/mol
Trong các yếu tố:
(1) Thêm một lượng N2 hoặc H2.
(2) Thêm một lượng NH3.
(3) Tăng nhiệt độ của phản ứng.
(4) Tăng áp suất của phản ứng.
(5) Dùng thêm chất xuc tác.
Có bao nhiêu yếu tố làm cho tỉ khối của hỗn hợp khí trong bình so với H2 tăng lên
A. 3
B. 5
C. 4
D. 2
ĐÁP ÁN D
Tỉ khối hỗn hợp khí với H2 tăng => chứng tỏ số mol khí giảm (vì khối lượng không đổi)
=> phản ứng dịch theo chiều thuận
Các yếu tố thỏa mãn : (1) ; (4)