Dữ kiện Số mol a.15,12g hỗn hợp MgCO3 và CaCO3 (tỉ lệ khối lượng 2:1) b.5,6 lít (đkc) hỗn hợp khí X gồm CO và CO2 có khối lượng bằng 8,6g. c.5,6 lít (đkc) hỗn hợp khí X gồm CO và CO2 có tỉ khối so với hidro bằng 18,8

Những câu hỏi liên quan
Cho 2,84g hỗn hợp
C
a
C
O
3
và
M
g
C
O
3
tác dụng hết với dung dịch HCl thu được 0,03 mol khí
C
O
2
. Thành phần % theo khối lượng của
C
a
C
O
3
và
M
g
C
O
3
trong hỗn hợp lần lượt là A. 70,4% và 29,6%. B. 29,6% và 70,4%. C. 59,15% và 40,85%. ...
Đọc tiếp
Cho 2,84g hỗn hợp C a C O 3 và M g C O 3 tác dụng hết với dung dịch HCl thu được 0,03 mol khí C O 2 . Thành phần % theo khối lượng của C a C O 3 và M g C O 3 trong hỗn hợp lần lượt là
A. 70,4% và 29,6%.
B. 29,6% và 70,4%.
C. 59,15% và 40,85%.
D. 40,85% và 59,15%.
Cho hỗn hợp MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 4,48 lít khí (đktc). Tổng số mol của hai chất trong hỗn hợp đầu là: A. 0,2 mol. B. 0,3 mol C. 0,4 mol D. 0,6 mol.
Đọc tiếp
Cho hỗn hợp MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 4,48 lít khí (đktc). Tổng số mol của hai chất trong hỗn hợp đầu là:
A. 0,2 mol.
B. 0,3 mol
C. 0,4 mol
D. 0,6 mol.
Bài 4: Hoà tan 3,68 gam hỗn hợp 2 muối CaCO3 và MgCO3 bằng dung dịch H2SO4 dư thu được 0,896 lít khí CO2 (đktc). Tính thành phần % số mol mỗi muối trong hỗn hợp
CaCO3 + H2SO4 --> CaSO4 + CO2 + H2O
x x x
MgCO3 + H2SO4 --> MgSO4 + CO2 + H2O
y y y
nCO2=\(\dfrac{0,896}{22,4}\)=0,04
100x+84y=3,68
x+y=0,04
\(\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
%mCaCO3=\(\dfrac{0,02.100}{3,68}\)=54,35%
%mMgCO3=100-54,35=45,65%
mCaSO4=0,02.136=2,72g
mMgSO4=0,02.120=2,4g
Đúng 1
Bình luận (0)
Cho 2,84 g hỗn hợp CaCO3 và MgCO3 tác dụng hết với dung dịch HCl thấy bay ra 672 ml khí CO2 (đktc). Phần trăm khối lượng của hai muối( CaCO3 , MgCO3) trong hỗn hợp là :
A. 35,2 % và 64,8%.
B. 70,4% và 29,6%.
C. 85,49% và 14,51%.
D. 17,6% và 82,4%.
Đáp án B.
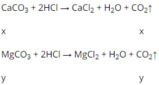
Số mol CO2: 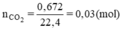
Gọi x, y lần lượt là số mol của CaCO3 và MgCO3 trong hỗn hợp
Theo bài ra ta có hệ phương trình:
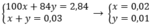
%mNa = 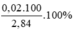 = 70,42%
= 70,42%
%mK = 100% - 70,42% = 29,58%
Đúng 0
Bình luận (0)
Nung hỗn hợp X gồm
C
a
C
O
3
và
M
g
C
O
3
theo phản ứng :
C
a
C
O
3
→
t
°
C
a
O
+
C
O
2
M
g
C
O
3
→
t
°
M
g...
Đọc tiếp
Nung hỗn hợp X gồm C a C O 3 và M g C O 3 theo phản ứng :
C a C O 3 → t ° C a O + C O 2
M g C O 3 → t ° M g O + C O 2
Nếu đem nung 31,8 gam hỗn hợp X thì thu được 7,84 lít C O 2 (đktc). Tính khối lượng của hỗn hợp của oxit thu được.
nhiệt phân hoàn toàn hỗn hợp A gồm MgCO3 và CaCO3 thu được 11,2 l CO2 và 2,2 g hỗn hợp B oxit của Mg và Ca. Tính hàm lượng CaCO3 có trong hỗn hợp? Tính khối lượng HCl cần để tác dụng hết với hỗn hợp ban đầu?
\(n_{MgCO_3}=a\left(mol\right)\)
\(n_{CaCO_3}=b\left(mol\right)\)
\(n_{CO_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(MgCO_3\underrightarrow{^{^{t^0}}}MgO+CO_2\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(\left\{{}\begin{matrix}a+b=0.5\\40a+56b=2.2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=1.6125\\b=-1.1125\end{matrix}\right.\)
Xem lại đề !
Đúng 1
Bình luận (1)
Cho hỗn hợp MgCO3 và CaCO3 tan trong dd HCl vừa đủ tạo ra 2.24l khí (đkc). tính tổng số mol của 2 chất trong hỗn hợp muối
hòa tan 2.84g hỗn hợp 2 muối CaCO3 và MgCO3 bằng dd HCl dư thu được 0.672 lít khí CO2 (đktc). TÍnh thành phần % số mol mỗi muối trong hỗn hợp
sai 1 chỗ mol CO2=0,627/22,4=0,03 sorry nhé
Đúng 0
Bình luận (0)
nCO2=6,72/22,4=0,03(mol)
pt ion:
H++CO32---------->HCO3-
------0,03---------0,03
Do HCl dư => H+ dư, tiếp tục xảy ra phản ứng:
H++HCO3----------->CO2+H2O
-----0,03---------0,03
Gọi số mol CaCO3 là x=>nCO32-=nCaCO3=x mol
MgCO3 là y=>nCO32-=nMgCO3=y mol
=>\(\Sigma\)nCO3=x+y (mol)
Mặt khác:
mCaCO3+mMgCO3=2,84 nên ta có hệ pt:
\(\left\{{}\begin{matrix}x+y=0,03\\100x+84y=2,84\end{matrix}\right.\)
<=>\(\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
Còn lại bạn tự tình đi cho quen
Chúc bạn học tốt! Thân
Đúng 0
Bình luận (0)
hòa tan 2.84g hỗn hợp 2 muối CaCO3 và MgCO3 bằng dd HCl dư thu được 0.672 lít khí CO2 (đktc). TÍnh thành phần % số mol mỗi muối trong hỗn hợp
Gọi x là số mol CaCO3
Gọi y là số mol MgCO3
PTHH: CaCO3 +2HCl -> CaCl2 +CO2+H2O(1)
xmol xmol
MgCO3 +2HCl -> MgCl2 +CO2+H2O(2)
ymol ymol
Theo đề ra và theo PT1,2 ta có hệ Pt:
100x +84y= 2,84 *
x+y =0,672/22,4
Giải hệ Pt, tìm x= 0,02= nCaCO3;
y=0,01= nMgCO3
%nCaCO3= 0,02/0,03.100%=67%
%nMgCO3= 33%
Đúng 1
Bình luận (1)
Ta có nCO2 = \(\dfrac{0,672}{22,4}\) = 0,03 ( mol )
CaCO3 + 2HCl → H2O + CO2 + CaCl2
x................2x...........x..........x..........x
MgCO3 + 2HCl → H2O + CO2 + MgCl2
y..................2y..........y..........y.............y
=> \(\left\{{}\begin{matrix}100x+84y=2,84\\x+y=0,03\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
=> mCaCO3 = 100 . 0,02 = 2 ( gam )
=> %mCaCO3 = \(\dfrac{2}{2,84}\times100\approx\) 70,4 %
=> %mMgCO3 = 100 - 70,4 = 29,6 %
Đúng 0
Bình luận (1)