đốt cháy 21 gam hỗn hợp bột nhôm và nhôm oxit tác dụng với dung dịch HCL làm thoát ra 13,44 lít k (đktc)
a tính khối lượng chất có trong hỗn hợp ban đầu
b, tính \(V_{ddHCl}\) 36% có d=1,18 để vừa đủ hoà tan hỗn hợp đócho 21g hỗn hợp bột nhôm và nhôm oxit tác dụng với dd HCL dư làm thoát ra 13,44 lít khí (đktc)
a)tính thành phần phần trăm theo khối lượng mỗi chất trong hỗm hợp đầu
b) tính thể tích dung dịch HCL 36% (D=1,18g /ml)để hào tan vừa đủ hỗn hợp đó
Cho 21g hỗn hợp bột nhôm và nhôm oxit tác dụng với đ HCl dư làm thoát ra 13,44 lít khí(đktc).
a) Tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp ban đầu.
b)Tính thể tích đ HCl 36%(D=1,18g/ml) để hòa tan vừa đủ hỗn hợp đó.
al td voi cl tao khi tinh mol khi suy he pt tinh khoi luong al lay khoi luong hh - khoi luong al tinh duoc khoi luong nhom oxit sau do tinh thanh phan phan tram.b)tu im
2 so mol cua 2 hon hop suy he pt tinh mol cua hcl tinh m hcl sau do tinh mddhcl dung cong thuc v=m/d tinh duoc vdd can t
cho 21g hỗn hợp bột nhôm và nhôm oxit tác dụng với hcl dư làm thoát ra 13,44 lít khí ( đktc )
a, tính thành phần % khối lượng mỗi chất trong hỗn hợp ban đầu
b, tính thể tích dung dịch hcl 36% ( d = 1,18g / ml ) đủ để hoàn tan hỗn hợp đó
ai biết làm thì giúp mình với mình đang cần gấp
PTHH: 2Al + 6HCl ===> 2AlCl3 + 3H2 (1)
0,4 1,2 0,6 (mol)
Al2O3 + 6HCl ===> 2AlCl3 + 3H2O (2)
0,1 0,6 (mol)
a/ 13,44 lít khí chính là sản phẩm của Al tác dụng với HCl
nH2 = 13,44 / 22,4 = 0,6 mol
Lập các sô mol trên phương trình, ta có
mAl = 0,4 x 27 = 10,8 gam
mAl2O3 = 21 - 10,8 = 10,2
=> Tính %m ( bạn tự tính nha)
b/ nAl2O3 = 10,2 / 102 = 0,1 mol
=> nHCl (2) = 0,1 x 6 = 0,6 mol
Lại có : nHCl (1) = 1,2 mol
=> Tổng số mol HCl = 0,6 + 1,2 = 1,8 mol
=> mHCl = 1,8 x 36,5 = 65,7 gam
=> mdung dịch HCl 36% = \(\frac{65,7.100}{36}\) = 182,5 gam
=> VHCl = 182,5 / 1,18 = 154,66 ml
Cho 31,2 gam hỗn hợp bột nhôm và Mg tác dụng vừa đủ với dung dịch HCL 2M.Sau phản ứng thu được 35,84 lít khí hiđrô bay ra(đktc)
a, Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu?
b,Tính thể tích dung dịch HCl đã dùng?
Cho 18,8g gram một hỗn hợp gồm Al và MgO tác dụng với dung dịch HCl 1,6 M vừa đủ thì thoát ra 6,72 lít khí Hidro ( thu được ở đktc ) a) Tính % theo khối lượng của Nhôm và Magie oxit trong hổn hợp ban đầu. b) Tính thể tích axit HCl đã dùng. c) Dùng toàn bộ lượng khí Hidro thu được đem thử hoàn toàn 1 lượng sắt oxit vừa đủ là 17,4 gram. Xác định công thức hóa học của oxit sắt. Help me
a)
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$MgO + 2HCl \to MgCl_2 + H_2O$
Theo PTHH : $n_{Al} = \dfrac{2}{3}n_{H_2} = 0,2(mol)$
$\%m_{Al} = \dfrac{0,2.27}{18,8}.100\% = 28,7\%$
$\%m_{MgO} = 100\% - 28,7\% =71,3\%$
b) $n_{MgO} = 0,335(mol)$
Theo PTHH : $n_{HCl} = 2n_{H_2} + 2n_{MgO} =1,27(mol)$
$V_{dd\ HCl} = \dfrac{1,27}{1,6} = 0,79375(lít)$
c)
$H_2 + O_{oxit} \to H_2O$
$\Rightarrow n_{O(oxit)} = n_{H_2} = 0,3(mol)$
$\Rightarrow n_{Fe} = \dfrac{17,4 - 0,3.16}{56} = 0,225(mol)$
Ta có :
$n_{Fe} : n_O = 0,225 : 0,3 = 3 : 4$
Vậy oxit là $Fe_3O_4$
Cho 25g hỗn hợp A gồm Nhôm và Nhôm oxit tác dụng vừa đủ vs a gam dung dịch axit clohidric, phản ứng tạo ra 5,6 lít khí (đktc)
a) Tính phần trăm về khối lượng mỗi chất có trong hỗn hợp A.
b) Tính a gam dung dịch axit clohidric đã phản ứng.
c) Tính thể tích dung dịch axit clohidric 20% (d=1,1g/cm³) vừa đủ để trung hòa hỗn hợp A trên.
d) Tính nồng độ phần trăm của các chất có trong dung dịch thu đc trong phản ứng.
\(a)n_{H_2}=\dfrac{5,6}{22,4}=0,25mol\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\dfrac{1}{6}\) \(0,5\) \(\dfrac{1}{6}\) \(0,25\)
\(\%m_{Al}=\dfrac{1:6.27}{25}\cdot100=18\%\\ \%m_{Al_2O_3}=100-18=82\%\\ b)n_{Al_2O_3}=\dfrac{25-1:6.27}{102}=\dfrac{41}{204}mol\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(\dfrac{41}{204}\) \(\dfrac{41}{36}\) \(\dfrac{41}{102}\)
\(m_{ddHCl}=\dfrac{\left(0,5+41:36\right)36,5}{20}\cdot100=299,1g\\ V_{ddHCl}=\dfrac{299,1}{1,1}=271,9ml\)
\(m_{dd}=299,1+25-0,25.2=323,6g\)
\(m_{AlCl_3}=\left(\dfrac{1}{6}+\dfrac{41}{102}\right)\cdot133,5=75,9g\\ C_{\%AlCl_3}=\dfrac{75,9}{323,6}\cdot100=23,45\%\)
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Đáp án A
Ta có sơ đồ phản ứng:
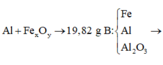
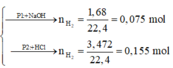
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
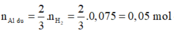
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
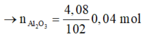
Ta có:
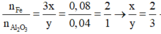
=> Oxit sắt cần tìm là Fe2O3
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Hòa tan hoàn toàn 21 gam hỗn hợp bột nhôm và nhôm oxit trong a gam dung dịch axit sunfuric 10% loãng (d=1,069 g/cm3) thì thu được 5,6 lít khí (đktc)
a) Tính thành phần % về khối lượng các chất có trong hỗn hợp đầu.
b) Tính thể tích dung dịch axit sunfuric 10% đã phản ứng.
Cho: Al: 27; O: 16; S: 32; H: 1đvC