đốt cháy V lít khí thiên nhiên chứa 96 phần trăm CH4, 2 phần trăm N2 và 2 phần trăm CO2 về thể tích. Toàn bộ sản phẩm cháy được dẫn qua dung dịch Ca(OH)2 dư thấy tạo ra 4.9 gam kết tủa.
a) viết PTHH (biết N2; CO2 không cháy)b)tính V?
Những câu hỏi liên quan
đốt cháy V lít khí thiên nhiên chứa 96 phần trăm CH4, 2 phần trăm N2 và 2 phần trăm CO2 về thể tích. Toàn bộ sản phẩm cháy được dẫn qua dung dịch Ca(OH)2 dư thấy tạo ra 4.9 gam kết tủa.
a) viết PTHH (biết N2; CO2 không cháy)b)tính V?a ,vì n2,co2 không cháy => pt hóa học: CH4 + 2O2 ----> CO2 + 2H2O
toàn bộ sp cháy dẫn qua dd Ca(OH)2 dư tạo ra kết tủa=> pt hóa học: CO2 + Ca(OH)2 dư ----> CaCO3 + H2Ob,gọi số mol hỗn hợp là x=> mol CH4 = 0.96x , mol CO2 trước phản ứng = 0.02xpt hóa học: CH4 + 2O2 ----> CO2 + 2H2Otheo pt 0.96x 0.96x (mol)pt hóa học: CO2 + Ca(OH)2 dư ----> CaCO3 + H2Otheo pt 0.049 0.049 (mol)=> tổng số mol CO2: 0.96x + 0.02x = 0.049 => x = 0.05=> v = 0.05 x 22.4 = 1.12 l
Đúng 1
Bình luận (0)
Đốt cháy V lít khí thiên nhiên chứa 96%
C
H
4
, 2%
N
2
và 2%
C
O
2
về thể tích. Toàn bộ sản phẩm cháy được dẫn qua dung dịch
C
a
O
H
2
dư thấy tạo ra 4,9 gam kết tủa. Giá trị của V là A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Đọc tiếp
Đốt cháy V lít khí thiên nhiên chứa 96% C H 4 , 2% N 2 và 2% C O 2 về thể tích. Toàn bộ sản phẩm cháy được dẫn qua dung dịch C a O H 2 dư thấy tạo ra 4,9 gam kết tủa. Giá trị của V là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít.

0 , 02 x m o l N 2 , 0 , 02 m o l C O 2 .
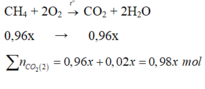
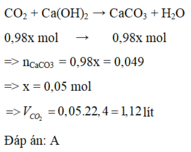
Đúng 0
Bình luận (0)
Đốt cháy 2,8 lít hỗn hợp khí CH4 và C2H2 ở đktc cần phải dùng 6,72 lít khí oxi a. Viết PTHH b. Tíng thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp c. Dẫn toàn bộ lượng khí sản phẩm hấp thụ hết vào dung dịch Ca(OH)2 dư, thấy xuất hiện kết tủa. Tính khối lượng kết tủa
\(n_{hhkhí}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ Gọi\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_2}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
CH4 + 2O2 \(\underrightarrow{t^o}\) CO2 + 2H2O
a 2a a
2C2H2 + 5O2 \(\underrightarrow{t^o}\) 4CO2 + 2H2O
b 2,5b 2b
Hệ phương trình: \(\left\{{}\begin{matrix}a+b=0,125\\2a+2,5b=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,025\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0,1}{0,125}=80\%\\ \%_{CH_4}=100\%-80\%=20\%\)
nCO2 = 2.0,025 + 2.0,1 = 0,25 (mol)
PTHH: Ca(OH)2 + CO2 -> CaCO3 + H2O
0,25 0,25
=> mCaCO3 = 0,25.100 = 25 (g)
Đúng 3
Bình luận (0)
Đốt cháy 4,48 lít hỗn hợp khí CH4 và SiH4 ở đktc thu được m gam chất rắn và sản phẩm khí và hơi. Dẫn toàn bộ sản phẩm khí vào dung dịch Ca(OH)2 dư thấy khối lượng dung dịch tăng 1,6 gam so với khối lượng dung dịch ban đầu. Thành phần phần trăm khối lượng của SiH4 trong hỗn hợp là: A. 50% B. 66,67% C. 33,33% D. 26,7%
Đọc tiếp
Đốt cháy 4,48 lít hỗn hợp khí CH4 và SiH4 ở đktc thu được m gam chất rắn và sản phẩm khí và hơi. Dẫn toàn bộ sản phẩm khí vào dung dịch Ca(OH)2 dư thấy khối lượng dung dịch tăng 1,6 gam so với khối lượng dung dịch ban đầu. Thành phần phần trăm khối lượng của SiH4 trong hỗn hợp là:
A. 50%
B. 66,67%
C. 33,33%
D. 26,7%
Đốt cháy hoàn toàn 4.48l(đktc) hỗn hợp khí X gồm CH4 và C2H5. Dẫn toàn bộ spham cháy vào dung dịch CA(OH)2 dư, thu đc 30g kết tủa. a) viết pthh của các phản ứg xảy ra b) Tính thành phần phần trăm thể tích mỗi khí trong X Cíu em voi ạ huhu
Bạn check lại đề cho mik chứ không có chất C2H5 aá :v
Đúng 1
Bình luận (0)
Peptit X và peptit Y có tổng liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lit O2 (đktc). Sản phẩm cháy gồm CO2,H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lit (đktc). Phần trăm khối lượng peptit Y trong E gần với : A. 91,0% B. 82,0% C. 82,5% D. 81,5%
Đọc tiếp
Peptit X và peptit Y có tổng liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lit O2 (đktc). Sản phẩm cháy gồm CO2,H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lit (đktc). Phần trăm khối lượng peptit Y trong E gần với :
A. 91,0%
B. 82,0%
C. 82,5%
D. 81,5%
Đáp án D
Gọi CT chung của amino axit tạo ra là ![]() có 0,22 mol;
có 0,22 mol;
k là số mol H2O cần để thủy phân E.
Bảo toàn khối lượng
![]()
Bảo toàn C, H :
![]() số mol gly = số mol val = 0,11
số mol gly = số mol val = 0,11
X là (gly)x(val)ycó a mol
(x + y) – 1 + (z + t) – 1 = 8) và (x + y) a + (z + t)3a = 0,22
Y là (gly)z(val)t có 3a mol
(x + y – 1)a + (z + t -1 )3a = 0,18 → a = 0,01 ; (x +y ) = 4; (z + t) = 6 → x = y = 2; t = z = 3
→%mY = 81,5%
Đúng 0
Bình luận (0)
Peptit X và peptit Y có tổng liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lit O2 (đktc). Sản phẩm cháy gồm CO2,H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lit (đktc). Phần trăm khối lượng peptit Y trong E gần với A. 91,0% B. 82,0% C. 82,5% D. 81,5%
Đọc tiếp
Peptit X và peptit Y có tổng liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lit O2 (đktc). Sản phẩm cháy gồm CO2,H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lit (đktc). Phần trăm khối lượng peptit Y trong E gần với
A. 91,0%
B. 82,0%
C. 82,5%
D. 81,5%
Peptit X và peptit Y có tổng liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lit O2 (đktc). Sản phẩm cháy gồm CO2, H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lit (đktc). Phần trăm khối lượng peptit Y trong E gần với : A. 91,0% B. 82,5% C. 82,0% D. 81,5%
Đọc tiếp
Peptit X và peptit Y có tổng liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lit O2 (đktc). Sản phẩm cháy gồm CO2, H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lit (đktc). Phần trăm khối lượng peptit Y trong E gần với :
A. 91,0%
B. 82,5%
C. 82,0%
D. 81,5%
Đáp án : D
Gọi CT chung của amino axit tạo ra là CnH2n+1O2N có 0,22 mol;
k là số mol H2O cần để thủy phân E.
Bảo toàn khối lượng 0,22(14n + 47) – 18k = 46,48 + 0,11. 28 – 0,99. 32 = 17,88 n = 3,5
Bảo toàn C, H : 0,22. 44. n + 18. 0,11(2n +1) – 18k = 46,48 k = 0,18 → số mol gly = số mol val = 0,11
X là (gly)x (val)y có a mol (x + y) – 1 + (z + t) – 1 = 8) và (x + y) a + (z + t)3a = 0,22
Y là (gly)z (val)t có 3a mol (x + y – 1)a + (z + t -1 )3a = 0,18 → a = 0,01 ; (x +y ) = 4; (z + t) = 6 → x = y = 2; t = z = 3
=> %mY = 81,5%
Đúng 0
Bình luận (0)
Peptit X và peptit Y đều mạch hở có tổng số liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lít O2 (đktc). Dẫn toàn bộ sản phẩm cháy gồm CO2, H2O và N2 qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lít (đktc). Phần trăm khối lượng của X trong hỗn hợp E có giá trị gần nhất với A. 14 B. 29 C. 19 D. 24
Đọc tiếp
Peptit X và peptit Y đều mạch hở có tổng số liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được Gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ mol tương ứng 1:3 cần dùng 22,176 lít O2 (đktc). Dẫn toàn bộ sản phẩm cháy gồm CO2, H2O và N2 qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48 gam, khí thoát ra khỏi bình có thể tích 2,464 lít (đktc). Phần trăm khối lượng của X trong hỗn hợp E có giá trị gần nhất với
A. 14
B. 29
C. 19
D. 24
Đáp án : C
Giả sử trong X có x axit amin và trong Y có y axit amin
=> x + y = số liên kết peptit + 1 + 1 = 10
,nO2 = 0,99 mol
,mbình tăng = 46,48g = mCO2 + mH2O(1)
Bảo toàn khối lượng : mE + mO2 = mCO2 + mH2O + mN2
=> mE = 17,88g có a mol X ; 3a mol Y
=> nN = ax + 3ay = 2nN2 = 0,22 mol
Khi đốt cháy : - nCO2 + nH2O + nN2 = nE => - nCO2 + nH2O = - 0,11 + 4a (2)
Bảo toàn O : nO(E) + 2nO2 = 2nCO2 + nH2O
Vì nO(E) = nCO + 2nCOO = nNH + nE = 4a + 0,22 mol
=> 2nCO2 + nH2O = 4a + 2,2 mol(3)
( nN = nCO + nCOO ; nE = nCOO )
Từ (1,2,3) => a = 0,01 ; nCO2 = 0,77 ; nH2O = 0,7 mol
=> x + 3y = 22
=> x = 4 ; y = 6
X : 0,01 mol (Gly)n(Val)4 – n
Y : 0,03 mol (Gly)m(Val)6 – m
=> mE = 0,01.(414 – 42n) + 0,03.(612 – 42m) = 17,88
=> n + 3m = 11
+) m = 3 ; n = 2 thỏa mãn
=> %mX(E) = 18,46%
Đúng 0
Bình luận (0)












