
Những câu hỏi liên quan
Hòa tan hoàn toàn 4,8 gam kim loại M (biết M chỉ có một hóa trị duy nhất) vào dung dịch axit HNO3 dư, thu được dung dịch A. Chia A thành 2 phần bằng nhau. - Phần 1: cho tác dụng với NaOH dư được kết tủa B. Nung B đến khối lượng không đổi thu được 4,0 gam oxit kim loại. - Phần 2: cô cạn ở điều kiện thích hợp thu được 25,6 gam một muối X duy nhất. Muối X có công thức phân tử là A. Mg(NO3)2.nH2O B. Mg(NO3)2.2H2O C. Cu(NO3)2 D. Mg(NO3)2.6H2O
Đọc tiếp
Hòa tan hoàn toàn 4,8 gam kim loại M (biết M chỉ có một hóa trị duy nhất) vào dung dịch axit HNO3 dư, thu được dung dịch A. Chia A thành 2 phần bằng nhau.
- Phần 1: cho tác dụng với NaOH dư được kết tủa
B. Nung B đến khối lượng không đổi thu được 4,0 gam oxit kim loại.
- Phần 2: cô cạn ở điều kiện thích hợp thu được 25,6 gam một muối X duy nhất. Muối X có công thức phân tử là
A. Mg(NO3)2.nH2O
B. Mg(NO3)2.2H2O
C. Cu(NO3)2
D. Mg(NO3)2.6H2O
Đáp án D
Gọi hóa trị của kim loại là n (1 ; 2 ; 3), Khối lượng mol là a (g)
Gọi số mol muối mỗi phần là x. Ta có số mol kim loại ban đầu là 2x
Có : 2ax = 4,8 nên ax = 2,4 (1)
Nếu muối tạo thành chỉ là M(NO3)n thì ta có : (a + 62n)x = 25,6 (2)
Từ (1) và (2) => x = (25,6 – 2,4)/(62n) = 0,187/n
Mặt khác , số mol oxit thu được là x/2
=> (2a + 16n).x/2 = 4 (3)
Từ (1) và (3) => x = (4 – 2,4)/(16n) = 0,1/n.
2 giá trị x không bằng nhau. Vì vậy muối phải là muối ngậm nước.
Đặt công thức muối là M(NO3)n.mH2O
Khối lượng muối mỗi phần là (a + 62n + 18m)x = 25,6 (4)
Kết hợp (1), (3), (4) ta có hệ sau :
ax = 2,4
(2a + 16n).x/2 = 4
(a + 62n + 18m)x = 25,6
=> nx = 0,2 ; mx = 0,6
=> a/n = 12. Thay n = 1, 2, 3 ta được a = 24g => Mg
Thay n = 2 => x = 0,1 ; do đó m = 6
Vậy M là Mg và muối là Mg(NO3)2.6H2O
Đúng 0
Bình luận (0)
Bài : Hòa tan hoàn toàn a gam kim loại M trong dung dịch HCl thu được dung dịch A và 2.24 lít H2 (đktc). CHia A thành 2 phần bằng nhau : Phần thứ nhất tác dụng hoàn toàn với KOH dư , thu được kết tủa B . Nung B trong không khí ở nhiệt độ cao tới khối lượng không đổi , thu được (b+2.4) gam chất rắn C . Hòa tan C trong H2SO4 loãng dư được dung dịch D . Xử lí D ở nhiệt độ thích hợp thu được 28.1 gam 1 muối duy nhất . Xử lí phần 2 chỉ thu được một muối Y duy nhất với khối lượng 19.9 gam . Xác định...
Đọc tiếp
Bài : Hòa tan hoàn toàn a gam kim loại M trong dung dịch HCl thu được dung dịch A và 2.24 lít H2 (đktc). CHia A thành 2 phần bằng nhau : Phần thứ nhất tác dụng hoàn toàn với KOH dư , thu được kết tủa B . Nung B trong không khí ở nhiệt độ cao tới khối lượng không đổi , thu được (b+2.4) gam chất rắn C . Hòa tan C trong H2SO4 loãng dư được dung dịch D . Xử lí D ở nhiệt độ thích hợp thu được 28.1 gam 1 muối duy nhất . Xử lí phần 2 chỉ thu được một muối Y duy nhất với khối lượng 19.9 gam . Xác định công thức X , Y biết a=2b
Đây mà là toán 1 hở
???????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????
Xem thêm câu trả lời
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau. – Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối. – Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa. a. Xác định tên kim loại M. b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X. c. Tính V và m.
Đọc tiếp
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D = 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau.
– Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối.
– Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa.
a. Xác định tên kim loại M.
b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X.
c. Tính V và m.
Hòa tan hoàn toàn 28,11 gam hỗn hợp gồm 2 muối R2CO3 và RHCO3 vào nước, thu được dung dịch X. Chia X thành 3 phần bằng nhau. Phần một tác dụng hoàn toàn với dung dịch Ca(OH)2 dư, thu được 11 gam kết tủa. Phần hai tác dụng hoàn toàn với dung dịch CaCl2 dư, thu được 4 gam kết tủa. Phần ba phản ứng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là A. 110 B. 220 C. 70 D. 140
Đọc tiếp
Hòa tan hoàn toàn 28,11 gam hỗn hợp gồm 2 muối R2CO3 và RHCO3 vào nước, thu được dung dịch X. Chia X thành 3 phần bằng nhau. Phần một tác dụng hoàn toàn với dung dịch Ca(OH)2 dư, thu được 11 gam kết tủa. Phần hai tác dụng hoàn toàn với dung dịch CaCl2 dư, thu được 4 gam kết tủa. Phần ba phản ứng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là
A. 110
B. 220
C. 70
D. 140
Đáp án : B
* Phân 2 : R2CO3 + CaCl2 à CaCO3↓ + 2RCl
0,04 ß 0,04
* Phần 1 : R2CO3 + Ca(OH)2 à CaCO3↓ + 2ROH
0,04 à 0,04
RHCO3 + Ca(OH)2 à CaCO3↓ +ROH + H2O
0,07 ß (0,11 – 0,04)
=> 0,04(2R + 60) + 0,07(R + 61) = 28,11/3 => R = 18 (NH4+)
* Phần 3 : (NH4)2CO3 + 2NaOH à Na2CO3 + NH3 + 2H2O
0,04 à 0,08
NH4HCO3 + 2NaOH à Na2CO3 + NH3 + 2H2O
0,07 à 0,14
=> nNaOH = 0,14 + 0,08 = 0,22 mol
=> V ddNaOH = 0,22/1 = 0,22 l = 220 ml
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 28,11 gam hỗn hợp gồm 2 muối R2CO3 và RHCO3 vào nước, thu được dung dịch X. Chia X thành 3 phần bằng nhau. Phần một tác dụng hoàn toàn với dung dịch Ca(OH)2 dư, thu được 11 gam kết tủA. Phần hai tác dụng hoàn toàn với dung dịch CaCl2 dư, thu được 4 gam kết tủa. Phần ba phản ứng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là A. 110. B. 220. C. 70. D. 140.
Đọc tiếp
Hòa tan hoàn toàn 28,11 gam hỗn hợp gồm 2 muối R2CO3 và RHCO3 vào nước, thu được dung dịch X. Chia X thành 3 phần bằng nhau. Phần một tác dụng hoàn toàn với dung dịch Ca(OH)2 dư, thu được 11 gam kết tủA. Phần hai tác dụng hoàn toàn với dung dịch CaCl2 dư, thu được 4 gam kết tủa. Phần ba phản ứng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là
A. 110.
B. 220.
C. 70.
D. 140.
Đáp án B
Khối lượng mỗi phần là 28,11/3 = 9,37g
Phần 2 tạo 0,04 mol CaCO3 => nCO32- = 0,04
Phần 1 tạo 0,11 mol CaCO3=> nHCO3- = 0,11 – 0,04 = 0,07
(2R + 60)0,04 + (R + 61)0,07 = 9,37 R = 18 R là NH4
Phần 3:
(NH4)2CO3 +2NaOH -> Na2CO3 + 2NH3 + 2H2O
NH4HCO3 + 2NaOH -> Na2CO3 + NH3 + 2H2O
nNaOH = (0,04 + 0,07).2 = 0,22 V = 0,22 lít
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 28,11 gam hỗn hợp gồm 2 muối R2CO3 và RHCO3 vào nước, thu được dung dịch X. Chia X thành 3 phần bằng nhau. Phần một tác dụng hoàn toàn với dung dịch Ca(OH)2 dư, thu được 11 gam kết tủa. Phần hai tác dụng hoàn toàn với dung dịch CaCl2 dư, thu được 4 gam kết tủa. Phần ba phản ứng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là A. 110. B. 220 C. 70. D. 140
Đọc tiếp
Hòa tan hoàn toàn 28,11 gam hỗn hợp gồm 2 muối R2CO3 và RHCO3 vào nước, thu được dung dịch X. Chia X thành 3 phần bằng nhau. Phần một tác dụng hoàn toàn với dung dịch Ca(OH)2 dư, thu được 11 gam kết tủa. Phần hai tác dụng hoàn toàn với dung dịch CaCl2 dư, thu được 4 gam kết tủa. Phần ba phản ứng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là
A. 110.
B. 220
C. 70.
D. 140
Chọn B
Khối lượng mỗi phần là 28,11/3 = 9,37g
Phần 2 tạo 0,04 mol CaCO3 → nCO32- = 0,04
Phần 1 tạo 0,11 mol CaCO3 → nHCO3- = 0,11 – 0,04 = 0,07
→ (2R + 60)0,04 + (R + 61)0,07 = 9,37
→ R = 18 → R là NH4
Phần 3:
(NH4)2CO3 +2NaOH → Na2CO3 + 2NH3 + 2H2O
NH4HCO3 + 2NaOH → Na2CO3 + NH3 + 2H2O
→ nNaOH = (0,04 + 0,07).2 = 0,22 → V = 0,22 lít
Đúng 0
Bình luận (0)
Thực hiện phản ứng nhiệt nhôm hỗn hợp Al và Fe3O4 ( trong điều kiện không có không khí thu được 234,75 gam chất rắn X. Chia X thành hia phần: -Cho phần 1 tác dụng với dung dịch NaOH dư thu được 1,68 lít khí H2 ở đktc và m gam chất rắn. Hòa tan hết m gam chất rắn vào dung dịch H2SO4 đực nóng thu được một dung dịch chứa 82,8 gam muối và 0,6 mol SO2 là sản phẩm khử duy nhất của S+6. -Hoàn tan hết phần 2 trong 12,97 lít dung dịch HNO3 1M, thu được hỗn hợp khí Y (gồm 1,25 mol NO và 1,51 mol NO2) và d...
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp Al và Fe3O4 ( trong điều kiện không có không khí thu được 234,75 gam chất rắn X. Chia X thành hia phần:
-Cho phần 1 tác dụng với dung dịch NaOH dư thu được 1,68 lít khí H2 ở đktc và m gam chất rắn. Hòa tan hết m gam chất rắn vào dung dịch H2SO4 đực nóng thu được một dung dịch chứa 82,8 gam muối và 0,6 mol SO2 là sản phẩm khử duy nhất của S+6.
-Hoàn tan hết phần 2 trong 12,97 lít dung dịch HNO3 1M, thu được hỗn hợp khí Y (gồm 1,25 mol NO và 1,51 mol NO2) và dung dịch A chứa các chất tan đều là muối, trong đó có a mol Fe(NO3)3.
Biết các phản ứng hoàn toàn. Giá trị a gần nhất với giá trị nào sau đây?
A. 1,10.
B. 1.50.
C. 1,00.
D. 1,20.
Phản ứng nhiệt nhôm:
![]()
X tác dụng với NaOH thu được => Al dư (*)
Phản ứng xảy ra hoàn toàn (**)
Kết hợp (*), (**) => F e 3 O 4 hết => X gồm Fe, A l 2 O 3 và Al dư
Chú ý: Bài toán chia làm hai phần không bằng nhau
*Xét phần một
Số mol H2 thu được là: ![]()
Trong X, chỉ có Al2O3 và Al dư tác dụng với NaOH theo sơ đồ sau:
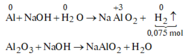
![]()
![]()
Chất rắn thu được là Fe
Chất rắn thu được tác dụng với H2SO4 đặc, nóng:
Sơ đồ phản ứng:
![]()
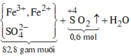
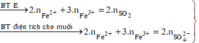
![]()
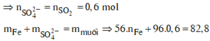
![]()
![]()
![]()
![]()
![]()
![]()
![]()
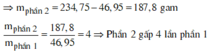
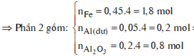
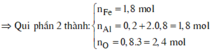
*Xét phần hai:
Số mol HNO3 là: ![]()
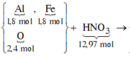
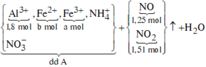
Các quá trình tham gia của H+:
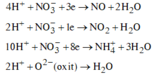
![]()
![]()
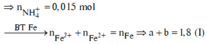
![]()
![]()
![]()

Đúng 0
Bình luận (0)
Chia 47,1 gam hỗn hợp X gồm Mg, Al, Zn, Ni thành 2 phần bằng nhau. Phần 1 tác dụng hoàn toàn với dung dịch HNO3 vừa đủ thu được 7,84 lít khí NO duy nhất (đktc) và dung dịch Y chứa x gam muối (không chứa NH4NO3). Nếu cho Y tác dụng với dung dịch NaOH thì lượng kết tủa lớn nhất thu được là y gam. Phần 2 tác dụng hoàn toàn vói dung dịch HC1 thu được V lít khi H2 (đktc). Giá trị của V là A. 11,76 B. 23,52 C. 13,44 D. 15,68
Đọc tiếp
Chia 47,1 gam hỗn hợp X gồm Mg, Al, Zn, Ni thành 2 phần bằng nhau. Phần 1 tác dụng hoàn toàn với dung dịch HNO3 vừa đủ thu được 7,84 lít khí NO duy nhất (đktc) và dung dịch Y chứa x gam muối (không chứa NH4NO3). Nếu cho Y tác dụng với dung dịch NaOH thì lượng kết tủa lớn nhất thu được là y gam. Phần 2 tác dụng hoàn toàn vói dung dịch HC1 thu được V lít khi H2 (đktc). Giá trị của V là
A. 11,76
B. 23,52
C. 13,44
D. 15,68
Đáp án A
Tương tự Câu 12, áp dụng định luật bảo toàn mol electron ta có
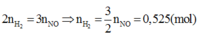
Vậy V= 11,76 (lít)
Đúng 0
Bình luận (0)
Chia 47,1 gam hỗn hợp X gồm Mg, Al, Zn, Ni thành 2 phần bằng nhau. Phần 1 tác dụng hoàn toàn với dung dịch HNO3 vừa đủ thu được 7,84 lít khí NO duy nhất (đktc) và dung dịch Y chứa x gam muối (không chứa NH4NO3). Nếu cho Y tác dụng với dung dịch NaOH thì lượng kết tủa lớn nhất thu được là y gam. Phần 2 tác dụng hoàn toàn vói dung dịch HC1 thu được V lít khi H2 (đktc).Giá trị của V là A. 11,76 B. 23,52 C. 13,44 D. 15,68
Đọc tiếp
Chia 47,1 gam hỗn hợp X gồm Mg, Al, Zn, Ni thành 2 phần bằng nhau. Phần 1 tác dụng hoàn toàn với dung dịch HNO3 vừa đủ thu được 7,84 lít khí NO duy nhất (đktc) và dung dịch Y chứa x gam muối (không chứa NH4NO3). Nếu cho Y tác dụng với dung dịch NaOH thì lượng kết tủa lớn nhất thu được là y gam. Phần 2 tác dụng hoàn toàn vói dung dịch HC1 thu được V lít khi H2 (đktc).Giá trị của V là
A. 11,76
B. 23,52
C. 13,44
D. 15,68
Đáp án A
Tương tự câu 12, áp dụng định luật bảo toàn mol electron ta có:
2 n H 2 = 3 n N O = > 3 2 n N O = 0 , 525 ( m o l )
Vậy V = 11,76 (lít)
Đúng 0
Bình luận (0)









