Cho sắt kim loại tác dụng với dd axit sunfuric loãng, sau đó cho bay hơi hết nước của dd thu được thì còn lại 55,6g tinh thể FeSO4.7H2O. Thể tích hiđro thoát ra(đktc) khi Fe tan là bao nhiêu lít ?

Những câu hỏi liên quan
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi thu được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2(đktc) được giải phóng làA. 8,19 lít. B. 7,33 lít.C. 4,48 lít. D. 6,23 lít.
Đọc tiếp
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi thu được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2(đktc) được giải phóng là
A. 8,19 lít. B. 7,33 lít.
C. 4,48 lít. D. 6,23 lít.
BTNT Fe: \(nFe=nFeSO_4.7H_2O=\dfrac{55,6}{278}=\dfrac{1}{5}=0,2mol\)
⇒ \(nH2=0,2mol\)
⇒ \(V=0,2.22,4=\dfrac{112}{25}=4,48\) lít
Đúng 2
Bình luận (0)
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là A. 4,48 lít. B. 8,19 lít. C. 7,33 lít D. 6,23 lít
Đọc tiếp
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là
A. 4,48 lít.
B. 8,19 lít.
C. 7,33 lít
D. 6,23 lít
Chọn A
BTNT Fe: nFe = nFeSO4.7H2O = 55,6/278 = 0,2 mol => nH2 = 0,2 mol => V = 0,2.22,4 = 4,48 lít
Đúng 0
Bình luận (0)
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là A. 4,48 lít. B. 8,19 lít. C. 7,33 lít. D. 6,23 lít.
Đọc tiếp
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là
A. 4,48 lít.
B. 8,19 lít.
C. 7,33 lít.
D. 6,23 lít.
BTNT Fe: nFe = nFeSO4.7H2O = 55,6/278 = 0,2 mol
=> nH2 = 0,2 mol => V = 0,2.22,4 = 4,48 lít
Đáp án A
Đúng 0
Bình luận (0)
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là A. 4,48 lít B. 8,19 lít. C. 7,33 lít. D. 6,23 lít.
Đọc tiếp
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là
A. 4,48 lít
B. 8,19 lít.
C. 7,33 lít.
D. 6,23 lít.
Đáp án A
BTNT Fe: nFe = nFeSO4.7H2O = 55,6/278 = 0,2 mol => nH2 = 0,2 mol => V = 0,2.22,4 = 4,48 lít
Đúng 0
Bình luận (0)
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi thu được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2(đktc) được giải phóng là :
A. 8,19 lít.
B. 7,33 lít.
C. 4,48 lít.
D. 6,23 lít.
Đáp án C.
Cứ 278 g FeSO4.7H2O có 152 g FeSO4
→ 55,6 g FeSO4.7H2O có x (g) FeSO4
Khối lượng FeSO4 là 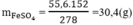
Số mol FeSO4: 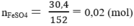
Fe + H2SO4 → FeSO4 + H2
nH2 = nFeSO4 = 0,2 (mol) ⇒ VH2 = 0,2.22,4 = 4,48 (lit)
Đúng 0
Bình luận (0)
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng. a) Viết các phương trình phản ứng. b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất? c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Đọc tiếp
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
a) Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4loãng → FeSO4 + H2
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
b) Giả sử cho cùng một khối lượng là a g kim loại kẽm sắt và nhôm
Zn + H2SO4 → ZnSO4 + H2 (1)
Fe + H2SO4loãng → FeSO4 + H2 (2)
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2 (3)
Ta có 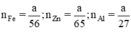
Theo pt nH2 (1) = nZn = 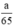 mol
mol
nH2 (2) = nFe = 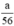 mol
mol
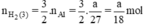
Như vậy ta nhận thấy 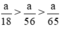 ⇒ nH2 (3) > nH2 (2) > nH2 (1)
⇒ nH2 (3) > nH2 (2) > nH2 (1)
Như vậy cho cùng một lượng kim loại tác dụng với axit H2SO4 loãng dư thì nhôm cho nhiều khí hidro hơn, sau đó đến sắt và ít nhất là kẽm
c) Nếu thu được cùng một lượng khí hidro thì khối lượng kim loại ít nhất là nhôm, sau đó đến sắt, cuối cùng là kẽm.
Đúng 1
Bình luận (0)
Cho 14 gam kim loại Fe tan hoàn toàn trong dd axit sunfuric (H2SO4) 20%.a/ Viết phương trình phản ứng xảy ra?b/ Tính thể tích khí hiđro thoát ra (ở đktc)?c/Tính khối lượng dd axit sunfuric cần dùng? d/ Tính nồng độ phần trăm của dung dịch sau phản ứng? giải giúp mk vs ạ
Đọc tiếp
Cho 14 gam kim loại Fe tan hoàn toàn trong dd axit sunfuric (H2SO4) 20%.
a/ Viết phương trình phản ứng xảy ra?
b/ Tính thể tích khí hiđro thoát ra (ở đktc)?
c/Tính khối lượng dd axit sunfuric cần dùng?
d/ Tính nồng độ phần trăm của dung dịch sau phản ứng?
giải giúp mk vs ạ![]()
Cho 22,4g sắt tác dụng với dung dịch loãng có chứa 24,5g axit sunfuric.
a) Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b) Tính thể tích khí hiđro thu được ở đktc.
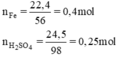
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 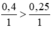 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.
Đúng 0
Bình luận (0)
Cho 6,75g kim loại của nhôm tác dụng với 196g dd axit sufuric 15% . Tính thể tích khí hiđro thoát ra ở đktc











