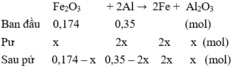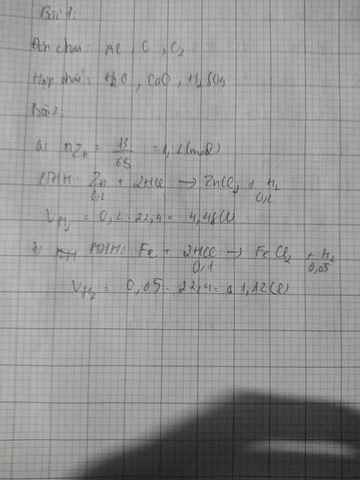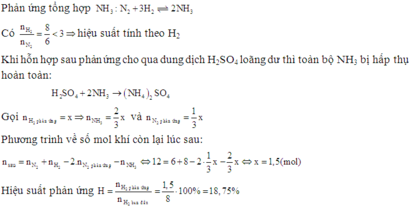Để điều chế Fe người ta dùng 16g Fe2O3 tác dụng hết vs H2 ở nhiệt độ cao. Sắt mới thu đc cho phản ứng vs dung dịch H2SO4 loãng dư. Sau cùng thu đc 3l H2(đktc). Tính hiệu suất của phản ứng tạo sắt.

Những câu hỏi liên quan
Để điều chế Fe người ta dùng 16g Fe2O3 tác dụng hết vs H2 ở nhiệt độ cao. Sắt mới thu đc cho phản ứng vs dung dịch H2SO4 loãng dư. Sau cùng thu đc 3l H2(đktc). Tính hiệu suất của phản ứng tạo sắt.
Mol \(Fe_2O_3\) bđ=16/160=0,1 mol
Mol \(H_2\) =3/22,4 mol\(Fe_2O_3\) +3\(H_2\) \(\rightarrow\)2\(Fe\) +3\(H_2O\)Bđ: 0,1 molPứ: 15/224 mol<=45/112 mol 3/22,4 molDư: 0,033 mol\(Fe\) + 2\(HCl\) \(\rightarrow\) \(FeCl_2+H_2\)3/22,4 mol<= 3/22,4 molLập tỉ lệ mol \(Fe_2O_3\) và \(H_2\) lần lượt với hệ số trong pt=> tính H% theo \(Fe_2O_3\)H%=(15/224)/0,1 .100%=66,96%
Đúng 1
Bình luận (0)
Trộn 27,84 gam
Fe
2
O
3
với 9,45 gam bột Al rồi thực hiện phản ứng nhiệt nhôm (giả sử chỉ có phản ứng khử oxit sắt thành Fe kim loại), sau một thời gian thu được hỗn hợp B. Cho hỗn hợp B tác dụng vớí dung dịch
H
2
SO
4
loãng dư thu được 9,744 lít khí
H
2
(đktc). Hiệu suất phản ứng nhiệt nhôm là ...
Đọc tiếp
Trộn 27,84 gam Fe 2 O 3 với 9,45 gam bột Al rồi thực hiện phản ứng nhiệt nhôm (giả sử chỉ có phản ứng khử oxit sắt thành Fe kim loại), sau một thời gian thu được hỗn hợp B. Cho hỗn hợp B tác dụng vớí dung dịch H 2 SO 4 loãng dư thu được 9,744 lít khí H 2 (đktc). Hiệu suất phản ứng nhiệt nhôm là
A. 51,43%,
B. 51,72%.
C. 75,00%.
D. 68,50%.
Tính thể tích khí H2 ở đktc để điều chế đc khi cho: a) 13g kẽm tác dụng hết vs dung dịch H2SO4 loãng. b ) dung dịch chứa 0.1mol axit HCl tác dụng vs sắt dư
Zn+2H2SO4->ZnSO4+H2
0,2----------------------------0,2
n Zn=\(\dfrac{13}{65}\)=0,2 mol
=>VH2=0,2.22,4=4,48l
b)
Fe+2HCl->FeCl2+H2
0,1--------------0,05 mol
=>VH2=0,05.22,4=1,12l
Đúng 1
Bình luận (0)
\(a,n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2}=n_{Zn}=0,2\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ b,Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{HCl}=0,1\left(mol\right)\Rightarrow n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 18g nhôm vào dung dịch H2SO4 loãng dưa. Tính thể tích H2 tạo thành ở điều kiện tiêu chuẩnb. Nếu dùng lượng H2 thu đc ở phản ứng trên cho phản ứng với 32g sắt 3 oxit đã đc nung nóng thì khối lượng sắt thu đc là bao nhiêuc. Tính thể tích không khí chứa 20% thể tích oxi ở điều kiện tiêu chuẩn cần dùng để phản ứng vừa đủ với lượng Sắt thu đc ở trên.Bt sản phẩm sau p.ứng là Sắt II.III oxit
Đọc tiếp
Hòa tan hoàn toàn 18g nhôm vào dung dịch H2SO4 loãng dư
a. Tính thể tích H2 tạo thành ở điều kiện tiêu chuẩn
b. Nếu dùng lượng H2 thu đc ở phản ứng trên cho phản ứng với 32g sắt 3 oxit đã đc nung nóng thì khối lượng sắt thu đc là bao nhiêu
c. Tính thể tích không khí chứa 20% thể tích oxi ở điều kiện tiêu chuẩn cần dùng để phản ứng vừa đủ với lượng Sắt thu đc ở trên.Bt sản phẩm sau p.ứng là Sắt II.III oxit
a)\(n_{Al}=\dfrac{18}{27}=\dfrac{2}{3}mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}\) 1
\(V_{H_2}=1\cdot22,4=22,4l\)
b)\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,2 1 0,4 0,6
\(m_{Fe}=0,4\cdot56=22,4g\)
c)\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,4 \(\dfrac{4}{15}\)
\(V_{O_2}=\dfrac{4}{16}\cdot22,4=\dfrac{448}{75}l\)
\(V_{kk}=5V_{O_2}=\dfrac{448}{15}l\approx29,87l\)
Đúng 3
Bình luận (0)
Cho 22,4g Fe tác dụng với dung dịch loãng có chứa 24,5 g H2SO4 sau phản ứng hãy cho biết: a, Chất nào dư sau phản ứng và dư bao nhiêu gam? b, Tính thể tích H2 thu được ở đktc. Có đc ghi fe +h2so4--->fe2(so4)3 +h2 đc ko ạ
`Fe + H_2 SO_4 -> FeSO_4 + H_2`
`0,25` `0,25` `0,25` `(mol)`
`a)n_[Fe]=[22,4]/56=0,4(mol)`
`n_[H_2 SO_4]=[24,5]/98=0,25(mol)`
Có: `[0,4]/1 > [0,25]/1=>Fe` hết, `H_2 SO_4`
`=>m_[Fe(dư)]=(0,4-0,25).56=8,4(g)`
`b)V_[H_2]=0,25.22,4=5,6(l)`
Ko được ghi `Fe+H_2 SO_4->Fe_2 (SO_4)_3+H_2` vì đây là `H_2 SO_4` loãng
Đúng 4
Bình luận (2)
Giả thiết: Nhôm tác dụng với Fe3O4 chỉ tạo Al2O3 và sắt. Trộn 10,8g bột Al với 34,8g bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng dư thu được 10,416 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là: A. 80,0% B. 90,0% C. 70,0% D. 60,0%
Đọc tiếp
Giả thiết: Nhôm tác dụng với Fe3O4 chỉ tạo Al2O3 và sắt. Trộn 10,8g bột Al với 34,8g bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng dư thu được 10,416 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là:
A. 80,0%
B. 90,0%
C. 70,0%
D. 60,0%
Đáp án B
nAl = 10,8: 27 = 0,4 mol ; nFe3O4 = 34,8: 232 = 0,15 mol
Ta thấy: 0,4/8 = 0,15/3 nên hiệu suất có thể tính theo Al hoặc Fe3O4
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
Mol x → 1,125x => nAl dư = (0,4 –x) mol
Khi chất rắn sau phản ứng + HCl thì:
Al + 3HCl → AlCl3 + 1,5H2
Mol (0,4 – x) → 1,5(0,4 – x)
Fe + 2HCl → FeCl2 + H2
Mol 1,125x → 1,125x
=> nH2 = 1,5(0,4 – x) + 1,125x = 10,416: 22,4 = 0,465 mol
=> x = 0,36 mol
Tính H theo Al => H% = nPứ / nbđ = 0,36: 0,4 = 90%
Đúng 0
Bình luận (0)
Người ta dùng H2 (dư) tác dụng hết với x gam Fe2O3 nung nóng thu được y gam Fe. Cho lượng sắt này tác dụng với dung dịch H2SO4 loãng dư thì thu được 6,72 lít khí H2 (đktc). Tính giá trị x và y.
Đọc tiếp
Người ta dùng H2 (dư) tác dụng hết với x gam Fe2O3 nung nóng thu được y gam Fe. Cho lượng sắt này tác dụng với dung dịch H2SO4 loãng dư thì thu được 6,72 lít khí H2 (đktc). Tính giá trị x và y.
PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)=n_{Fe}\)
\(\Rightarrow n_{Fe_2O_3}=0,15\left(mol\right)\) \(\Rightarrow m_{Fe_2O_3}=x=0,15\cdot160=24\left(g\right)\)
Đúng 2
Bình luận (0)
Thực hiện phản ứng giữa 8 mol H2 và 6 mol N2 với bột sắt làm xúc tác. Hỗn hợp sau phản ứng cho qua dung dịch H2SO4 loãng dư còn lại 12 mol khí. Tính hiệu suất phản ứng. (Thể tích các khí đo ở cùng điều kiện nhiệt độ và áp suất) A. 24%. B. 36% C. 18,75% D. 35,5%
Đọc tiếp
Thực hiện phản ứng giữa 8 mol H2 và 6 mol N2 với bột sắt làm xúc tác. Hỗn hợp sau phản ứng cho qua dung dịch H2SO4 loãng dư còn lại 12 mol khí. Tính hiệu suất phản ứng. (Thể tích các khí đo ở cùng điều kiện nhiệt độ và áp suất)
A. 24%.
B. 36%
C. 18,75%
D. 35,5%
Trong phòng thí nghiệm người ta điều chế sắt bằng cách dùng khí hiđrô khử Fe2o3. Sắt mới điều chế cho phản ứng với axit h2so4 loãng có dư. Sau cùng thì thu đc 3 lít khí hiđrô (đktc). Tính hiệu suất phản ứng tạo ra sắt.