Hai bình có thể tích V1 vàV2 = 2V1 được nối với nhau bởi một ống nhỏ cách nhiệt, chứa ôxi ở áp suất 105Pa và 27oC. Sau đó cho bình V1 giảm nhiệt xuống 0oC, bình V2 tăng 57oC. Tính áp suất của khí trong bình.

Những câu hỏi liên quan
Hai bình A và B lần lượt có thể tích V1 và V2 (V1 2V2) được nối với nhau bằng một ống nhỏ, trong ống có một cái van. Van chỉ mở khi độ chênh lệch áp suất hai bên là p bằng 1,1 atm. Ban đầu bình A chưa khí lí tưởng ở nhiệt độ 27oC, áp suất 1 atm, trong bình B là chân không. Người ta nung nóng hai bình lên đến 127oC. Xem thể tích hai bên là không đổi.A. tính nhiệt độ khi van mởb. tính áp suất cuối cùng trong mỗi bình
Đọc tiếp
Hai bình A và B lần lượt có thể tích V1 và V2 (V1 = 2V2) được nối với nhau bằng một ống nhỏ, trong ống có một cái van. Van chỉ mở khi độ chênh lệch áp suất hai bên là p > bằng 1,1 atm. Ban đầu bình A chưa khí lí tưởng ở nhiệt độ 27oC, áp suất 1 atm, trong bình B là chân không. Người ta nung nóng hai bình lên đến 127oC. Xem thể tích hai bên là không đổi.
A. tính nhiệt độ khi van mở
b. tính áp suất cuối cùng trong mỗi bình
Hai bình A và B lần lượt có thể tích V1V2 được nối với nhau bằng một ống nhỏ, trong ống có một cái van. Van chỉ mở khi độ chênh lệch áp suất hai bên là p 1,1 atm. Ban đầu bình A chưa khí lí tưởng ở nhiệt độ 27oC, áp suất 1 atm, trong bình B là chân không. Người ta nung nóng hai bình lên đến 107oC. Xem thể tích hai bên là không đổi. tính áp suất cuối cùng trong mỗi bình.
Đọc tiếp
Hai bình A và B lần lượt có thể tích V1=V2 được nối với nhau bằng một ống nhỏ, trong ống có một cái van. Van chỉ mở khi độ chênh lệch áp suất hai bên là p =1,1 atm. Ban đầu bình A chưa khí lí tưởng ở nhiệt độ 27oC, áp suất 1 atm, trong bình B là chân không. Người ta nung nóng hai bình lên đến 107oC. Xem thể tích hai bên là không đổi. tính áp suất cuối cùng trong mỗi bình.
Có hai bình chứa hai loại khí khác nhau có thể tích lần lượt là
V
1
3
lít và
V
2
4
,
5
lít. Các bình được nối thông với nhau bằng một ống nhỏ có khóa K. Ban đầu, khóa K đóng, áp suất trong các bình là
p
1
1
,
6
a
t
và
p
2...
Đọc tiếp
Có hai bình chứa hai loại khí khác nhau có thể tích lần lượt là V 1 = 3 lít và V 2 = 4 , 5 lít. Các bình được nối thông với nhau bằng một ống nhỏ có khóa K. Ban đầu, khóa K đóng, áp suất trong các bình là p 1 = 1 , 6 a t và p 2 = 3 , 4 a t . Mở khóa K nhẹ nhàng để khí trong hai bình thông với nhau sao cho nhiệt độ không đổi, tính áp suất của hỗn hợp khí khi đó. Coi hai khí không xảy ra tác dụng hóa học khi tiếp xúc.
Khi khóa K mở (bình đã thông nhau). Gọi p 1 ' và p 2 ' là áp suất riêng phần của chất khí thứ nhất và thứ hai.
Khi đó áp suất của hỗn hợp khí trong bình là:
p = p 1 ' + p 2 ' (1)
Xét chất khí trong bình A và B khi khóa K đóng và mở.
Theo định luật Bôi-lơ – Ma-ri-ốt ta có:
p 1 V 1 = p 1 ' ( V 1 + V 2 )
⇒ p 1 ' = p 1 V 1 V 1 + V 2 (2)
p 2 V 2 = p 2 ' ( V 1 + V 2 )
⇒ p 2 ' = p 2 V 2 V 1 + V 2 (3)
Thay (2) và (3) vào (1) ta được:
p = p 1 ' + p 2 ' = p 1 V 1 + p 2 V 2 V 1 + V 2
= 1 , 6.3 + 3 , 4.4 , 5 3 + 4 , 5 = 2 , 68 a t
Đúng 0
Bình luận (0)
Hai bình có thể tích
V
1
40
l
í
t
,
V
2
10
l
í
t
thông với nhau bằng một ống có khóa ban đầu đóng. Khóa này chỉ mở nếu
p
1
≥
p
2
+
10
5
P...
Đọc tiếp
Hai bình có thể tích V 1 = 40 l í t , V 2 = 10 l í t thông với nhau bằng một ống có khóa ban đầu đóng. Khóa này chỉ mở nếu p 1 ≥ p 2 + 10 5 P a ; p 1 , p 2 là áp suất khí trong hai bình. Ban đầu bình 1 chứa khí ở áp suất p 0 = 0 , 9 . 10 5 P a và nhiệt độ T 0 = 300 K . Trong bình 2 là chân không. Người ta nung nóng đều hai bình từ T 0 đến T 0 = 500 K . Tới nhiệt độ nào thì khóa mở? Tính áp suất cuối cùng trong bình 2 ?. Chọn đáp án đúng.
A. T m = 593 K , p = 0 , 9 . 10 5 P a .
B. T m = 583 K , p = 0 , 9 . 10 5 P a .
C. T m = 333 K , p = 0 , 4 . 10 5 P a .
D. T m = 383 K , p = 0 , 6 . 10 5 P a .
Chọn D.
Khóa mở: p1 = pm = 105 Pa
Đối với bình 1 quá trình diễn ra trước khi K mở là quá trình đẳng tích.
![]()
Chênh lệch áp suất hai bên sau khi K mở: ∆p = 105 Pa
Bình 1 ban đầu: p0.V1 = ν.R.T0
Sau khi khóa K mở: (p + ∆p).V1 = ν1.R.T
Ở bình 2 sau khi K mở ta có: p.V2 = ν2.R.T
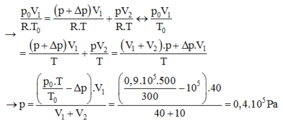
Mặt khác: ν = ν1 + ν2
Đúng 0
Bình luận (0)
Một bình được nạp khí ở nhiệt độ 57 o C dưới áp suất 280kPa. Sau đó bình được chuyển đến một nơi có nhiệt độ 86 o C . Tính độ tăng áp suất của khí trong bình.
Ta có T 1 = 273 + 57 = 330 o K ;
T 2 = 273 + 86 = 359 o K .
Theo định luật Sác-lơ: p 1 T 1 = p 2 T 2
⇒ p 2 = T 2 T 1 p 1 = 359 330 .280
= 304 , 6 k P a .
Độ tăng áp suất:
Δ p = p 2 − p 1 = 304 , 6 − 280
= 24 , 6 k P a .
Đúng 1
Bình luận (0)
Hai bình có thể tích lần lượt là
V
1
40
l
,
V
2
10
l
thông nhau qua một cái van. Van chỉ mở khi áp suất trong bình 1 lớn hơn trong bình 2 từ
10
5
P
a
trở lên. Ban đầu bình 1 chứa khí ở áp suất
p
0
0
,
9
....
Đọc tiếp
Hai bình có thể tích lần lượt là V 1 = 40 l , V 2 = 10 l thông nhau qua một cái van. Van chỉ mở khi áp suất trong bình 1 lớn hơn trong bình 2 từ 10 5 P a trở lên. Ban đầu bình 1 chứa khí ở áp suất p 0 = 0 , 9 . 10 5 P a và nhiệt độ T 0 = 300 K , còn bình 2 là chân không. Người ta làm nóng đều cả hai bình từ nhiệt độ T 0 lên nhiệt độ T = 500 K . Tính áp suất cuối cùng trong mỗi bình.
A. p 2 = 4 . 10 5 P a
B. p 2 = 0 , 9 . 10 5 P a
C. p 2 = 0 , 54 . 10 5 P a
D. p 2 = 0 , 4 . 10 5 P a
Chọn D.
Tới nhiệt độ nào thì van mở:
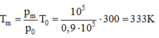
Bắt đầu từ nhiệt độ Tm áp suất trong bình 1 tăng nhanh hơn trong bình 2, nhưng khi hiệu áp suất vượt quá 105 Pa thì van lại mở. Van giữ cho hiệu áp suất là 105 Pa trong quá trình tăng nhiệt độ cho đến khi T = 500 K. Khi đó:
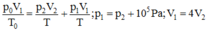
Ta có p1 = 1,4.105 Pa , từ đó rút ra p2 = 0,4.105 Pa
Đúng 0
Bình luận (0)
bơm khí nitơ vào một bình thép có thể tích cố định V1=8,31 đến áp suất p1=15at ở nhiệt độ 27C. Sau đó hơ nóng bình khí này đến nhiệt độ 127C ta có áp suất p2. Khối lượng của khối khí Nitơ và áp suất lúc sau tính được là bao nhiêu?
mọingười giúp em câu nàyvới giải chi tiết ra hộ em
Một bình kín chứa khí ôxi ở nhiệt độ 270C và áp suất 105Pa. Nếu đem bình phơi nắng ở nhiệt độ 1770C thì áp suất trong bình sẽ là bao nhiêu?
Ta có
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\\ \Rightarrow p_2=\dfrac{10^5.450}{300}=15.10^4Pa\)
Đúng 4
Bình luận (0)
Hai bình có thể tích lần lượt là thông nhau qua một cái van . Van chỉ mở khi áp suất trong bình 1 lớn hơn trong bình 2 từ 105Pa trở lên. Ban đầu bình 1 chứa khí ở áp suất và nhiệt độ
T
o
300 K , còn bình 2 là chân không. Người ta làm nóng đều cả hai bình từ nhiệt độ
T
o
lên nhiệt độ T 500K . Tính áp suất cuối cùng trong mỗi bình. A. B. C. D.
Đọc tiếp
Hai bình có thể tích lần lượt là ![]() thông nhau qua một cái van
thông nhau qua một cái van
. Van chỉ mở khi áp suất trong bình 1 lớn hơn trong bình 2 từ 105Pa trở lên. Ban đầu bình 1 chứa khí ở áp suất ![]()
và nhiệt độ T o = 300 K ,
còn bình 2 là chân không. Người ta làm nóng đều cả hai bình từ nhiệt độ T o lên nhiệt độ T = 500K . Tính áp suất cuối cùng trong mỗi bình.
A. ![]()
B. ![]()
C. ![]()
D. ![]()
Đáp án D
Tới nhiệt độ nào thì van mở:
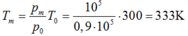
Bắt đầu từ nhiệt độ T m áp suất trong bình 1 tăng nhanh hơn trong bình 2,
nhưng khi hiệu áp suất vượt quá 105Pa thì van lại mở. Van giữ cho hiệu áp suất là 105Pa trong quá trình tăng nhiệt độ cho đến khi T = 500K. Khi đó:
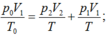
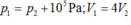
Ta có ![]() , từ đó rút ra
, từ đó rút ra ![]()
Đúng 0
Bình luận (0)











