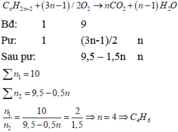Cho ankan A và O2 (trong đó A chiếm 1/10 thể tích)vào bình kín thì áp suất trong bình là 2atm. Đốt hh khì, spu ngưng tụ hơi nc rồi đưa bình về nhiệt độ đầu thì áp suất còn là 1,4 atm.Xđ CTPT

Những câu hỏi liên quan
cho hỗn hợp gồm ankan A và O2 (trong đó A chiếm mười phần trăm về thể tích ) vào bình kín thi suất trong bình là 2atm. Đốt cháy hỗn hợp khí sau phản ứng ngưng tụ hơi nước rồi đưa bình về nhiệt độ ban đầu thì áp suất còn lại là 1.4 atm. Xác định công thức phân tử của A
Giả sử số mol hỗn hợp ban đầu là 1 mol
--> nA=0,9(mol) , nO2=0,1(mol)
pt CnH2n+2 + (3n+1)/2 O2 ---> nCO2 + (n+1)H2O (*)
Từ (*) => nA phản ứng là 0,2/(3n+1) mol, nCO2 = 0,2n/(3n+1) mol
Số mol hh sau phản ứng là 0,9 - 0,2/(3n+1) + 0,2n/(3n+1) mol
Áp dụng pt trạng thái Vp=nRT ta có
n hh ban dau/ n hh sau phản ứng = p1/p2 = 2/1,4
tức là 1/(0,9 - 0,2/(3n+1) + 0,2n/(3n+1)) = 2/1,4
biến đổi đại số tìm được n.
Nếu ko tìm được n thì đề bài có vấn đề.
Mình tìm ra n = 0, nếu sửa đề bài là áp suất bình sau phản ứng là 1,8 atm thì kết quả là CH4
Đúng 0
Bình luận (0)
Một hỗn hợp gồm ankađien X và O2 lấy dư (O2 chiếm 90% thể tích) được nạp đầy vào một bình kín ở áp suất 2 atm. Bật tia lửa điện để đốt cháy hết X rồi đưa bình về nhiệt độ ban đầu cho hơi nước ngưng tụ hết thì áp suất giảm 0,5 atm. Công thức phân tử của X là: A. C3H4 B. C6H10. C. C4H6 D. C5H8
Đọc tiếp
Một hỗn hợp gồm ankađien X và O2 lấy dư (O2 chiếm 90% thể tích) được nạp đầy vào một bình kín ở áp suất 2 atm. Bật tia lửa điện để đốt cháy hết X rồi đưa bình về nhiệt độ ban đầu cho hơi nước ngưng tụ hết thì áp suất giảm 0,5 atm. Công thức phân tử của X là:
A. C3H4
B. C6H10.
C. C4H6
D. C5H8
Một hỗn hợp gồm ankađien X và O2 lấy dư (O2 chiếm 90% thể tích) được nạp đầy vào một bình kín ở áp suất 2 atm. Bật tia lửa điện để đốt cháy hết X rồi đưa bình về nhiệt độ ban đầu cho hơi nước ngưng tụ hết thì áp suất giảm 0,5 atm. Công thức phân tử của X là A. C4H6 B. C6H10 C. C3H4 D. C5H8
Đọc tiếp
Một hỗn hợp gồm ankađien X và O2 lấy dư (O2 chiếm 90% thể tích) được nạp đầy vào một bình kín ở áp suất 2 atm. Bật tia lửa điện để đốt cháy hết X rồi đưa bình về nhiệt độ ban đầu cho hơi nước ngưng tụ hết thì áp suất giảm 0,5 atm. Công thức phân tử của X là
A. C4H6
B. C6H10
C. C3H4
D. C5H8
Trong 1 bình kín chứa hơi chất hữu cơ X(CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139,9oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Đọc tiếp
Trong 1 bình kín chứa hơi chất hữu cơ X(CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139,9oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là
A. C2H4O2
B. C3H6O2
C. C4H8O2
D. C5H10O2
Chọn đáp án B
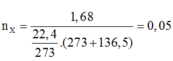
Nhận xét: tất cả các chất trong X đều có công thức dạng C H 2 n O 2
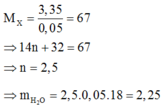
Đúng 0
Bình luận (0)
Trong 1 bình kín chứa hơi chất hữu cơ X (CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139,9oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Đọc tiếp
Trong 1 bình kín chứa hơi chất hữu cơ X (CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139,9oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là
A. C2H4O2
B. C3H6O2
C. C4H8O2
D. C5H10O2
Đáp án B
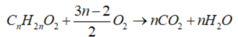
→ n t r = 2 x + 2 x 3 n - 2
n s = 2 x - x + 2 . 2 n x 3 n - 2
n t r n s = p t r p s = 16 19
⇔ 2 x + 2 x 3 n - 2 x + 4 n x 3 n - 2 = 16 19 ⇔ n = 3
⇒ X l à C 3 H 6 O 2
Đúng 0
Bình luận (0)
Trong 1 bình kín chứa hơi chất hữu cơ X (CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139,9oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Đọc tiếp
Trong 1 bình kín chứa hơi chất hữu cơ X (CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139,9oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là
A. C2H4O2
B. C3H6O2
C. C4H8O2
D. C5H10O2
Cho vào bình kín thể tích không đổi 0,2 mol NO và 0,3 mol O2, áp suất trong bình là P1. Sau khi phản ứng hoàn toàn đưa bình về nhiệt độ ban đầu thì áp suất là P2. Tỉ lệ của P1 và P2 là: A. P1 1,25P2 B. P1 0,8P2 C. P1 2P2 D. P1 P2
Đọc tiếp
Cho vào bình kín thể tích không đổi 0,2 mol NO và 0,3 mol O2, áp suất trong bình là P1. Sau khi phản ứng hoàn toàn đưa bình về nhiệt độ ban đầu thì áp suất là P2. Tỉ lệ của P1 và P2 là:
A. P1 = 1,25P2
B. P1 = 0,8P2
C. P1 = 2P2
D. P1 = P2
Đáp án A
2NO+ O2 → 2NO2
Tổng số mol khí trước phản ứng là n1= 0,2+ 0,3= 0,5 mol
Ta có 0,2/2 < 0,3/1 nên NO phản ứng hết và O2 còn dư
2NO+ O2 → 2NO2
Trước pứ: 0,2 0,3 mol
Phản ứng: 0,2 0,1 0,2 mol
Sau pứ: 0 0,2 0,2 mol
Số mol khí sau phản ứng là n2= nO2+ nNO2= 0,4 mol
Do sau khi phản ứng đưa bình về nhiệt độ ban đầu nên tỉ lệ về áp suất chính là tỉ lệ về số mol.
Ta có P1/P2= n1/n2=0,5/0,4=1,25 → P1= 1,25P2
Đúng 0
Bình luận (0)
trong một bình kín dung tích ko đổi chứa hỗn hợp hơi chất A (CxHyO) với O2 vừa đủ để đốt cháy hợp chất A ở 136,5 độ C và 1 atm. Sau khi đốt cháy, đưa bình về nhiệt độ ban đầu, thì áp suất trong bình là 1,2 atm. Mặt khác, khi đốt cháy 0,03 mol A lượng CO2 sinh ra được cho vô 400ml dd Ba(OH)2 0,15M thấy có hiện tượng hòa tan kết tủa, nhưng nếu cho vô 800ml dd Ba(OH)2 nói trên thì thấy Ba(OH)2 dư. Tìm ctpt A
Đọc tiếp
trong một bình kín dung tích ko đổi chứa hỗn hợp hơi chất A (CxHyO) với O2 vừa đủ để đốt cháy hợp chất A ở 136,5 độ C và 1 atm. Sau khi đốt cháy, đưa bình về nhiệt độ ban đầu, thì áp suất trong bình là 1,2 atm. Mặt khác, khi đốt cháy 0,03 mol A lượng CO2 sinh ra được cho vô 400ml dd Ba(OH)2 0,15M thấy có hiện tượng hòa tan kết tủa, nhưng nếu cho vô 800ml dd Ba(OH)2 nói trên thì thấy Ba(OH)2 dư. Tìm ctpt A
Trong một bình kín dung tích không đổi chứa hỗn hợp hơi chất X (CxHyO) với O2 vừa đủ để đốt cháy hợp chất X ở 136,5oC và?
Đúng 0
Bình luận (0)
Este E no, đơn chức, mạch hở. Trong một bình kín chứa hơi E và khí O2 (dùng gấp đôi lượng cần phản ứng) ở nhiệt độ 109,2oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn E rồi đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. Công thức phân tử của E là A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Đọc tiếp
Este E no, đơn chức, mạch hở. Trong một bình kín chứa hơi E và khí O2 (dùng gấp đôi lượng cần phản ứng) ở nhiệt độ 109,2oC, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn E rồi đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. Công thức phân tử của E là
A. C2H4O2
B. C3H6O2
C. C4H8O2
D. C5H10O2
Chọn đáp án B
đốt E dạng C n H 2 n O 2 + 3 n - 2 2 O 2 → t o n C O 2 + n H 2 O
chọn n E = 1 m o l
⇒ n O 2 t r o n g b ì n h = 2 n O 2 c ầ n = 3 n - 2 m o l
điều kiện cùng T và V ⇒ n s a u : n t r ư ớ c = p s a u : p t r ư ớ c = 0 , 95 : 0 , 8
⇒ n s a u = 1 , 1875 × 3 n - 1 m o l = ∑ n C O 2 + n H 2 O + n O 2 c ò n d ư
⇄ 2n + (3n – 2) ÷ 2 = 1,1875 × (3n – 1)
⇒ n = 3 → CTPT của E là C 3 H 6 O 2 .
Đúng 0
Bình luận (0)