Đốt 13,7 ml hh A gồm CH4,C3H8,CO ta thu đc 25,7 ml khí CO2 (CÙNG ĐK) .tính % thể tích propan trong hh A

Những câu hỏi liên quan
Đốt cháy hết 30ml hh C3H8 và C4H10 thu được 100ml CO2. Tính: a/ %(V) mỗi khí trong hh. b/ VKK (chứa 20% VO2) cần phản ứng. Biết các thể tích khí đo ở cùng đk t° và P.
Đốt cháy 11.1555 lít hh khí CH4 và C2H6 thu đc 16.1135 lít CO2. (đkc) Tính % thể tích mỗi lhi1 trong hh ban đầu
Gọi \(n_{CH_4}=a\left(mol\right)\) và \(n_{C_2H_6}=b\left(mol\right)\)
\(n_{hh}=\dfrac{11,1555}{22,4}=0,5\)
\(\Rightarrow a+b=0,5\left(1\right)\)
\(n_{CO_2}=\dfrac{16,1135}{22,4}=0,72mol\)
Bảo toàn C: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_6}=a+2b=0,72\left(2\right)\)
Từ (1) và (2)\(\Rightarrow\left\{{}\begin{matrix}a=0,28mol\\b=0,22mol\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,28}{0,28+0,22}\cdot100\%=56\%\)
\(\%V_{C_2H_6}=100\%-56\%=44\%\)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 20,0 ml hỗn hợp X gồm C3H6, CH4, CO (thể tích CO gấp hai lần thể tích CH4), thu được 24,0 ml CO2 (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất). Tỉ khối của X so với khí H2 là: A. 12,9. B. 25,8. C. 22,2. D. 11,1
Đọc tiếp
Đốt cháy hoàn toàn 20,0 ml hỗn hợp X gồm C3H6, CH4, CO (thể tích CO gấp hai lần thể tích CH4), thu được 24,0 ml CO2 (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất). Tỉ khối của X so với khí H2 là:
A. 12,9.
B. 25,8.
C. 22,2.
D. 11,1
Đặt VC3H6 = a ; VCH4 = b ⇒ VCO = 2b
Có VC3H6 + VCH4 + VCO = Vhỗn hợp = a + 3b = 20 (1)
Áp dụng định luật bảo toàn nguyên tố C có:
VCO2 = 3VC3H6 + VCH4 + VCO ⇒ 24 = 3a + 3b (2)
Từ (1) và (2) ⇒ a = 2 ; b = 6
⇒ nC3H6 : nCH4 : nCO = 2 : 6 : 12 = 1 : 3 : 6
Gỉa sử: nC3H6 = 1 ⇒ nCH4 = 3 ⇒ nCO = 6
MX = ( mC3H6 + mCH4 + mCO ) / nX = (42 + 16.3 + 6.28) / (1+3+6) = 25,8
⇒ dX/H2 = 12,9
Đáp án A
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 20,0 ml hỗn hợp X gồm
C
3
H
6
,
C
H
4
,
C
O
(thể tích CO gấp hai lần thể tích
C
H
4
), thu được 24,0 ml CO2 (các thể tích khí đo cùng ở điều kiện nhiệt độ và áp suất). Tỉ khối của X so với khí hiđro là A. 22,2 B. 25,8 C. 12,9 D. 11,1
Đọc tiếp
Đốt cháy hoàn toàn 20,0 ml hỗn hợp X gồm C 3 H 6 , C H 4 , C O (thể tích CO gấp hai lần thể tích C H 4 ), thu được 24,0 ml CO2 (các thể tích khí đo cùng ở điều kiện nhiệt độ và áp suất). Tỉ khối của X so với khí hiđro là
A. 22,2
B. 25,8
C. 12,9
D. 11,1
Chọn C
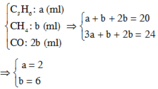
M ¯ = 2.42 + 6.16 + 12.28 20 = 25 , 8 ⇒ d x / H 2 = 25 , 8 2 = 12 , 9
Đúng 0
Bình luận (0)
crackinh propan thu được 8,8 gam hh khí A gồm H2, CH4, C2H6, C3H6 và C3H8 dư. Hiệu xuất p/ứ đạt 90%. Dẫn hh khí A qua dd Brom vừa đủ thì có bao nhiêu gam Brom p/ứ
Có lẽ đề cho C2H4 thay vì C2H6 bạn nhỉ?
Gọi: nC3H8 = x (mol)
H% = 90% ⇒ nC3H8 pư = 0,9x (mol), nC3H8 dư = 0,1x (mol)
\(C_3H_8\rightarrow C_3H_6+H_2\)
a________a______a (mol)
\(C_3H_8\rightarrow C_2H_4+CH_4\)
b_________b______b (mol)
⇒ a + b = 0,9x (1)
Mà: mA = 8,8 (g)
\(\Rightarrow42a+2a+28b+16b+0,1x.44=8,8\)
\(\Rightarrow44a+44b+0,1x.44=8,8\)
\(\Rightarrow a+b=0,2-0,1x\left(2\right)\)
Từ (1) và (2) ⇒ x = 0,2 (mol), a + b = 0,9.0,2 = 0,18 (mol)
Có: \(n_{Br_2}=n_{C_3H_6}+n_{C_2H_4}=a+b=0,18\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,18.160=28,8\left(g\right)\)
Đúng 2
Bình luận (2)
Đốt 28 ml hh metan và exetilen cần dùng 6,72 lít oxi
a) tính % thể tích mỗi khí trong hh
b) tính thể tích CO2 tạo thành
Đốt cháy hoàn toàn 40,0 ml hỗn hợp X gồm C3H6, CH4, CO (số mol CO gấp hai lần số mol CH4), thu được 48 ml CO2 (các thể tích khí được đo ở cùng điều kiện nhiệt độ và áp suất). Tỉ khối của X so với khí hiđro là: A. 25,8 B. 12,9 C. 22,2 D. 11,1
Đọc tiếp
Đốt cháy hoàn toàn 40,0 ml hỗn hợp X gồm C3H6, CH4, CO (số mol CO gấp hai lần số mol CH4), thu được 48 ml CO2 (các thể tích khí được đo ở cùng điều kiện nhiệt độ và áp suất). Tỉ khối của X so với khí hiđro là:
A. 25,8
B. 12,9
C. 22,2
D. 11,1
Đốt cháy 50ml hh CH4 và C2H2 cần 110ml khí O2. Tính: a/ %(V) mỗi khí trong hh b/ Thể tích CO2 sinh ra các khí đo ở cùng điều kiện t° và P (áp suất)
Giả sử các khí đo ở điều kiện sao cho 1 mol khí chiếm thể tích V lít
Gọi số mol CH4, C2H2 là a, b (mol)
=> \(a+b=\dfrac{0,05}{V}\) (1)
\(n_{O_2}=\dfrac{0,11}{V}\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a-->2a---------->a
2C2H2 + 5O2 --to--> 4CO2 + 2H2O
b--->2,5b-------->2b
=> \(2a+2,5b=\dfrac{0,11}{V}\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{0,03}{V}\left(mol\right)\\b=\dfrac{0,02}{V}\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{\dfrac{0,03}{V}.V}{0,05}.100\%=60\%\\\%V_{C_2H_2}=\dfrac{\dfrac{0,02}{V}.V}{0,05}.100\%=40\%\end{matrix}\right.\)
b) \(n_{CO_2}=a+2b=\dfrac{0,07}{V}\left(mol\right)\)
=> \(V_{CO_2}=\dfrac{0,07}{V}.V=0,07\left(l\right)\)
Đúng 5
Bình luận (0)
Tham khảo:
a)
{VC2H2=x(ml)
VC2H4=y(ml)
⇒ x + y = 50(1)
C2H2+5/2O2(to)→2CO2+H2O
C2H4+3O2(to)→2CO2+2H2O
Theo PTHH : 2,5x + 3y = 140(2)
Từ (1)(2) suy ra: x = 20 ; y = 30
Vậy :
%VC2H2=2050.100%=40%%
VC2H4=100%−40%=60%
b)VCO2=2VC2H2+2VC2H4=2.50=100(ml)
Đúng 3
Bình luận (0)
a)
{VC2H2=x(ml)
VC2H4=y(ml)
⇒ x + y = 50(1)
C2H2+5/2O2(to)→2CO2+H2O
C2H4+3O2(to)→2CO2+2H2O
Theo PTHH : 2,5x + 3y = 140(2)
Từ (1)(2) suy ra: x = 20 ; y = 30
Vậy :
%VC2H2=2050.100%=40%%
VC2H4=100%−40%=60%
b)VCO2=2VC2H2+2VC2H4=2.50=100(ml)
Đúng 0
Bình luận (0)
Đốt cháy 3,36l hh khí CH4 và C2H4 thu được 4,48l khí CO2
a)Tính TPPT thể tích mỗi khí trong hh ban đầu.Biết các khí đo ở (đktc).
b)Dẫn hh khí qua bình đựng dd Br2 tính khối lượng Br2 đã tham gia phản ứng .
Xem chi tiết
\(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\end{matrix}\right.\)\(\Rightarrow a + b = \dfrac{3,36}{22,4} = 0,15(1) \)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ n_{CO_2} = a + 2b = \dfrac{4,48}{22,4} = 0,2(2)\)
Từ (1)(2) suy ra: a = 0,1 ; b = 0,05
Suy ra:
\(\%V_{CH_4} = \dfrac{0,1}{0,15}.100\% = 66,67\%\\ \%V_{C_2H_4} = 100\% - 66,67\% = 33,33\%\)
b)
\(C_2H_4 + Br_2 \to C_2H_4Br_2\\ n_{Br_2} = n_{C_2H_4} = 0,05(mol)\\ \Rightarrow m_{Br_2} = 0,05.160 = 8\ gam\)
Đúng 2
Bình luận (0)




















