Cho 8,16 gam hh X gồm (Fe, FeO, Fe2O3 và Fe3O4 phản ứng với dd HNO3 (dd Y) thu được 1,344 lít khí NO (đktc) và dd Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, tạo ra khí NO. Tính số mol của HNO3 trong Y.

Những câu hỏi liên quan
Cho 8,16 gam hỗn hợp X gồm Fe, FeO,
F
e
3
O
4
v
à
F
e
2
O
3
tan hết trong dung dịch
H
N
O
3
loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, N...
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, F e 3 O 4 v à F e 2 O 3 tan hết trong dung dịch H N O 3 loãng (dung dịch Y), thu được
1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N 5 + . Số mol H N O 3 có trong Y là
A. 0,78 mol
B. 0,54 mol
C. 0,50 mol
D. 0,44 mol
Đáp án C
Fe + ddZ → khí NO => X chứa H N O 3 dư. Quy X về Fe và O
Trong X, đặt ![]()
Bảo toàn electron:
![]()
Giải hệ có: x = 0,12 mol; y = 0,09 mol
Xét cả quá trình : do hòa tan tối đa Fe => Fe chỉ lên số oxi hóa +2.
Xét cả quá trình : do hòa tan tối đa Fe => Fe chỉ lên số oxi hóa +2.
![]()
![]()
![]()
Đúng 0
Bình luận (0)
Cho 8,16 gam hỗn hợp X gồm Fe, FeO,
F
e
3
O
4
và
F
e
2
O
3
phản ứng hết với dung dịch
H
N
O
3
loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm...
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, F e 3 O 4 và F e 2 O 3 phản ứng hết với dung dịch H N O 3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N + 5 . Số mol H N O 3 có trong Y là
A. 0,50 mol.
B. 0,78 mol.
C. 0,54 mol.
D. 0,44 mol.
Đ á p á n A + X ↔ F e O ⇒ m X = 56 n F e + 16 n O 2 = 8 , 16 B T e : 3 n F e = 2 n O + 3 . n N O = 0 , 18 ⇒ n F e = 0 , 12 n O = 0 , 09 X é t t o à n q u á t r ì n h : F e → 0 F e + 2 B T e : 2 . n F e ⏟ 0 , 09 + 0 , 12 = 3 . n N O + 2 n O ⏟ 0 , 09 B T N T N : n H N O 3 = 2 n F e N O 3 2 + n N O ⇒ n N O = 0 , 08 n O = 0 , 5
Đúng 0
Bình luận (0)
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với dung dịch HNO3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là A. 0,78 mol B. 0,54 mol C. 0,50 mol D. 0,44 mol
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với dung dịch HNO3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là
A. 0,78 mol
B. 0,54 mol
C. 0,50 mol
D. 0,44 mol
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với dung dịch HNO3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là : A. 0,78 mol. B. 0,54 mol. C. 0,50 mol. D. 0,44 mol.
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với dung dịch HNO3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là :
A. 0,78 mol.
B. 0,54 mol.
C. 0,50 mol.
D. 0,44 mol.
Chọn C.
X → ← q u ỳ t í m F e O ⇒ 56 n F e + 16 n O = 8 , 16 3 n F e = 2 n O + 3 n O 0 , 06 ⇒ n F e = 0 , 12 n O = 0 , 09 2 n F e = 3 n O + 2 n O 0 , 09 + 0 , 12 ? 0 , 09 n H N O 3 = 2 n F e + n O n N O = 0 , 08 n H N O 3 = 0 , 5
Đúng 0
Bình luận (0)
Cho 8,16 gam hỗn hợp X gồm Fe, FeO,
Fe
3
O
4
và
Fe
2
O
3
phản ứng hết với dung dịch
HNO
3
loãng, thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của
N...
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe 3 O 4 và Fe 2 O 3 phản ứng hết với dung dịch HNO 3 loãng, thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N + 5 . Số mol HNO 3 đã phản ứng là
A. 0,32
B. 0,78
C. 0,5
D. 0,44
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với dung dịch HNO3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe sinh ra khí NO. Biết trong ác phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là
Quy hỗn hợp về Fe và O với số mol lần lượt là a;b
$\Rightarrow 56a+16b=8,16$
Bảo toàn e ta được $3a-2b=0,06.3$
Giải hệ ta được $a=0,12;b=0,09$
Bảo toàn e cho phản ứng (2) ta có: $n_{NO}=0,02(mol)\Rightarrow n_{H^+/du}=0,08(mol)$
Dùng phương trình $H^+$ suy ra $n_{HNO_3}=0,5(mol)$
Đúng 2
Bình luận (0)
Coi hỗn hợp X gồm : Fe , O
\(n_{Fe}=a\left(mol\right),n_O=b\left(mol\right)\)
\(m_X=56a+16b=8.16\left(g\right)\left(1\right)\)
\(n_{NO}=\dfrac{1.344}{22.4}=0.06\left(mol\right)\)
\(\text{Bảo toàn e : }\)
\(3a=2b+3\cdot0.06\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.12,b=0.09\)
\(\text{Bảo toàn e cho cả quá trình : }\)
\(2n_{Fe}=3n_{NO\left(1\right)}+2n_{NO\left(2\right)}\)
\(\Rightarrow n_{NO\left(2\right)}=0.08\)
\(n_{HNO_3}=0.5\left(mol\right)\)
Đúng 1
Bình luận (0)
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với dung dịch HNO3 loãng (dung dịch Y), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe sinh ra khí NO. Biết trong ác phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là
Quy hỗn hợp về Fe và O với số mol lần lượt là a;b(mol)
$\Rightarrow 56a+16b=8,16$
Bảo toàn e ta được $3a-2b=0,06.3$
Giải hệ ta được $a=0,12'b=0,09$
Bảo toàn e cho phản ứng (2) ta có:
$n_{NO}=0,02(mol)\Rightarrow n_{H^+/dư}=0,08(mol)$
Dùng phương trình $H^+$ suy ra $n_{HNO_3}=0,5(mol)$
Đúng 2
Bình luận (0)
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 tan hết trong dung dịch HNO3 loãng (dung dịch Y) thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hóa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là A. 0,78 mol B. 0,54 mol C. 0,50 mol D. 0,44 mol
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 tan hết trong dung dịch HNO3 loãng (dung dịch Y) thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hóa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là
A. 0,78 mol
B. 0,54 mol
C. 0,50 mol
D. 0,44 mol
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 tan hết trong dung dịch HNO3 loãng (dung dịch Y) thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hóa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là A. 0,78 mol B. 0,54 mol C. 0,50 mol D. 0,44 mol
Đọc tiếp
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 tan hết trong dung dịch HNO3 loãng (dung dịch Y) thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hóa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Số mol HNO3 có trong Y là
A. 0,78 mol
B. 0,54 mol
C. 0,50 mol
D. 0,44 mol
Đáp án C
Bài toán nhỏ “cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 tan hết trong dung dịch HNO3 loãng (dung dịch Y) thu được 1,344 lít NO (đktc) và dung dịch Z” → đủ giả thiết
Quy đổi 8,16 gam X gồm x mol Fe và y mol O → 56x + 16y = 8,16
Do thêm Fe vào Z tiếp tục thu được NO → chứng tỏ HNO3 còn dư trong Z → muối Fe trong Z là muối Fe3+
Bảo toàn electron ta có: 3x = 2y + 0,06.3.
Kết hợp giải hệ được x = 0,12mol, y = 0,09mol
Hòa tan tối đa Fe nên dung dịch sản phẩm cuối cùng chỉ chứa muối sắt II
Gộp cả quá trình → quan sát:
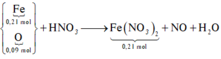
Bảo toàn electron có nNO = (0,21.2 – 0,09.2) : 3 = 0,08mol
Bảo toàn nguyên tố N có số mol HNO3 là 0,08 + 0,21.2 = 0,5mol
Đúng 0
Bình luận (0)












