Hoà tan hoàn toàn một kim loại hoá trị II trong 150ml dd h2so4 0.5M thu được dung dịch X chứa 7.2 g muối . Để trung hoà axit dư trong dd X , phải dùng hết 30ml dd NaOH 1M . kim loại do là

Những câu hỏi liên quan
Hòa tan 1,44 gam một kim loại hóa trị II trong 150ml dung dịch H2SO4 0,5M. Muốn trung hòa axit dư trong dung dịch thu được, phải dùng hết 30ml dung dịch NaOH 1M. Kim loại đó là
A. Ba.
B. Ca.
C. Mg.
D. Be.
\(KL:A\left(II\right)\\ n_{H_2SO_4}=0,15.0,5=0,075\left(mol\right)\\n_{NaOH}=0,03.1=0,03\left(mol\right)\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4 +2H_2O\left(1\right)\\ A+H_2SO_4\rightarrow ASO_4+H_2\left(2\right)\\n_{H_2SO_4\left(1\right)}=\dfrac{0,03}{2}=0,015\left(mol\right)\\ n_{H_2SO_4\left(2\right)}=0,075-0,015=0,06\left(mol\right)=n_A\\ \Rightarrow M_A=\dfrac{1,44}{0,06}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Magie\left(Mg=24\right)\\ \Rightarrow C\)
Đúng 0
Bình luận (0)
Hòa tan 1,44 gam một kim loại hóa trị II trong 150ml dung dịch H2SO4 0,5M. Muốn trung hòa axit dư trong dung dịch thu được, phải dùng hết 30ml dung dịch NaOH 1M. Kim loại đó là :
A. Ba.
B. Ca.
C. Mg.
D. Be.
Đáp án C.
Gọi kim loại cần tìm là R. Các PTHH:
R + H2SO4 → RSO4 +H2 (1)
H2SO4 + 2NaOH → Na2SO4 + H2O (2)
Số mol H2SO4 là nH2SO4 = 0,15.0,5 = 0,075 (mol);
Số mol NaOH là nNaOH = 0,03.1 = 0,03 (mol)
Theo pt (2) 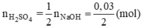
Số mol H2SO4 phản ứng (1) là:
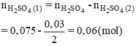
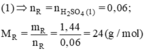
Vậy R là Mg.
Đúng 0
Bình luận (0)
Hòa tan 1,44g một kim loại hóa trị II trong 150ml axit H2SO4 0,5M. Để trung hòa axit dư phải dùng 30ml dung dịch NaOH 1M. Xác định kim loại đó? A. Ba B. Ca C. Mg D. Be
Đọc tiếp
Hòa tan 1,44g một kim loại hóa trị II trong 150ml axit H2SO4 0,5M. Để trung hòa axit dư phải dùng 30ml dung dịch NaOH 1M. Xác định kim loại đó?
A. Ba
B. Ca
C. Mg
D. Be
Đáp án C
nH+ pứ KL = 2nH2SO4 – nNaOH = 0,12 mol = 2nKL
=> nKL = 0,06 mol => MKL = 24g (Mg)
Đúng 0
Bình luận (0)
Cho 1,44g một kim loại R có hoá trị II phản ứng hoàn toàn trong 250ml dung dịch H2SO4 0,3M. Dung dịch thu được còn chứa axit dư và phải trung hoà axit dư bằng 60ml dung dịch NaOH 0,5M. Hãy xác định kim loại R
\(n_{NaOH}=0.06\cdot0.5=0.03\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\dfrac{0.03}{2}=0.015\left(mol\right)\)
\(n_{H_2SO_4\left(pư\right)}=0.25\cdot0.3-0.015=0.06\left(mol\right)\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
\(0.06....0.06\)
\(M_R=\dfrac{1.44}{0.06}=24\left(\dfrac{g}{mol}\right)\)
\(R:Mg\)
Đúng 3
Bình luận (0)
n NaOH = 0,06.0,5 = 0,03(mol)
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
n H2SO4 dư = 1/2 n NaOH = 0,015(mol)
n H2SO4 pư = 0,25.0,3 - 0,015 = 0,06(mol)
$R + H_2SO_4 \to RSO_4 + H_2$
n R = n H2SO4 pư = 0,06(mol)
M R = 1,44/0,06 = 24(Mg)
Vậy R là Magie
Đúng 3
Bình luận (0)
Hoà tan hoàn toàn 1,44g kim loại có hoá trị 2 vào 250ml dd H2SO4 0,3 M, sau đó thêm tiếp 60ml dd KOH 0,5M để trung hoà hết lượng axit còn dư .Kim loại ?
Gọi kim loại cần tìm là R
\(n_{H_2SO_4}=0,25.0,3=0,075\left(mol\right)\)
\(n_{KOH}=0,06.0,5=0,03\left(mol\right)\)
PTHH: R + H2SO4 --> RSO4 + H2
0,06<--0,06
2KOH + H2SO4 --> K2SO4 + 2H2O
0,03-->0,015
=> \(M_R=\dfrac{1,44}{0,06}=24\left(g/mol\right)\)
=> R là Mg
Đúng 4
Bình luận (0)
Số mol H2SO4 và KOH lần lượt là 0,3.0,25=0,075 (mol) và 0,5.0,06=0,03 (mol).
Số mol H2SO4 phản ứng là (0,075.2-0,03):2=0,06 (mol) và bằng số mol của kim loại ban đầu.
Nguyên tử khối của kim loại cần tìm là 1,44:0,06=24 (g/mol).
Vậy kim loại đã cho là magie (Mg).
Đúng 0
Bình luận (0)
Hoà tan 3,2g Oxit kim loại hoá trị III bằng 200g dung dịch H2SO4 loãng. Khi thêm vào hoà tan 1 oxit kim loai htri IV biết rằng hoà tan 8g oxit này bằng 300ml dd H2SO4 1M. sau p/ứ trung hoà lượng axit còn dư bằng 50g dd NaOH 24%. tìm cthỗn hợp sau phản ứng 1 lượng CaCO3 vừa đủ thấy 0,0224dm3 CO2 ở đktc sau đó cô cạn dung dịch thu được 9,36g muối sunfat khô. Tìn công thức õit kim loại và C% H2SO4
R là một kim loại có hoá trị II. Đem hoà tan hoàn toàn a g oxit của kim loại này vào 48 g ddH2SO4 6,125% tạo thành dd A có chứa 0,98% H2SO4.Khi dùng 2,8 lít cacbon (II) oxit để khử hoàn toàn a g oxit trên thành kim loại, thu được khí B.Nếu lấy 0,7 lít khí B cho qua dd nước vôi trong (dư) làm tạo ra 0,625g kết tủa. 1. Tính a và khối lượng của R, biết rằng các phản ứng xảy ra hoàn toàn, các thể tích khí đềuđo ở đktc. 2. Cho 0,54g bột nhôm vào 20 g dd A, sau khi phản ứng kết thúc lọc tách được m g...
Đọc tiếp
R là một kim loại có hoá trị II. Đem hoà tan hoàn toàn a g oxit của kim loại này vào 48 g dd
H2SO4 6,125% tạo thành dd A có chứa 0,98% H2SO4.
Khi dùng 2,8 lít cacbon (II) oxit để khử hoàn toàn a g oxit trên thành kim loại, thu được khí B.
Nếu lấy 0,7 lít khí B cho qua dd nước vôi trong (dư) làm tạo ra 0,625g kết tủa.
1. Tính a và khối lượng của R, biết rằng các phản ứng xảy ra hoàn toàn, các thể tích khí đều
đo ở đktc.
2. Cho 0,54g bột nhôm vào 20 g dd A, sau khi phản ứng kết thúc lọc tách được m g chất rắn.
Tính m.
Hòa tan hoàn toàn 24 gam một kim loại hóa trị 2 trong 750 ml H2SO4 1M. Để trung hòa axit dư trong dung dịch thu được phải dùng hết 150 ml dung dịch NaOH 2M. xác định kim loại
\(n_{NaOH} = 0,15.2 = 0,3(mol)\\ 2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O\\ n_{H_2SO_4\ dư} = \dfrac{1}{2}n_{NaOH} = 0,15(mol)\\ n_{H_2SO_4\ pư} = 0,75 - 0,15 = 0,6(mol)\\ \)
Gọi kim loại cần tìm là R
\(R + H_2SO_4 \to RSO_4 + H_2\\ n_R = n_{H_2SO_4} = 0,6(mol)\\ \Rightarrow M_R = \dfrac{24}{0,6} =40(Ca)\)
Vậy kim loại cần tìm là Canxi
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 0,8 g một kim loại hoá trị II hoà tan hoàn toàn trong 100 ml H 2 S O 4 0,5 M. Lượng axit còn dư phản ứng vừa đủ với 33,4 ml dung dịch NaOH 1,00 M. Xác định tên kim loại.
Số mol H 2 S O 4 trong 100ml dung dịch 0,5M là :
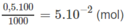
Số mol NaOH trong 33,4 ml nồng độ 1M :
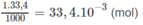
H 2 S O 4 + 2NaOH → N a 2 S O 4 + 2 H 2 O
Lượng H 2 S O 4 đã phản ứng với NaOH :

Số mol H 2 S O 4 đã phản ứng với kim loại là :
5. 10 - 2 - 1.67. 10 - 2 = 3,33. 10 - 2 mol
Dung dịch H 2 S O 4 0,5M là dung dịch loãng nên :
X + H 2 S O 4 → X S O 4 + H 2 ↑
Số mol X và số mol H 2 S O 4 phản ứng bằng nhau, nên :
3,33. 10 - 2 mol X có khối lượng 0,8 g
1 mol X có khối lượng: 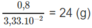
⇒ Mkim loại = 24 g/mol.
Vậy kim loại hoá trị II là magie.
Đúng 0
Bình luận (0)
















